-
汽车尾气中排放的NOx和CO污染环境,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。已知:
①2CO(g)+O2(g)=2CO2(g) ΔH1=-566.0 kJ·mol-1
②N2(g)+O2(g)=2NO(g) ΔH2=+180.5 kJ·mol-1
(1)CO的燃烧热为________。
(2)若1molN2(g)、1molO2(g)分子中化学键断裂时分别需要吸收946 kJ、498 kJ的能量,则1molNO(g)分子中化学键断裂时需吸收的能量为_____kJ(保留到小数点后一位)。
-
汽车尾气中排放的NOx和CO污染环境,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。已知:① 2CO(g)+O2(g) 2CO2(g) ΔH=−566.0 kJ/mol,② N2(g)+O2(g)
2CO2(g) ΔH=−566.0 kJ/mol,② N2(g)+O2(g) 2NO(g) ΔH=+180.5 kJ/mol,③ 2NO(g)+O2(g)
2NO(g) ΔH=+180.5 kJ/mol,③ 2NO(g)+O2(g) 2NO2(g) ΔH=−116.5 kJ/mol。 回答下列问题:
2NO2(g) ΔH=−116.5 kJ/mol。 回答下列问题:
(1)CO的燃烧热为________。若1molN2(g)、1molO2(g)分子中化学键断裂时分别需要吸收946kJ、498kJ的能量,则1molNO(g)分子中化学键断裂时需吸收的能量为______kJ。
(2)CO将NO2还原为单质的热化学方程式为______________。
(3)为了模拟反应2NO(g)+2CO(g) N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如下表:
N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(10-4 mo l·L-1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)/(10-3 mo l·L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
① 前2s内的平均反应速率v(N2)=____________,此温度下,该反应的平衡常数K=____。
② 能说明上述反应达到平衡状态的是__________。
A.2n(CO2)=n(N2) B.混合气体的平均相对分子质量不变
C.气体密度不变 D.容器内气体压强不变
③ 当NO与CO浓度相等时,体系中NO的平衡转化率与温度、压强的关系如图所示,则NO的平衡转化率随温度升高而减小的原因是__________________________________,图中压强(p1,p2、p3)的大小顺序为_______。

-
日常生活中,汽车尾气中排放的NOx和CO污染环境,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。
已知:①2CO(g)+O2(g)  2CO2(g) ΔH= -akJ/mol
2CO2(g) ΔH= -akJ/mol
②N2(g)+O2(g)  2NO(g) ΔH= +bkJ/mol
2NO(g) ΔH= +bkJ/mol
③2NO(g)+O2(g)  2NO2(g) ΔH= -ckJ/mol
2NO2(g) ΔH= -ckJ/mol
回答下列问题:
(1)CO的燃烧热为____________________。
(2)CO将NO2还原为单质的热化学方程式为_____________________________。
(3)为了模拟反应2NO(g)+2CO(g)  N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如下表:
N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(10-4mol/L) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)/(10-3mol/L) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
①前2s内的平均反应速率V(N2)=_________________________________。
②能说明上述反应达到平衡状态的是_______________。
A.2n(CO2)=n(N2)
B.混合气体的平均相对分子质量不变
C.气体密度不变
D.容器内气体压强不变
③当NO与CO浓度相等时,体系中NO的平衡转化率与温度、压强的关系如图所示。
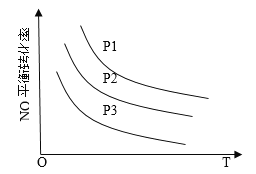
则NO的平衡转化率随温度升高而减小的原因是______________________________
图中压强(P1、P2、P3)的大小顺序为_____________________。
-
汽车尾气中排放的NOx和CO污染环境,在汽车尾气系统装置中安装催化转化器,可有效降低NOx和CO的排放。已知:
①2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ/mol
②N2(g)+O2(g)=2NO(g) △H=+180.5kJ/mol
③2NO(g)+O2(g)=2NO2(g) △H=-116.5kJ/mol
请回答下列问题:
(1)若1molN2(g)、1molNO(g)分子中化学键断裂时分别需要吸收946kJ、631.75kJ的能量,则1molO2(g)分子中化学键成键时需释放的能量为___kJ。
(2)CO与NO2反应生成无毒气体的热化学方程式为___。
(3)为了模拟反应2NO(g)+2CO(g) N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用现代传感技术测得不同时间NO和CO的浓度如下表:
N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用现代传感技术测得不同时间NO和CO的浓度如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(10-4mol・L-1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)/(10-3mol・L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
①前2s的平均反应速率v(N2)=___;此温度下,该反应的平衡常数K=___。
②能说明上述反应达到平衡状态的是____。
a.2v正(CO)=v逆(N2)
b.c(CO)=c(CO2)
c.容器内压强不变
d.混合气体密度不变
e.混合气体的平均相对分子质量不变
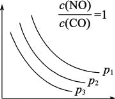
③当NO与CO初始浓度相等时,体系中NO的平衡转化率与温度、压强的关系如右图所示,则NO的平衡转化率随温度升高而减小的原因___,压强(p1,p2,p3)的由大到小的顺序为___。
-
Ⅰ.汽车尾气排放的NOX和CO污染环境,在汽车尾气系统中安装催化转化器,可有效降低NOX和CO的排放。
已知:①2CO(g)+O2(g) 2CO2(g), △H=-566.0kJ·mol-1
2CO2(g), △H=-566.0kJ·mol-1
②N2(g)+O2(g) 2NO(g) △H=+180.5 kJ·mol-1
2NO(g) △H=+180.5 kJ·mol-1
回答下列问题:
(1) CO的燃烧热为___________,若1molN2(g)、1molO2(g)分子中化学键断裂时分别需要吸收946kJ、498kJ的能量,则1molNO (g) 分子中化学键断裂时需吸收的能量为___________kJ。
(2)为了模拟反应2CO(g)+2NO(g) 2CO2(g)+N2(g) 在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如表:
2CO2(g)+N2(g) 在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(10-4 kJ·mol-1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)/(10-3kJ·mol-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
①前2s内的平均反应速率v(N2)___________。
②能说明上述反应达到平衡状态的是___________。
A.2n(CO2)=n(N2) B.混合气体的平均相对分子质量不变
C.气体密度不变 D.容器内气体压强不变
(3)在某恒容容器中发生下列反应:2NO2(g) 2NO(g)+O2(g),将一定量的NO2放入恒容密闭容器中,测得其平衡转化率随温度变化如图所示。
2NO(g)+O2(g),将一定量的NO2放入恒容密闭容器中,测得其平衡转化率随温度变化如图所示。
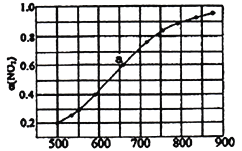
该反应为___________反应(填“吸热”或“放热”),已知图中a 点对应温度下,NO2的起始压强P0为120kPa,计算该温度 下反应的平衡常数 Kp 的值为___________。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅱ.N2H4-O2燃料电池是一种高效低污染的新型电池,其装置如图所示:
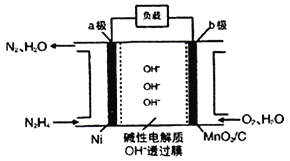
N2H4的电子式为___________ ;a极的电极反应方程式为___________;
-
汽车尾气系统中的催化转化器,可有效降低尾气中的CO、NO和NO2等向大气排放。在催化转化器的前半部发生的反应为2CO(g) + 2NO(g)  2CO2(g) + N2(g)。下列说法能充分说明该反应已经达到化学平衡状态的是
2CO2(g) + N2(g)。下列说法能充分说明该反应已经达到化学平衡状态的是
A. CO的转化率100% B. CO、NO、CO2、N2的浓度相等
C. CO、NO、CO2、N2在容器中共存 D. CO、NO、CO2、N2的浓度均不再变化
-
机动车排放的污染物主要有碳氢化合物、一氧化碳和氮氧化物等。
I.汽油燃油车上安装三元催化转化器,可有效降低汽车尾气污染。
(1)已知: C(s)+O2(g) = CO2(g) △H1 =− 393.5kJ·mol−1
2C(s)+O2(g) = 2CO(g) △H2 =− 221.0 kJ·mol−1
N2(g)+O2(g) = 2NO(g) △H 3 =+180.5 kJ·mol−1
CO和NO两种尾气在催化剂作用下生成N2的热化学方程式是_______。
(2)研究CO和NO的催化反应,用气体传感器测得在某温度下、一定体积的密闭容器中,不同时间NO和CO浓度如下表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(10−4mol·L−1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)/(10−3mol·L−1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
① 前4 s内的平均反应速率υ(CO) =______mol·L−1·s−1。
② L、X可分别代表压强或温度。下图A表示L一定时,NO(g)的平衡转化率随X的变化关系。X代表的物理量是___________。判断L1、L2的大小关系,并简述理由:_________。
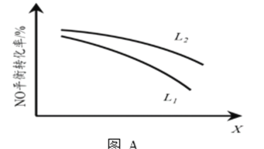
(3)实验测得,v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2) ·c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数_________(填“>”、“<”或 “=”)k逆增大的倍数。
②若在2 L的密闭容器中充入1 mol CO和1 mol NO,在一定温度下达到平衡时,CO的转化率为40%,则k正︰k逆 =_____________。(保留一位小数)
-
请阅读下列材料,完成下面小题。
汽车彻底改变了我们生活,成为我们的不可或缺的交通工具之一。汽车尾气系统中的催化转化器,可有效降低尾气中的CO、NO和NO2等向大气的排放,在催化转化器的前半部发生的反应为2CO(g)+2NO(g) 2CO2(g)+N2(g)。
2CO2(g)+N2(g)。
1.上述催化器中发生的反应属于
A.复分解反应 B.分解反应 C.置换反应 D.不属于四种基本反应
2.关于反应2CO(g)+2NO(g) 2CO2(g)+N2(g)中,下列说法正确的是
2CO2(g)+N2(g)中,下列说法正确的是
A.CO作氧化剂 B.CO发生氧化反应
C.NO被氧化 D.NO作还原剂
3.已知汽车尾气处理反应能量过程如下图,下列说法正确的是
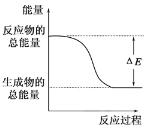
A.该反应为放热反应
B.该反应为吸热反应
C.形成N≡N化学键需要吸收热量
D.反应物的总能量小于生成物的总能量
4.下列反应条件的改变对该反应速率的影响正确的是
A.升高温度能减慢反应速率
B.增大反应物浓度能减缓反应速率
C.达到平衡时,CO能100%转化为CO2
D.使用催化剂能加快该反应的速率
-
2016年世界环境日我国的主题是:改善环境质量,推动绿色发展。符合该主题的措施有( )
A. 燃煤烟气脱硫
B. 大力发展和使用清洁能源
C. 直接排放电镀废水
D. 在汽车尾气系统中装置催化转化器
-
SCR技术可有效降低柴油发动机尾气中NOx的排放。SCR(选择性催化还原)工作原理如图所示。

(1)汽车尾气直接排放会造成_______
a. 硝酸型酸雨 b. 硫酸型酸雨 c. 臭氧层空洞
(2)尿素[CO(NH2)2]水溶液热分解为NH3和CO2,反应器中NH3可以还原NO2,起到转化有害物质为无害物质的作用,已知参加反应的氨气与NO2的体积比为4:3,其反应方程式为_________。
(3)根据元素守恒,最终处理产物除了N2和H2O,还有_______。
(4)若通入尾气中含67.2L NO2(标准状况),则与氨气完全反应转移电子数为_____mol。
N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用现代传感技术测得不同时间NO和CO的浓度如下表:







