-
化学兴趣小组中和热测定值与正确值有偏差,某同学甚至怀疑盐酸物质的量浓度不准确,他准备亲手配制0.50mol·L-1NaOH溶液,然后用中和滴定的方法测定盐酸物质的量浓度。
(1)配制100mL0.50mol·L-1 NaOH溶液,用托盘天平称取NaOH固体___g。
(2)下面是一段关于酸碱中和滴定实验操作的叙述:①取一锥形瓶,用待测HCl溶液润洗两次;②在一锥形瓶中加入20.00mL待测HCl溶液;③加入足量的合适试剂作指示剂;④取一支酸式滴定管,先用蒸馏水洗涤,再用待测HCl溶液润洗;⑤直接往碱式滴定管中注入标准NaOH溶液,进行滴定;⑥左手旋转滴定管的玻璃活塞,右手不停摇动锥形瓶;⑦两眼注视着滴定管内NaOH溶液液面下降,直至滴定终点。文中所述操作有错误的序号为(______)
A.④⑥⑦ B.①⑤⑥⑦ C.③⑤⑦ D.①③⑤⑦
(3)他若选择酚酞试剂作指示剂,判断达到滴定终点的正确方法是___。
高二化学实验题中等难度题查看答案及解析
-
某实验小组设计用50 mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液进行中和反应,测定中和热,中和热测定实验的关键是要比较准确地配制一定物质的量浓度的溶液,量热器要尽量做到绝热;在量热的过程中要尽量避免热量的散失,比较准确地测量出反应前后溶液温度的变化。回答下列问题:
(1)中和热的测定所需的玻璃仪器有________
(2)本实验中用稍过量的NaOH的原因是。
(3)在反应中若因为有放热现象,而造成少量HCl挥发,则测得的中和热数值________(填偏高、偏低或不变);
(4)该实验小组做了三次实验,每次取溶液各50mL,并记录如下原始数据。
实验序号
起始温度t1/℃
终止温度(t2)℃
温差(t2-t1)℃
盐酸
NaOH溶液
平均值
1
25.1
24.9
25.0
31.6
6.6
2
25.1
25.1
25.1
31.8
6.7
3
25.1
25.1
25.1
31.9
6.8
已知盐酸、NaOH溶液密度近似为1.00g/cm3,中和后混和液的比热容 C=4.18J/(g·℃)则该反应的中和热为△H=_______________________________;
(5)若用等浓度的醋酸代替盐酸与NaOH溶液反应,则测得的中和热的数值会________(填偏高、偏低或不变),其原因________;
高二化学实验题困难题查看答案及解析
-
化学兴趣小组的同学用0.100 0 mol/L 盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应)。实验步骤如下:
(1)配制待测液:用分析天平准确称取烧碱样品2.500 g,全部溶于水配制成500 mL溶液。配制溶液需用的玻璃仪器除了烧杯、胶头滴管外,还需要 。
(2)滴定:
①用碱式滴定管量取20.00 mL所配溶液放在锥形瓶中,滴加几滴指示剂,待测。滴定管在装入反应液之前应进行的操作有__________________。
②用浓度为0.100 0 mol/L的盐酸标准溶液进行滴定。开始滴定前的一步操作是____________。
③滴定过程中用pH计测定锥形瓶中溶液的pH,临近滴定终点时每滴一滴测一次pH。滴定过程中,测得锥形瓶中溶液的pH变化如下表:
V(HCl)/mL
0.00
12.00
18.00
22.00
23.00
23.96
pH
13.1
12.6
12.2
11.7
11.4
9.9
V(HCl)/mL
24.00
24.04
25.00
26.00
30.00
pH
7.0
4.0
2.7
2.4
1.9
(3)数据处理:
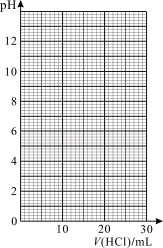
①在坐标图中绘出上述中和滴定曲线。
②所测样品中NaOH的质量百分含量为___________。
高二化学实验题困难题查看答案及解析
-
某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、50 mL 0.50mol/L盐酸、50 mL 0.55mol/LNaOH溶液,实验尚缺少的玻璃用品是____、____。
(2)NaOH稍过量的原因是_______。
(3)实验中若改用60 mL 0.50 mol/L盐酸和50 mL 0.55 mol/LNaOH溶液进行上述反应,与上述实验相比,所放出的热量_______(填“相等”或“不相等”),所求中和热____(填“相等”或“不相等”),理由是________。
(4)他们记录的实验数据如下:
实 验 用 品
溶液温度
t1
t2
①
50 mL 0.55mol/LNaOH溶液
20 ℃
23.3 ℃
50 mL 0.50mol/L盐酸
②
50 mL 0.55mol/LNaOH溶液
20 ℃
23.5 ℃
50 mL 0.50mol/L盐酸
已知:Q=cm(t2-t1),反应后溶液的比热容c为4.18 J/(℃•g),各物质的密度均为1 g/cm3。根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:____。
(5)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热(ΔH)______(填“偏大”“偏小”或“不变”),其原因是_______。
高二化学实验题中等难度题查看答案及解析
-
某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、50 mL 0.50mol/L盐酸、50 mL 0.55mol/LNaOH溶液,实验尚缺少的玻璃用品是____、____。
(2)NaOH稍过量的原因是_______。
(3)实验中若改用60 mL 0.50 mol/L盐酸和50 mL 0.55 mol/LNaOH溶液进行上述反应,与上述实验相比,所放出的热量_______(填“相等”或“不相等”),所求中和热____(填“相等”或“不相等”),理由是________。
(4)他们记录的实验数据如下:
实 验 用 品
溶液温度
t1
t2
①
50 mL 0.55mol/LNaOH溶液
20 ℃
23.3 ℃
50 mL 0.50mol/L盐酸
②
50 mL 0.55mol/LNaOH溶液
20 ℃
23.5 ℃
50 mL 0.50mol/L盐酸
已知:Q=cm(t2-t1),反应后溶液的比热容c为4.18 J/(℃•g),各物质的密度均为1 g/cm3。根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:____。
(5)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热(ΔH)______(填“偏大”“偏小”或“不变”),其原因是_______。
高二化学实验题中等难度题查看答案及解析
-
(12分)某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.50mol· L-1 盐酸、0.55mol· L-1NaOH溶液,尚缺少的实验玻璃用品是____ 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?________(填“能”或“否”),
其原因是________。
(3)他们记录的实验数据如下:
实 验 用 品
溶 液 温 度
△t
t1
t2
①
50mL0.55mol.L-1NaOH
50mL.0.5mol.L-1HCl
20℃
23.3℃
②
50mL0.55mol.L-1NaOH
50mL.0.5mol.L-1HCl
20℃
23.5℃
③
50mL0.55mol.L-1NaOH
50mL.0.5mol.L-1HCl
20℃
25.5℃
已知:Q=Cm(t2 -t1),反应后溶液的比热容C为4.18KJ·℃-1· Kg-1,各物质的密度均为1g·cm-3,△H值保留小数点后两位
根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:________
(4)若用KOH代替NaOH,测定结果________(填“偏大”、“偏小”或“无影响”,下同);若用醋酸代替HCl做实验,测定结果________。
高二化学实验题简单题查看答案及解析
-
I.(9分)某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.50 mol·L-1 NaOH溶液、0.55 mol·L-1盐酸,实验尚缺少的玻璃仪器是 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否)。
(3)他们记录的实验数据如下:
实验用品
溶液温度
中和热
t1
t2
ΔH
①
50 mL
0.50 mol·L-1
NaOH溶液
50 mL
0.55 mol·L-1
HCl溶液
20 ℃
23.2 ℃
②
50 mL
0.50 mol·L-1
NaOH溶液
50 mL
0.55 mol·L-1
HCl溶液
20 ℃
23.4 ℃
已知:Q =cm Δt,c为4.18 J·℃-1·g-1,各溶液的密度均为1 g· cm-3。
①通过计算得到中和热ΔH = kJ/mol(保留一位小数)。
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式: 。
(4)若用0.60 mol·L-1NaOH溶液代替0.50 mol·L-1NaOH溶液做实验,对测定结果 (填“有”或“无”,下同)影响;若用0.55 mol·L-1醋酸代替0.55 mol·L-1盐酸做实验,对测定结果 影响。
(5)计算结果发现本次实验测定值与正确值57.3 kJ/mol有偏差,产生偏差的原因可能是 (填序号)操作。
①量取NaOH溶液的体积时仰视读数
②用温度计测定NaOH溶液的温度后直接测定盐酸的温度
③分多次把NaOH溶液倒入装盐酸的小烧杯中
II.(6分)甲、乙两同学拟定用pH试纸验证醋 酸是弱酸。方案分别是:
甲:①称取一定量的冰醋酸准确配制0.1mol/L的醋酸溶液100mL
②用pH试纸测出该溶液的pH,即可证明醋酸是弱酸。
乙:①称取一定量的冰醋酸准确配制pH=1的醋酸溶液100mL;
②取醋酸溶液10mL,加水稀释为100 mL;
③用pH试纸测出该溶液的pH,即可证明醋酸是弱酸。
(1)两个方案的第①步中,都要用到的定量仪器是 。
(2)简要说明pH试纸的使用方法: 。
(3)甲方案中,说明醋酸是弱酸的理由是测得醋酸溶液的pH 1(选填“>”“<”“=”);乙方案中,说明醋酸是弱酸的理由是测得醋酸溶液的pH 2(选填“>”“<”“=”)。
(4)请你也提出一个用pH试纸来证明醋酸是弱酸的合理且容易进行的方案(可以不再叙述pH试纸的使用方法,但叙述中应包括实验方法、现象和结论) 。
高二化学实验题困难题查看答案及解析
-
I.某化学兴趣小组要完成中和热的测定实验。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.50 mol·L-1 NaOH溶液、0.55 mol·L-1盐酸,实验尚缺少的玻璃仪器是 。
(2)实验中 (填“能”或“不能”)用环形铜丝搅拌棒代替环形玻璃搅拌棒。
II.甲、乙两同学拟定用pH试纸验证醋酸是弱酸。方案分别是:
(1)pH试纸的使用方法是:剪半条pH试纸放在玻璃片上, 。
(2)甲:①称取一定量的冰醋酸准确配制0.1mol/LCH3COOH溶液100mL
②若用pH试纸测出该溶液的pH 1(选填“>”、“<”、“=”),即可证明醋酸是弱酸。
乙:①称取一定量的冰醋酸准确配制pH=1的醋酸溶液100mL;
②取醋酸溶液1mL,加水稀释为100mL;
③若用pH试纸测出该溶液的pH的范围为 ,即可证明醋酸是弱酸。
(3)甲、乙方案的共同依据是 。
(4)请你另外设计一个用pH试纸来证明醋酸是弱酸的实验方案: 。
高二化学实验题困难题查看答案及解析
-
某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、50mL量筒两个,0.55mol·L-1NaOH溶液、0.50mol·L-1盐酸,实验尚缺少的玻璃仪器是__。
(2)他们记录的实验数据如下:(t1为起始终止温度,t2为终止温度)
实验用品
溶液温度
中和热
t1
t2
ΔH
①
50mL
0.55mol·L-1
NaOH溶液
50mL
0.50mol·L-1
HCl溶液
20℃
23.2℃
②
50mL
0.55mol·L-1
NaOH溶液
50mL
0.50mol·L-1
HCl溶液
20℃
23.4℃
已知:Q=cmΔt,c为4.18J·℃-1·g-1,各溶液的密度均为1g·cm-3。
①通过计算得到中和热ΔH=___kJ/mol(只列出计算式不计算结果)。
②根据①的计算式计算出中和热的数值为55.2,写出NaOH溶液与HCl溶液反应的热化学方程式:___。
(3)若用0.50mol·L-1醋酸代替0.50mol·L-1盐酸做实验,对测定结果___影响(填“有”或“无”)。
(4)本次实验测定值与正确值57.3kJ/mol有偏差,产生偏差的原因可能是___(填序号)操作。
①量取NaOH溶液的体积时仰视读数
②用温度计测定NaOH溶液的温度后直接测定盐酸的温度
③分多次把NaOH溶液倒入装盐酸的小烧杯中
高二化学实验题中等难度题查看答案及解析
-
某化学小组用50ml 0.50mol/L NaOH溶液和30ml 0.50mol/L硫酸溶液进行中和热的测定实验。
(1)实验中大约要使用230mL NaOH溶液,配制溶液时至少需要称量NaOH固体__ g。
(2)做中和热的测定实验时:桌上备有大、小两个烧杯、泡沫塑料、硬纸板、胶头滴管、环形玻璃搅拌棒.实验尚缺少的玻璃仪器(用品)是______、______。
(3)他们记录的实验数据如下:
①请填写表中的空白:
实验次数
起始温度t1
终止温度t2/℃
温度差平均值(t2﹣t1)/℃
H2SO4
NaOH
1
25.0℃
25.0℃
29.1
Δt=________
2
25.0℃
25.0℃
29.8
3
25.0℃
25.0℃
28.9
4
25.0℃
25.0℃
29.0
②已知:溶液的比热容c为4.18 J·℃-1·g-1,溶液的密度均为1 g·cm-3。写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式____________(用该实验的数据,取小数点后一位)。
(4)若用氨水代替NaOH做实验,测定结果ΔH会___(填“偏大”、“偏大”、“无影响”)。
高二化学实验题中等难度题查看答案及解析