-
现有A、B、C、D、E、F六种无色溶液,它们可能是:CH3COONa溶液、NH4Cl溶液、NaOH溶液、CH3COOH溶液、氨水、NaCl溶液中的某一种(若室温下NH3·H2O的Ka=1.8×10-5)。已知B、D两溶液呈酸性,但B溶液中水的电离程度大于D溶液中水的电离程度;A、C、F焰色反应均为黄色,F溶液呈中性,A、C溶液呈碱性,但物质的量浓度相同时,C溶液的pH大于A溶液的pH。试回答下列问题:
(1)在B、C、F三种溶液中,水的电离程度由大到小的顺序为___。(填序号)。
(2)室温下,将等物质的量浓度,等体积的B、E两溶液相混合,则溶液中各离子浓度大小关系为___。
(3)室温下,若C溶液与D溶液的pH之和等于14,将二者等体积混合,所得混合溶液的pH___7(填“大于”或“等于”或“小于”);
(4)室温下,xmol·L-1CH3COOH溶液与0.01mol·L-1NaOH溶液等体积混合,混合溶液的pH恰好等于7(体积变化忽略不计),则CH3COOH电离平衡常数为___(用含x的代数式表示)。
(5)仅从以上六种无色溶液中选择试剂(其它器材自选),用简单的实验证明CH3COOH是弱酸,请简述实验操作___。
高二化学综合题中等难度题查看答案及解析
-
现有下列化合物:①NaCl、②NaOH、③HCl、④NH4Cl、⑤CH3COONa、⑥CH3COOH、⑦NH3·H2O、⑧H2O。回答下列问题。
(1)NH4Cl溶液显_____________性,用离子方程式表示原因:_____________。其溶液中离子浓度大小顺序为__________________________。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=_____________mol/L;在pH=3的CH3COOH溶液中,水电离出来的c(H+)=_____________mol/L。
(3)已知纯水中存在如下平衡:H2O⇌H+OH-∆H>0。现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是____________填字母序号)。
A.向水中加入NaHSO4固体 B.向水中加Na2CO3固体
C.加热至100℃ D.向水中加入(NH4)2SO4固体
(4)若将等pH、等体积的②NaOH和⑦NH3·H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m____________填“<”“>”或“=”)n。
(5)①NaCl、②NaOH、③HCl、⑤CH3COONa、⑥CH3COOH这5种溶液的物质的量浓度相同,则这5种溶液按pH由大到小的顺序为_________________________填序号)。
高二化学填空题困难题查看答案及解析
-
下列化合物:①HCl ②NaOH ③CH3COOH ④NH3·H2O ⑤CH3COONa ⑥NH4Cl
(1)溶液呈碱性的有________(填序号)。
(2)常温下0.01mol·L-1 NaOH溶液的pH=________;pH=11的CH3COONa溶液中由水电离产生的c(OH-)=________。
(3)将等pH等体积的HCl和CH3COOH分别稀释m倍和n倍,稀释后两溶液的pH仍相等,则m________n(填“大于”、“等于”或“小于”)。
高二化学填空题简单题查看答案及解析
-
①pH=2的CH3COOH溶液:②pH=2的盐酸;③pH=2的NH4Cl溶液;④pH=12的氨水;⑤pH=12的NaOH溶液;⑥pH=12的CH3COONa溶液。室温下,有关上述溶液的比较中,正确的是( )
A. 水电离的c(H+):③=⑥>①=②=④=⑤
B. 将②、④溶液混合后,pH=7,消耗溶液的体积:②<④
C. 等体积的①、②、⑤溶液分别与足量铝粉反应,生成H2的量,②最大
D. 向等体积溶液中加入100mL水后,熔液的pH:④>⑥>⑤>③>①>②
高二化学单选题困难题查看答案及解析
-
下列溶液一定呈中性的是 ( )
A.pH=7的溶液
B.c(NH4+)=c(Cl-)的NH4Cl和氨水的混合溶液
C.PH=2的CH3COOH和PH=12的NaOH溶液等体积混合
D.CH3COONa溶液
高二化学选择题简单题查看答案及解析
-
根据下列化合物:①NaCl ②NaOH ③HCl ④NH4Cl ⑤CH3COONa ⑥CH3COOH ⑦NH3•H2O ⑧H2O,回答下列问题.
(1)NH4Cl溶液显酸性,用离子方程式表示原因 ,其溶液中离子浓度大小顺序为
。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH﹣)= ,在pH=3的CH3COOH溶液中,水电离出来的c(H+)= 。
(3)若将等pH、等体积的②NaOH和⑦NH3•H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m n。(填“<”、“>”或“=”)
(4)若前五种溶液的物质的量浓度相同,用序号排出这五种溶液pH由大到小的顺序 。
高二化学填空题简单题查看答案及解析
-
下列化合物:①HCl ②NaOH ③CH3COOH④NH3·H2O ⑤CH3COONa ⑥NH4Cl
(1)溶液呈碱性的有 (填序号)。
(2)常温下0.01 mol/L HCl溶液的PH= ;
(3)常温下PH=11的CH3COONa溶液中由水电离产生的c(OH-) = 。
(4)用离子方程式表示CH3COONa溶液呈碱性的原因 。
高二化学填空题中等难度题查看答案及解析
-
下列化合物:①HCl、②NaOH、③CH3COOH、④NH3•H2O、⑤CH3COONa、⑥NH4Cl
(1)属于弱电解质的是 ,溶液呈碱性的有 (填序号).
(2)常温下0.01mol/L HCl溶液的pH= ;pH=11的CH3COONa溶液中由水电离产生的c(OH﹣)= .
(3)将等pH等体积的HCl和CH3COOH分别稀释m倍和n倍,稀释后两溶液的pH仍相等,则m n (填“大于、等于、小于”).
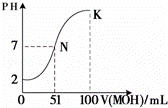
(4)常温下,向100mL 0.01mol•L﹣1HA溶液逐滴加入0.02mol•L﹣1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:
①N点对应的溶液中,c(M+) c(A﹣)(填“大于、等于、小于”).
②K点对应的溶液中,c(M+)+c(MOH)= mol•L﹣1.
高二化学填空题中等难度题查看答案及解析
-
根据下列化合物:①NaCl、②NaOH、③HCl、④NH4Cl、⑤CH3COONa、⑥CH3COOH、⑦NH3·H2O、⑧H2O。回答下列问题。
(1)NH4Cl溶液显________性,用离子方程式表示原因______________,其溶液中离子浓度大小顺序为________________
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=__________mol/L,在pH=3的CH3COOH溶液中,水电离出来的c(H+)=__________mol/L。
(3)已知纯水中存在如下平衡:H2O+H2O
H3O++OH- △H>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是______(填字母序号)。
A.向水中加入NaHSO4固体 B.向水中加Na2CO3固体
C.加热至100℃ D.向水中加入(NH4)2SO4固体
(4)若将等pH、等体积的②NaOH和⑦NH3·H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m______n(填“<”、“>”或“=”)。
(5)除④⑦⑧外,若其余5种溶液的物质的量浓度相同,则这5种溶液按pH由大到小的顺序为:_________________(填序号)
高二化学填空题中等难度题查看答案及解析
-
根据下列化合物:①NaCl、②NaOH、③HCl、④NH4Cl、⑤CH3COONa、⑥CH3COOH、⑦NH3·H2O、⑧H2O。回答下列问题。
(1)NH4Cl溶液显__________性,用离子方程式表示原因 , 其溶液中离子浓度大小顺序为_________
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=__________mol/L在pH=3的CH3COOH溶液中,水电离出来的c(H+)=__________mol/L。
(3)已知纯水中存在如下平衡:H2O
H++OH- △H>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是_____________(填字母序号)。
A.向水中加入NaHSO4固体 B.向水中加Na2CO3固体
C.加热至100℃ D.向水中加入(NH4)2SO4固体
(4)若将等pH、等体积的②NaOH和⑦NH3·H2O分别加水稀释m倍、n倍,稀 释后两种溶液的pH仍相等,则m__________n(填“<”、“>”或“=”)。
(5)①NaCl、②NaOH、③HCl、⑤CH3COONa、⑥CH3COOH,这5种溶液的物质的量浓度相同,则这5种溶液按 pH由大到小的顺序为:______________(填序号)
高二化学填空题极难题查看答案及解析