-
铜及其化合物有着十分重要的用途:如氨基乙酸铜[结构简式为(H2NCH2COO)2Cu]常用作食品补铜剂及矿物元素饲料添加剂,硒化铜纳米晶在光电转化中有着广泛地应用;硫酸铜可用作配制农药等。
(1)基态硒原子的电子排布式为____,基态氮原子电子的空间运动状态有__种,与硒同周期相邻的三种元素第一电离能由大到小的顺序为______
(2)(H2NCH2COO)2Cu氨基乙酸铜中,碳原子的杂化轨道类型是______;与氮原子成键的原子(含氮原子本身)形成的空间构型是__________。
(3)硫酸铜晶体的组成可表示为[Cu(H2O)4]SO4·H2O,实验测得该物质中存在氢键且水分子成“键”情况与冰中类似,则1mol[Cu(H2O)4]SO4·H2O中氢键数目为__NA。
(4)硫酸铜在高温下分解有可能得到CuO、Cu2O、SO2、SO3等物质,其中CuO的熔点为1026℃。
①CuO的晶体类型是_____,熔点Cu2O>Cu2S的原因是______
②SO2与SO3中,属于非极性分子的是__,SO2在溶剂水与溶剂CCl4中,相同温度能溶解更多SO2的溶剂是___________
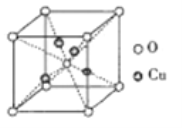
③铜的某种氧化物的晶胞如下图所示,则该氧化物的化学式为_______,若组成粒子氧、铜的半径分别为rOpm、rCupm,密度ρg/cm3,阿伏加德罗常数值为NA,则该晶胞的空间利用率为______(用含π的式子表示)。
-
铜及其化合物有着十分重要的用途:如氨基乙酸铜[结构简式为(H2NCH2COO)2Cu]常用作食品补铜剂及矿物元素饲料添加剂,硒化铜纳米晶在光电转化中有着广泛地应用;硫酸铜可用作配制农药等。
(1)基态硒原子的电子排布式为____,基态氮原子电子的空间运动状态有__种,与硒同周期相邻的三种元素第一电离能由大到小的顺序为______
(2)(H2NCH2COO)2Cu氨基乙酸铜中,碳原子的杂化轨道类型是______;与氮原子成键的原子(含氮原子本身)形成的空间构型是__________。
(3)硫酸铜晶体的组成可表示为[Cu(H2O)4]SO4·H2O,实验测得该物质中存在氢键且水分子成“键”情况与冰中类似,则1mol[Cu(H2O)4]SO4·H2O中氢键数目为__NA。
(4)硫酸铜在高温下分解有可能得到CuO、Cu2O、SO2、SO3等物质,其中CuO的熔点为1026℃。
①CuO的晶体类型是_____,熔点Cu2O>Cu2S的原因是______
②SO2与SO3中,属于非极性分子的是__,SO2在溶剂水与溶剂CCl4中,相同温度能溶解更多SO2的溶剂是___________
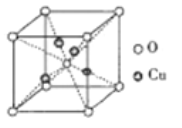
③铜的某种氧化物的晶胞如下图所示,则该氧化物的化学式为_______,若组成粒子氧、铜的半径分别为rOpm、rCupm,密度ρg/cm3,阿伏加德罗常数值为NA,则该晶胞的空间利用率为______(用含π的式子表示)。
-
铜及其化合物有着十分重要的用途:如氨基乙酸铜[结构简式为(H2NCH2COO)2Cu]常用作食品补铜剂及矿物元素饲料添加剂,硒化铜纳米晶在光电转化中有着广泛地应用;硫酸铜可用作配制农药等。
(1)基态硒原子的电子排布式为____,基态氮原子电子的空间运动状态有__种,与硒同周期相邻的三种元素第一电离能由大到小的顺序为______
(2)(H2NCH2COO)2Cu氨基乙酸铜中,碳原子的杂化轨道类型是______;与氮原子成键的原子(含氮原子本身)形成的空间构型是__________。
(3)硫酸铜晶体的组成可表示为[Cu(H2O)4]SO4·H2O,实验测得该物质中存在氢键且水分子成“键”情况与冰中类似,则1mol[Cu(H2O)4]SO4·H2O中氢键数目为__NA。
(4)硫酸铜在高温下分解有可能得到CuO、Cu2O、SO2、SO3等物质,其中CuO的熔点为1026℃。
①CuO的晶体类型是_____,熔点Cu2O>Cu2S的原因是______
②SO2与SO3中,属于非极性分子的是__,SO2在溶剂水与溶剂CCl4中,相同温度能溶解更多SO2的溶剂是___________
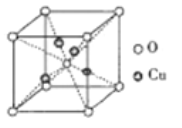
③铜的某种氧化物的晶胞如下图所示,则该氧化物的化学式为_______,若组成粒子氧、铜的半径分别为rOpm、rCupm,密度ρg/cm3,阿伏加德罗常数值为NA,则该晶胞的空间利用率为______(用含π的式子表示)。
-
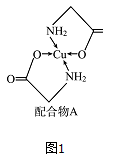
已知铜的配合物A结构如图。请回答下列问题:

(1)写出基态Cu的外围电子排布式:__。
(2)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中σ键和π键数目之比是__;N2O与CO2互为等电子体,则N2O的空间结构为___。
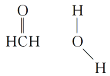
(3)在Cu催化下,甲醇可被氧化为甲醛,甲醛分子中HCO的键角__(填“大于”“等于”或“小于”)120°;甲醛能与水形成氢键,请在如图中表示出来___。
(4)立方氮化硼如图1与金刚石结构相似,是超硬材料。立方氮化硼晶体内B—N键数与硼原子数之比为__。

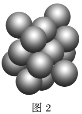
(5)Cu晶体的堆积方式如图2所示,设Cu原子半径为a,晶体中Cu原子的配位数为___,晶体的空间利用率为__。(已知: ≈1.4)
≈1.4)
-
已知铜的配合物A结构如图图1。请回答下列问题:
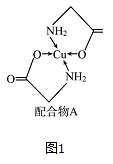
(1)写出基态Cu的外围电子排布式________
(2)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中σ键和x键数目之比是___;N2O与CO2互为等电子体,则N2O的电子式为_______。
(3)在Cu催化下,甲醇可被氧化为甲醛,甲醇分子中HCO的键角____(选填“大于”、“等于”或“小于”) l20°;甲醛能与水形成氢健,请在如图2中表示出来____。


(4)立方氮化硼如图3、图4与金刚石结构相似,是超硬材料。立方氮化硼晶体内B一N键数与硼原子数之比为__________;
(5)Cu晶体的堆积方式如图5所示,设Cu原子半径为a,晶体中Cu原子的配位数为_____,晶体的空间利用率为_________。(已知: ,列式并计算出结果)
,列式并计算出结果)
-
已知铜的配合物A结构如图图1。请回答下列问题:
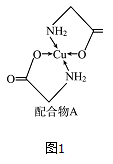
(1)写出基态Cu的外围电子排布式________
(2)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中σ键和x键数目之比是___;N2O与CO2互为等电子体,则N2O的电子式为_______。
(3)在Cu催化下,甲醇可被氧化为甲醛,甲醇分子中HCO的键角____(选填“大于”、“等于”或“小于”) l20°;甲醛能与水形成氢健,请在如图2中表示出来____。

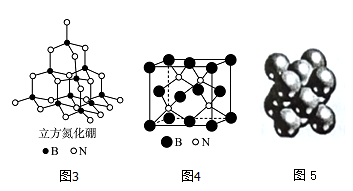
(4)立方氮化硼如图3、图4与金刚石结构相似,是超硬材料。立方氮化硼晶体内B一N键数与硼原子数之比为__________;
(5)Cu晶体的堆积方式如图5所示,设Cu原子半径为a,晶体中Cu原子的配位数为_____,晶体的空间利用率为_________。(已知: ,列式并计算出结果)
,列式并计算出结果)
-
已知铜的配合物A结构如图图1。请回答下列问题:
(1)写出基态Cu的外围电子排布式________
(2)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中σ键和x键数目之比是___;N2O与CO2互为等电子体,则N2O的电子式为_______。
(3)在Cu催化下,甲醇可被氧化为甲醛,甲醇分子中HCO的键角____(选填“大于”、“等于”或“小于”) l20°;甲醛能与水形成氢健,请在如图2中表示出来____。

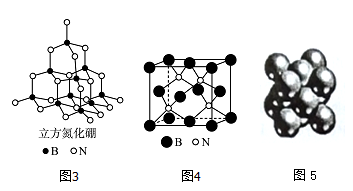
(4)立方氮化硼如图3、图4与金刚石结构相似,是超硬材料。立方氮化硼晶体内B一N键数与硼原子数之比为__________;
(5)Cu晶体的堆积方式如图5所示,设Cu原子半径为a,晶体中Cu原子的配位数为_____,晶体的空间利用率为_________。(已知: ,列式并计算出结果)
,列式并计算出结果)
-
氨基呈碱性,氨基酸呈两性。把甘氨酸(氨基乙酸)放入一定pH的溶液中,所得溶液中不能同时大量存在的微粒是①H2NCH2COOH ②H3N+-CH2COOH ③H2NCH2COO- ④H3N+-CH2COO-
A.①与② B.①与③ C.②与③ D.②与④
-
氨基酸微量元素螯合物在饲料生产应用、解决过量添加无机盐造成环境污染等方面有重要应用。该类螯合物通常以蛋氨酸、赖氨酸、甘氨酸等为配位体,以铜、铁、锌、锰、铬、钴等元素为中心离子。
(1)甘氨酸中共有_____个σ键,所含元素的电负性由大到小的顺序为______,官能团中C原子的杂化方式为_______。
(2)上述金属元素中,基态原子有五个未成对电子的原子的核外电子排布式为______。
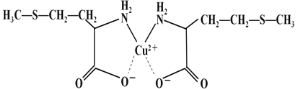
(3)蛋氨酸铜的结构式如下图。该螯合物中含有的化学键类型有_________(填序号)。
a.配位键 b.极性键 c.离子键 d.非极性键
(4)Cr是周期表中第ⅥB族元素,化合价可以是0~+6的整数价态。某化合物的化学式为Na3CrO8,其阴离子结构可表示为 ,则Cr的化合价为______。
,则Cr的化合价为______。 呈四面体构型,结构为
呈四面体构型,结构为 ,
, 由两个
由两个 四面体组成,这两个
四面体组成,这两个 四面体通过共用一个顶角氧原子彼此连接,结构为
四面体通过共用一个顶角氧原子彼此连接,结构为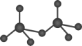 。则由n(n>1)个
。则由n(n>1)个 通过顶角氧原子连结的链式结构的化学式为____。
通过顶角氧原子连结的链式结构的化学式为____。
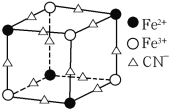
(5)实验室中可用KSCN或K4[Fe(CN)6]来检验Fe3+。FeCl3 与KSCN溶液混合,可得到配位数为5的配合物的化学式是____;K4[Fe(CN)6]与Fe3+反应可得到一种蓝色沉淀KFe[Fe(CN)6],该物质晶胞的 结构如下图所示(K+未画出),则一个晶胞中的K+个数为____。
结构如下图所示(K+未画出),则一个晶胞中的K+个数为____。
-
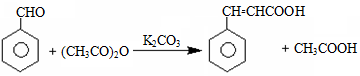
肉桂酸用途广泛,常被用作食品保鲜剂、食品添加剂、有机合成中间体等。其一种合成原理如下:
【实验步骤】
①向A中依次加入沸石、一定比例的苯甲醛、乙酸酐及少许碳酸钾。
②控制温度1500C~1700C,使其充分反应。
③向冷却后的三口瓶内加入饱和碳酸钠溶液,调节pH至9~10。
④如装置B所示,用水蒸气蒸馏,除去未反应的苯甲醛。
⑤加入活性炭,充分振荡并煮沸脱色。
⑥……
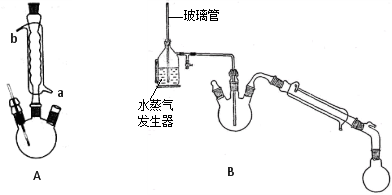
(1)装置A中冷凝管由 端(填“a”或“b”)通入冷凝水。
(2)步骤③中加入饱和碳酸钠溶液将肉桂酸、醋酸转化为肉桂酸钠和醋酸钠的原因: 。
(3)装置B在进行水蒸气蒸馏之前,需进行的操作为 ,玻璃管的作用为 。
(4)当观察到冷凝管中 ,说明水蒸气蒸馏结束。
(5)步骤⑥通过以下操作分离、提纯得较纯净的肉桂酸(难溶于水),其正确的操作顺序是 (填字母)。
a.重结晶 b.冷却、抽滤,水洗晶体
c.加入浓盐酸调节pH=3 d.静置,趁热过滤得肉桂酸钠溶液














 。则由n(n>1)个
。则由n(n>1)个

