-
酯广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业。乙酸乙酯一般通过乙酸和乙醇酯化合成。请根据要求回答下列问题:
(1)将乙酸、乙醇、浓硫酸混合的同时加入碎瓷片的目的是____,在合成过程中控制乙酸过量的作用是____。
(2)向反应后混合液中加入5% Na2CO3溶液洗涤至中性。分液,取上层油状液体,加入无水Na2SO4固体,过滤后蒸馏,收集76~78 ℃馏分。实验中加入少量无水Na2SO4固体的目的是____。
(3)此反应以浓硫酸为催化剂,会造成____等问题,目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂。实验数据如下表所示(乙酸和乙醇以等物质的量混合)。
| 同一反应时间 | 同一反应温度 |
| 反应温度/℃ | 转化率(%) | 选择性(%)* | 反应时间/h | 转化率(%) | 选择性(%)* |
| 40 | 77.8 | 100 | 2 | 80.2 | 100 |
| 60 | 92.3 | 100 | 3 | 87.8 | 100 |
| 80 | 92.6 | 100 | 4 | 92.3 | 100 |
| 120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
| *选择性100%表示反应生成的产物是乙酸乙酯和水 |
根据表中数据,下列____(填字母)为该反应的最佳条件。
A.40℃,3h B.60℃,4h C.80℃,2h D.120℃,4h
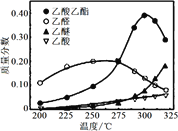
(4)近年,科学家研究了乙醇催化合成乙酸乙酯的新方法:2C2H5OH CH3COOC2H5+2H2,在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。当反应温度高于300 ℃时,乙酸乙酯的质量分数迅速下降的原因可能是____。
CH3COOC2H5+2H2,在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。当反应温度高于300 ℃时,乙酸乙酯的质量分数迅速下降的原因可能是____。
-
(12分)酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常用冰醋酸、无水乙醇和浓硫酸混合,在加热条件下反应制得:
请根据要求回答下列问题:
(1) 写出该反应的化学方程式________
(2)此反应中浓硫酸的作用是 ________
饱和碳酸钠的作用是________
(3)若采用同位素示踪法研究该化学反应,反应物无水乙醇中含有18O,冰醋酸中均为16O,反应后的混合物中,含有18O的物质有________
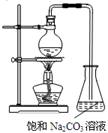
(4)若用如图所示装置来制备少量的乙酸乙酯,锥形瓶中的现象为________,不过往往产率偏低,其原因可能为(任填2种)
-
(16分)酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业,乙酸乙酯的实验室和工业制法常采用如下反应:

请根据要求回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有________,________。(任写两点只要合理即可)
(2)浓硫酸的作用是:①________、②________。
(3)饱和NaCO3溶液的作用:
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)
| 同一反应时间 | 同一反应温度 |
| 反应温度/℃ | 转化率/% | 选择性/% | 反应时间/h | 转化率/% | 选择性/% |
| 40 | 77.8 | 100 | 2 | 80.2 | 100 |
| 60 | 92.3 | 100 | 3 | 87.8 | 100 |
| 80 | 92.6 | 100 | 4 | 92.3 | 100 |
| 120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
| 选择性100%表示反应无副反应发生 |
根据表中数据,下列________(填字母)为该反应的最佳条件。
A.120 ℃,4 h B. 80 ℃,2 h C. 60 ℃,4 h D.40 ℃,3 h
-
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业.乙酸乙酯的实验室和工业制法常采用如下反应:CH3COOH+C2H5OH
 CH3COOC2H5+H2O
CH3COOC2H5+H2O
请根据要求回答下列问题:
(1)若用右图所示装置来制备少量的乙酸乙酯,其中饱和碳酸钠溶液的作用是______.
(2)此反应以浓硫酸为催化剂,可能会造成______、______等问题.
(3)在图所示的装置中进行50mL 0.50mol/L醋酸与50mL 0.55mol/L NaOH溶液的中和反应.通过测定反应过程中所放出的热量可计算反应热.回答下列问题: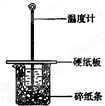
①从实验装置上看,图中尚缺少的一种玻璃用品是______;
②在题述反应条件下,测得反应前醋酸和NaOH溶液的温度均为25.43℃,反应后混合溶液的温度为28.73℃.已知反应前醋酸
和NaOH溶液的密度均为1.0g•cm-3,反应后混合溶液的比热容为c=4.18J/.试写出中和反应的热化学方程式:______.
-
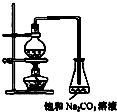
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、妨织等工业。乙酸乙酯的实验室制法常采用如图装置:
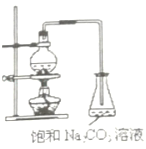
(1)烧瓶中除了乙酸和乙醇之外,还必须加的药品是___,其作用是___。
(2)能不能把饱和Na2CO3溶液换成饱和NaCl溶液?___,为什么?___。
(3)为了乙酸和乙醇回流,减少它们损失,该装置应该改进之处是:___。
(4)分离乙酸乙酯和饱和溶液,所需要的操作是___。
-
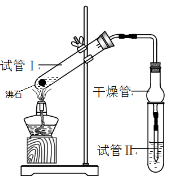
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。某学生在实验室利用下图的实验装置制备乙酸乙酯并研究其反应条件。
| 物质 | 沸点/C | 密度/gcm3 |
| 乙醇 | 78.0 | 0.79 |
| 乙酸 | 117.9 | 1.05 |
| 乙酸乙酯 | 77.5 | 0.90 |
| 异戊醇 | 131 | 0.8123 |
| 乙酸异戊酯 | 142 | 0.8670 |
实验步骤如下:
① 配制反应混合液:2mL浓H2SO4、3mL乙醇、2mL乙酸
② 按图连接实验装置并检验气密性
③ 分别在试管1、试管2中加入反应液
④ 用酒精灯微热3min,再加热使之微微沸腾3min
⑤ 分离提纯乙酸乙酯
(1)在试管1中加入物质分别是:______________(按着加入的先后顺序写出名称),乙醇过量的目的是:_______________;
(2)该反应的平衡常数表达式K=______________;
(3)试管Ⅱ中所盛试剂为___________,欲将其物质分离使用的仪器为___________,在充分振荡的过程中,发生的反应为________________;
(4)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用右图所示装置进行了以下四个实验,实验结束后充分振荡试管Ⅱ再测有机层的厚度,实验记录如下:
| 实验编号 | 试管Ⅰ中的试剂 | 测得有机层的厚度/cm |
| A | 2mL乙醇、2mL乙酸、1mL 18mol/L浓硫酸 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 |
| C | 3mL乙醇、2mL乙酸、6mL 3mol/L硫酸 | 1.2 |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是_________mL和_________mol/L;
②分析实验________(填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是____________;
③加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是_______________;
(5)若利用该装置制备乙酸异戊酯,产物将主要在装置中_______的得到,那么产率会_____(“较高”或“偏低”);
-
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室制取乙酸乙酯的主要步骤如下:
①在甲试管(如图)中加入 2mL 浓硫酸、3mL 乙醇和 2mL 乙酸的混合溶液。

②按如图连接好装置(装置气密性良好)并加入混合液,小火均匀地加热 3-5min。
③待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。
(1)若实验中用乙酸和含18O 的乙醇作用,该反应的化学方程式是_____。
(2)甲试管中,混合溶液的加入顺序:_____;
(3)步骤②中需要用小火均匀加热,其主要原因是___________;
(4)上述实验中饱和碳酸钠溶液的作用是_____(填字母代号)。
A.反应掉乙酸和乙醇
B.反应掉乙酸并吸收乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
(5)欲将乙试管中的物质分离开以得到乙酸乙酯,必须使用的仪器是_____;分离时,乙酸乙酯应该从仪器_____(填:“下口放”或“上口倒”)出。
(6)生成乙酸乙酯的反应是可逆反应,反应一段时间后,下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有_____(填序号)。
①混合物中各物质的浓度不再变化;
②单位时间里,生成 1mol 乙醇,同时生成 1mol 乙酸;
③单位时间里,生成 1mol 乙酸乙酯,同时生成 1mol 乙酸。
(7)若现有乙酸 90g,乙醇 138g 发生酯化反应得到 88g 乙酸乙酯,试计算该反应的产品产率为_____。(产率%=(实际产量/理论产量)×100%)
-
(10分)
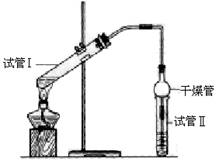
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室用乙酸与乙醇反应制备乙酸乙酯。为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下四个实验,实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡试管Ⅱ再测有机层的厚度,实验记录如下:
| 实验 编号 | 试管Ⅰ中的试剂 | 试管Ⅱ中试剂 | 测得有机层的厚度/cm |
| A | 2mL乙醇、2mL乙酸、1mL 18mol·L-1浓硫酸 | | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 |
| C | 3mL乙醇、2mL乙酸、6mL 3mol·L-1硫酸 | 1.2 |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
(1)试管Ⅱ中试剂的名称为 ________,其作用是 ________
________,使用干燥管的目的是 ________。
(2)分析比较实验________(填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是________。
(3)实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是________mL和________mol·L-1。
-
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室用无水乙醇与乙酸制备乙酸乙酯的化学方程式如下:
CH3COOH+C2H5OH CH3COOC2H5+H2O
CH3COOC2H5+H2O
(1)该反应的平衡常数表达式K= ________ 。
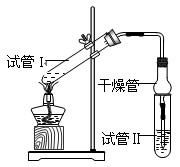
(2)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用右图所示装置进行了以下四个实验,实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡试管Ⅱ再测有机层的厚度,实验记录如下:
| 实验 编号 | 试管Ⅰ中的试剂 | 试管Ⅱ中试剂 | 测得有机层的厚度/cm |
| A | 2mL乙醇、2mL乙酸、1mL 18mol/L浓硫酸 | 饱和碳酸钠溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 |
| C | 3mL乙醇、2mL乙酸、6mL 3mol/L硫酸 | 1.2 |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是________mL和________mol/L。
②分析实验________(填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是________。
③加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是________。
-
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。
(1)乙醇、乙酸和浓硫酸的加入顺序是___________。制取乙酸乙酯的反应原理为:__________________________________。

(2)为证明浓硫酸在该反应中起到了______和________的作用, 为证明其作用,某同学利用上图所示装置进行了以下四个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管II再测有机层的厚度,实验记录如下:
| 实验编 号 | 试管I中的试剂 | 试管II中的试剂 | 测得有机层的厚度/cm |
| A | 2mL乙醇、2mL乙酸、1mL18mo/L浓硫酸 | | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 饱和碳酸钠溶液 | 0.1 |
| C | 3mL乙醇、2mL乙酸、6mL3mol/L硫酸 | | 1.2 |
| D | 3mL乙醇、2mL乙酸、盐酸 | | 1.2 |
①验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是_____mL和_____mol/L。
②分析实验_______(填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是___________。
(3)饱和碳酸钠溶液的作用是溶解没有反应的乙醇,除去没有反应的乙酸和___________,本实验装置有明显的缺陷,其可能造成的后果是__________________________。
(4)加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,一个可能的原因是_______________。
(5)分离饱和碳酸钠溶液和乙酸乙酯的方法是_________。
CH3COOC2H5+2H2,在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。当反应温度高于300 ℃时,乙酸乙酯的质量分数迅速下降的原因可能是____。









