-
电石可以与水剧烈反应生成C2H2方程式如下:CaC2+2H2O→C2H2↑+Ca(OH)2。已知:①工业电石中常含有硫化钙、磷化钙等杂质,它们与水作用可以生成硫化氢及磷化氢等恶臭且有毒的还原性气体。②用Hg(NO3)2作催化剂时,浓硝酸能将乙炔气体氧化为草酸(H2C2O4)。实验装置如图所示(夹持装置略去),回答下列问题:
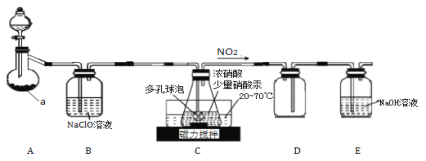
(1)仪器a的名称是___。
(2)装置B中的NaClO溶液能与H2S、PH3反应生成硫酸、磷酸,此过程中NaClO是__(填“氧化剂”或“还原剂”)。
(3)装置D的作用是__。
(4)装置C中生成H2C2O4的化学方程式为___。
(5)为测定晶体中H2C2O4·2H2O的质量分数,实验步骤如下:
i.准确称取mg晶体,加入适量的蒸馏水溶解,再加入少量稀硫酸;
ii.将i所得溶液用cmol/LKMnO4标准溶液进行滴定,滴定时KMnO4被还原为Mn2+,滴定至终点时消耗标准溶液VmL。
①滴定终点的现象是__。
②上述滴定完成后,若滴定管尖嘴处留有气泡会导致测量结果偏__。(填“高”或“低”)。
-
已知:CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都属于离子型化合物;碳化钙(CaC2)和水发生反应制备C2H2的方程式如下:CaC2+2H2O→C2H2↑+Ca(OH)2.请通过CaC2制C2H2的反应进行思考,从中得到必要的启示,判断下列反应产物正确的是( )
A. ZnC2水解生成乙烷(C2H6)
B. Al4C3水解生成丙烷(C3H4)
C. Mg2C3水解生成丙炔(C3H4)
D. Li2C2水解生成乙烯(C2H4)
-
电石中的碳化钙和水能完全反应: CaC2+2H2O→C2H2↑+Ca(OH)2
现在使该反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量。
(1)用下列仪器和导管组装该实验装置:

如果所制气体流向从左向右时,上述仪器和导管从上到下和从左到右直接连接的顺序(填各仪器、导管的序号)是:( )接( )接( )接( )接( )接( );
(2)一般实验产生的气体含有 (填化学式,至少2种)等杂质导致测定结果偏大,通常用 (填化学式)溶液除去;
(3) 实验室制取乙炔时,为了 通常用饱和食盐水代替蒸馏水;
(4)若实验时称取的电石1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448mL,此电石中碳化钙的质量分数是 。
-
I、现有含CaO杂质的CaC2试样。设计以下实验,测定CaC2试样的纯度。(反应方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑),请从下图中选用适当的装置,完成该实验。
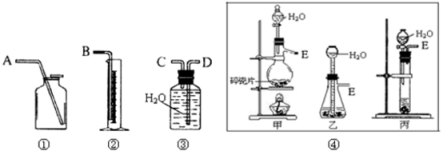
(1)制取C2H2最好选④中的 装置(填“甲”“乙”或“丙”),所选用装置的连接顺序是 (填各接口A~E的顺序)。
(2)若实验时称取的试样为1.4g,产生的乙炔在标准状况下的体积为448mL,此试样中CaC2的质量分数为 。(保留3为有效数字)

II、某同学在实验室从如图标签的试剂瓶中取少许钠进行燃烧实验,实验后 发现还有少许黑色固体生成。从反应物及实验操作猜测:
该黑色物质可能为碳与另一种氧化物组成的混合物。
根据题意和图示回答下面问题:
(1)装置图⑤中A的名称 。
(2)此氧化物可能是 或 (写化学式)。
(3)对黑色固体物质的组成作如图⑥所示研究
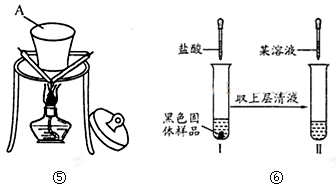
①实验I中加入盐酸溶液的目的是 。
②仅通过实验II,用最简步骤能快速确定黑色氧化物的组成,请完善该设计。(限选试剂:稀盐酸、KSCN溶液、10%H2O2溶液)
| 实验操作 | 预期现象与结论 | 相关离子方程式 |
| 取少量实验I中的澄清溶液,加入试剂 | | |
-
(12分)工业上,可以由下列反应合成三聚氰胺:
CaO+3C CaC2+CO↑;CaC2+N2
CaC2+CO↑;CaC2+N2 CaCN2+C;CaCN2+2H2O=NH2CN+Ca(OH)2
CaCN2+C;CaCN2+2H2O=NH2CN+Ca(OH)2
NH2CN与水反应生成尿素[CO(NH2)2],再由尿素合成三聚氰胺。
(1)写出与Ca在同一周期的Cu原子的基态电子排布式 。
(2)写出CaC2中阴离子C22-的一种等电子体的化学式 。
(3)1mol 尿素分子[CO(NH2)2]中含有的π键与σ键的数目之比为 。
(4)三聚氰胺俗称“蛋白精”,其结构为 。其中氮原子的杂化方式有 。
。其中氮原子的杂化方式有 。
(5)CaO晶胞如下图所示,CaO晶体中与O2-距离最近的O2-的个数为 。CaO晶体的熔点比NaCl晶体的熔点高的主要原因是 。

-
电石中的碳化钙和水能完全反应: CaC2+2H2O=C2H2↑+Ca(OH)2,使反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量。
(1)若用下列仪器和导管组装实验装置:
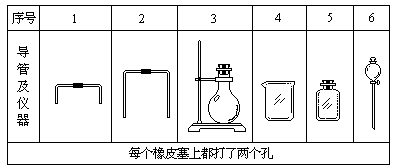
如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是:( )接( )接( )接( )接( )接( )。
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器3中,塞紧橡皮塞。
②检查装置的气密性。
③在仪器6和5中注入适量水。
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计)。
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不发生气体时,关闭活塞。
正确的操作顺序(用操作编号填写)是 。
(3)若实验产生的气体有难闻的臭鸡蛋这是因为含有 杂质。检验此杂质的反应为 。
(4)若实验时称取的电石1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448mL,此电石中碳化钙的质量分数是 %。
-
电石中的碳化钙和水能完全反应:CaC2+2H2O=C2H2↑+Ca(OH)2使反应产生的气体排水,测量排出水的体积,可计算出标准状况下乙炔的体积,从而可测定电石中碳化钙的含量。
(1)若用下列仪器和导管组装实验装置
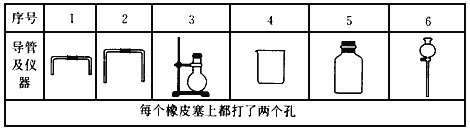
如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是:____接____接____接____接____接____。
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器3中,塞紧橡皮塞。
②检查装置的气密性。
③在仪器6和5中注入适量水。
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计)。
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不产生气体时,关闭活塞。
正确的操作顺序(用操作编号填写)是__________________。
(3)若实验产生的气体有难闻气味,且测定结果偏大,这是因为电石中含有___________杂质。
(4)若实验时称取的电石1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448mL,此电石中碳化钙的质量分数是_________%。
-
草酸是一种二元弱酸,可用作还原剂、沉淀剂等。某校课外小组的同学设计利用C2H2气体制取H2C2O4·2H2O。回答下列问题:
(1)甲组的同学以电石(主要成分CaC2,少量CaS及Ca3P2杂质等)为原料,并用下图1装置制取C2H2。
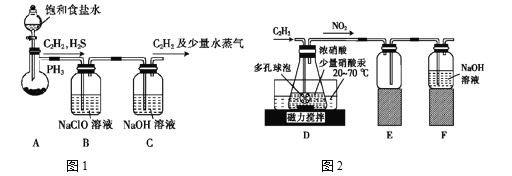
①电石与水反应很快,为了减缓反应速率,装置A中除用饱和食盐水代替水之外,还可以采取的措施是__________(写一种即可)。
②装置B中,NaClO将H2S、PH3 氧化为硫酸及磷酸,本身被还原为NaCl,其中PH3被氧化的离子方程式为______。该过程中,可能产生新的杂质气体Cl2,其原因是: _____________(用离子方程式回答)。
(2)乙组的同学根据文献资料,用Hg(NO3)2作催化剂,浓硝酸氧化C2H2制取H2C2O4·2H2O。制备装置如上图2所示:
①装置D中多孔球泡的作用是______________________。
②装置D中生成H2C2O4的化学方程式为____________________________。
③从装置D中得到产品,还需经过_____________(填操作名称)、过滤、洗涤及干燥。
(3)丙组设计了测定乙组产品中H2C2O4·2H2O的质量分数实验。他们的实验步骤如下:准确称取m g产品于锥形瓶中,加入适量的蒸馏水溶解,再加入少量稀硫酸,然后用c mol·L-1酸性KMnO4标准溶液进行滴定至终点,共消耗标准溶液V mL。
①滴定终点的现象是______________________。
②滴定过程中发现褪色速率开始很慢后逐渐加快,分析可能的原因是_______________。
③产品中H2C2O4·2H2O的质量分数为_______________(列出含 m、c、V 的表达式)。
-
CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都同属于离子型碳化物。请通过对CaC2制C2H2的反应(CaC2+2H2O→Ca(OH)2+C2H2)进行思考,从中得到必要的启示,判断下列反应产物正确的是
A.ZnC2水解生成乙烷(C2H6) B.Al4C3水解生成丙炔(C3H4)
C.Mg2C3水解生成丙炔(C3H4) D.Li2C2水解生成乙烯(C2H4)
-
三聚氰胺可以用以下三个反应合成:CaO+3C=CaC2+CO↑,CaC2+N2=CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排
布式:_____________________________________________。
CaCN2中阴离子为CN ,与CN
,与CN 互为等电子体的分子有________(填两种化学式),由此可以推知CN
互为等电子体的分子有________(填两种化学式),由此可以推知CN 的空间构型为________,画出CN
的空间构型为________,画出CN 电子式___________。
电子式___________。
(2)尿素分子中C原子采取________杂化。尿素分子的结构简式是________。
(3)三聚氰胺( )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸( )后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
)后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为________。CaO晶体和NaCl晶体的晶格能分别为:CaO 3401 kJ·mol-1、NaCl 786 kJ·mol-1。导致两者晶格能差异的主要原因是______________。










 )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸( )后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
)后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。