常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol·L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是

A.曲线起点处水的电离程度最大,可用pH试纸测定溶液pH
B.②点之前所发生反应的离子方程式为Cl2+H2O=2H++Cl-+ClO-
C.氯气~氯水体系中:c(H+)=c(Cl2) +c(HClO)+c(ClO-)
D.③点所示溶液中:c(Na+) = c(Cl-)+c(ClO-)
高三化学单选题中等难度题
常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol·L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是

A.曲线起点处水的电离程度最大,可用pH试纸测定溶液pH
B.②点之前所发生反应的离子方程式为Cl2+H2O=2H++Cl-+ClO-
C.氯气~氯水体系中:c(H+)=c(Cl2) +c(HClO)+c(ClO-)
D.③点所示溶液中:c(Na+) = c(Cl-)+c(ClO-)
高三化学单选题中等难度题
常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol·L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是
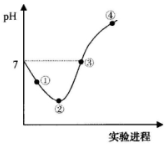
A.②点之前所发生反应的离子方程式为Cl2+H2O=2H++Cl-+ClO﹣
B.③点所示溶液中:c(Na+)= c(HClO)+2c(ClO-)
C.实验进程中溶液的pH可以用pH试纸测得
D.曲线的起始点水的电离程度最大
高三化学选择题中等难度题查看答案及解析
常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol·L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是
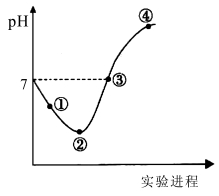
A.曲线起点处水的电离程度最大,可用pH试纸测定溶液pH
B.②点之前所发生反应的离子方程式为Cl2+H2O=2H++Cl-+ClO-
C.氯气~氯水体系中:c(H+)=c(Cl2) +c(HClO)+c(ClO-)
D.③点所示溶液中:c(Na+) = c(Cl-)+c(ClO-)
高三化学选择题困难题查看答案及解析
常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol·L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是

A.曲线起点处水的电离程度最大,可用pH试纸测定溶液pH
B.②点之前所发生反应的离子方程式为Cl2+H2O=2H++Cl-+ClO-
C.氯气~氯水体系中:c(H+)=c(Cl2) +c(HClO)+c(ClO-)
D.③点所示溶液中:c(Na+) = c(Cl-)+c(ClO-)
高三化学单选题中等难度题查看答案及解析
常温下,将Cl2缓慢通入100 mL水中至饱和,然后向所得饱和氯水中逐滴加入0.1 mol·L-1 NaOH溶液,整个过程中pH的变化如图所示。下列有关叙述正确的是
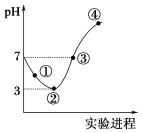
A. 曲线③④段有离子反应:HClO+OH-===ClO-+H2O
B. 可依据②处数据计算所溶解的n(Cl2)
C. ③处表示氯气与氢氧化钠溶液恰好反应完全
D. ①处c(H+)约为②处c(H+)的两倍
高三化学单选题中等难度题查看答案及解析
常温下,将Cl2缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol/L NaOH溶液,整个过程中pH的变化如图所示。下列有关叙述中正确的是
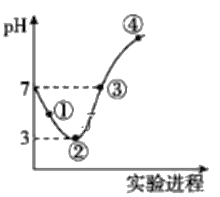
A. 曲线③④段有离子反应:HClO+OH-=ClO-+H2O
B. 可依据②处数据计算所溶解的n(Cl2)
C. ③处表示氯水与氢氧化钠溶液恰好反应完全
D. ①处c(H+)约为②处c(H+)的两倍
高三化学单选题中等难度题查看答案及解析
常温下,将Cl2缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加入0.1 mol/L NaOH溶液,整个过程中pH的变化如图所示。下列有关叙述正确的是( )
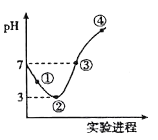
A.用pH试纸测①处c(H+)约为②处c (H+)的两倍
B.可依据②处数据计算所溶解的n(Cl2)
C.③处表示溶液中,c(Na+)= c(ClO-) + c(Cl-)
D.曲线③④段有离子反应:HClO+OH-=ClO-+H2O
高三化学多选题困难题查看答案及解析
在常温下,取一定量的蒸馏水,然后将Cl2缓慢通入水中至饱和,再向所得饱和氯水中滴加0.1mol/L的NaOH溶液。整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是
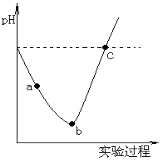
A.实验进程中可用pH试纸测定溶液的pH
B.向a点所示溶液中能入SO2,溶液的酸性和漂白性均增强
C.由a点到b点的过程中,溶液中c(H+)/c(ClO-)减小
D.c点所示的溶液中,c(Na+)= c(ClO-) + c(Cl-)
高三化学选择题简单题查看答案及解析
在常温下,取一定量的蒸馏水,然后将Cl2缓慢通入水中至饱和,再向所得饱和氯水中滴加0.1mol/L的NaOH溶液。整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是

A.实验进程中可用pH试纸测定溶液的pH
B.向a点所示溶液中能入SO2,溶液的酸性和漂白性均增强
C.由a点到b点的过程中,溶液中c(H+)/c(ClO-)减小
D.c点所示的溶液中,c(Na+)= c(ClO-) + c(Cl-)
高三化学选择题简单题查看答案及解析
常温常压下,将C12缓慢通入100 mL水中至饱和,然后向所得饱和氯水中逐滴加入0.1 mol·L-1 NaOH溶液,整个过程溶液中H+的浓度变化如图所示。(已知常温常压下C12溶于水时,只有部分C12会和水发生反应)下列叙述正确的是
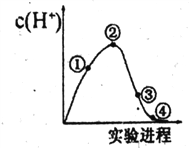
A.①处溶液的酸性比②处溶液的酸性强
B.依据②处c(H+)可计算溶解的C12的物质的量
C.整个实验过程中,溶液的颜色先变深后变浅,最后变为无色
D.④处表示C12与NaOH溶液恰好完全反应,共转移了0.1mol电子
高三化学单选题中等难度题查看答案及解析
常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液,整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是

A.实验进程中可用pH试纸测定溶液的pH
B.a点的溶液中:c(H+)=c(Cl-)+c(HClO)+c(OH-)
C.c点所示溶液中:c(Na+)=2c(ClO-)+c(HClO)
D.由a点到b点的过程中,溶液中 减小
减小
高三化学单选题困难题查看答案及解析