-
常温下,下列说法不正确的是
A.0.2mol/L的NaHCO3溶液的pH>7,则溶液中:c(H2CO3)>c(CO32-)
B.叠氮酸(HN3)与醋酸酸性相近,0.1mol/LNaN3水溶液中离子浓度的大小顺序为c(Na+)>c(N3-)>c(OH-)>c(H+)
C.向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+)=c(Cl-)
D.0.02mol/L的NaOH溶液与0.02mol/L的NaHC2O4溶液等体积混合后溶液中:c(OH-)+c(C2O42-)=c(HC2O4-)+2c(H+)
高三化学单选题中等难度题查看答案及解析
-
常温下,向Na2CO3溶液中逐滴滴入0.1mol/L盐酸,溶液的pH随着滴入盐酸溶液体积变化曲线如下图,则下列说法正确的是

A.a点时溶液pH=11.5,原因是:CO32-+2H2O → H2CO3+2OH-
B.a-b段发生反应为:CO32-+2H+→ CO2↑+H2O
C.b-c段发生反应为:HCO3-+H+→ CO2↑+H2O
D.c-d段发生反应为:H++OH-→ H2O
高三化学选择题中等难度题查看答案及解析
-
已知在常温下测得浓度均为0.1 mol·L-1的下列三种溶液的pH:
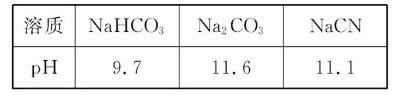
下列说法中正确的是( )
A.阳离子的物质的量浓度之和:Na2CO3>NaCN>NaHCO3
B.相同条件下的酸性:H2CO3<HCN
C.三种溶液中均存在电离平衡和水解平衡
D.升高Na2CO3溶液的温度,
减小
高三化学选择题中等难度题查看答案及解析
-
常温下含碳各微粒H2CO3、HCO3-和CO32-存在于CO2和NaOH溶液反应后的溶液中,它们的物质的量分数与溶液pH的关系如图所示,下列说法错误的是( )

A. 为获得尽可能纯的NaHCO3,宜控制溶液的pH为7~9之间
B. pH=10.25时,c(Na+)=c(CO32-)+c(HCO3-)
C. 根据图中数据,可以计算得到H2CO3第一步电离的平衡常数K1(H2CO3)=10-6.37
D. 若是0.1mol NaOH反应后所得的1L溶液,pH=10时,溶液中存在以下关系: c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
高三化学单选题中等难度题查看答案及解析
-
下列说法不正确的是
A.NaHCO3和Na2CO3混合溶液中:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
B.常温下,浓度均为0.1 mol·L-1下列各溶液的pH:NaOH>Na2CO3> NaHCO3> NH4Cl
C.向冰醋酸中逐滴加水,醋酸的电离程度、pH均先增大后减小
D.常温下,pH=1的稀硫酸与醋酸溶液中,c (SO42-)与c(CH3COO-)之比为2∶1
高三化学选择题中等难度题查看答案及解析
-
下图是某水溶液常温下pH 从0 到14 的范围内H2CO3、HCO3-、CO32- 三种成分平衡时组成分数,下列叙述正确的是
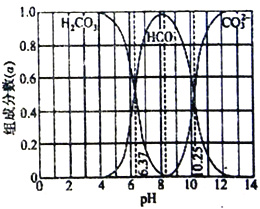
A. 此图是1.0mol/L碳酸钠溶液滴定1.0mol/L 盐酸的滴定曲线
B. 向pH=10.25 的溶液中通HCl 气体使pH=7,此时c(H2CO3)>c(Cl-)= c(HCO3-)>c(CO32- )
C. 人体血液的pH 约为7.4,则CO2在血液中多以HCO3-形式存在
D. 该温度下,碳酸氢根的水解平衡常数Kh= 10-3.75
高三化学单选题困难题查看答案及解析
-
常温时,配制一组c(Na2CO3)+c(NaHCO3)=0.100 mol·L-1的混合溶液,溶液中c(CO32-)、c(HCO3-)与pH的关系如图所示。下列说法中错误的是
(己知:CO32-+H2O
HCO3-+OH- K=2×10-4,1g5=0.7)

A. a点的溶液中:c(HCO3-)> c(H2CO3)+c(CO32-)
B. b点横坐标数值大约为10.3
C. c点的溶液中:c(Na+)<2c(CO32-)十c(HCO3-)
D. 溶液中水的电离程度:a<b<c
高三化学单选题困难题查看答案及解析
-
常温时,在H2CO3溶液中逐滴加入NaOH溶液,溶液中H2CO3、HCO3-和CO32-的物种分布分数
(X)=
与pH的关系如图所示:
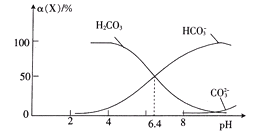
下列说法正确的是
A. 反应HCO3-
H++CO32-的lgK=-6.4
B. pH═8的溶液中:c(Na+)>c(HCO3-)
C. NaHCO3溶液中滴入少量盐酸至溶液显中性:c(Na+)═c(Cl-)
D. 向pH=6.4的溶液中滴加NaOH溶液至pH=8,主要发生的离子反应:HCO3-+OH-═CO32-+H2O
高三化学单选题困难题查看答案及解析
-
常温时,在H2CO3溶液中逐滴加入NaOH溶液,溶液中H2CO3、HCO3-和CO32-的物种分布分数
(X)=
与pH的关系如图所示:
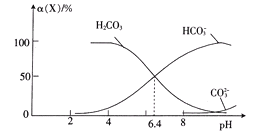
下列说法正确的是
A. 反应HCO3-
H++CO32-的lgK=-6.4
B. pH═8的溶液中:c(Na+)>c(HCO3-)
C. NaHCO3溶液中滴入少量盐酸至溶液显中性:c(Na+)═c(Cl-)
D. 向pH=6.4的溶液中滴加NaOH溶液至pH=8,主要发生的离子反应:HCO3-+OH-═CO32-+H2O
高三化学单选题困难题查看答案及解析
-
常温时,在H2CO3溶液中逐滴加入NaOH溶液,溶液中H2CO3、HCO3-和CO32-的物种分布分数
(X)=
与pH的关系如图所示:
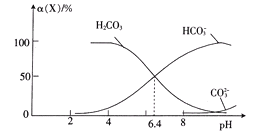
下列说法正确的是
A. 反应HCO3-
H++CO32-的lgK=-6.4
B. pH═8的溶液中:c(Na+)>c(HCO3-)
C. NaHCO3溶液中滴入少量盐酸至溶液显中性:c(Na+)═c(Cl-)
D. 向pH=6.4的溶液中滴加NaOH溶液至pH=8,主要发生的离子反应:HCO3-+OH-═CO32-+H2O
高三化学单选题困难题查看答案及解析