已知:2Fe3++SO32-+H2O2Fe2++SO42-+2H+,如图所示是一套电化学实验装置,图中C、D均为铂电极,U为盐桥,A是灵敏电流表,其指针总是偏向电源负极,A杯中为FeCl3溶液;B杯中为Na2SO3溶液。以下关于该装置的说法错误的是( )
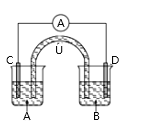
A.A指针向右偏转
B.U中阳离子向左烧杯移动
C.一段时间后,化学反应达到平衡状态,导线中无电流通过
D.一段时间后,右烧杯中溶液pH增大
高二化学单选题中等难度题
已知:2Fe3++SO32-+H2O2Fe2++SO42-+2H+,如图所示是一套电化学实验装置,图中C、D均为铂电极,U为盐桥,A是灵敏电流表,其指针总是偏向电源负极,A杯中为FeCl3溶液;B杯中为Na2SO3溶液。以下关于该装置的说法错误的是( )

A.A指针向右偏转
B.U中阳离子向左烧杯移动
C.一段时间后,化学反应达到平衡状态,导线中无电流通过
D.一段时间后,右烧杯中溶液pH增大
高二化学单选题中等难度题
已知:2Fe3++SO32-+H2O2Fe2++SO42-+2H+,如图所示是一套电化学实验装置,图中C、D均为铂电极,U为盐桥,A是灵敏电流表,其指针总是偏向电源负极,A杯中为FeCl3溶液;B杯中为Na2SO3溶液。以下关于该装置的说法错误的是( )

A.A指针向右偏转
B.U中阳离子向左烧杯移动
C.一段时间后,化学反应达到平衡状态,导线中无电流通过
D.一段时间后,右烧杯中溶液pH增大
高二化学单选题中等难度题查看答案及解析
某化学研究性学习小组讨论Fe3+和SO32-之间发生怎样的反应,提出了两种可能:一是发生氧化还原反应2Fe3++SO32-+H2O=2Fe2++SO42-+2H+;二是发生水解相互促进反应2Fe3++3SO32-+6H2O=2Fe(OH)3(胶体)+3H2SO3。为了证明是哪一种反应发生,同学们设计并实施了下列实验,请填写下列空白:
实验Ⅰ,学生选择的实验用品:Na2SO3浓溶液、BaCl2稀溶液、稀盐酸;试管若干、胶头滴管若干。从选择的药品分析,设计这个实验的目的是___________________________。
实验Ⅱ,取5 mL FeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色。这种红褐色液体是________。向红褐色液体中逐滴加入稀盐酸至过量,可以观察到的现象是__________________________________。
将溶液分成两等份,其中一份加入KSCN溶液,溶液变成血红色,反应的离子方程式为_______________________________________________________。
另一份加入BaCl2稀溶液,有少量白色沉淀生成,产生该白色沉淀的离子方程式是___________________________________________________________。
实验Ⅲ,换用稀释的FeCl3溶液和Na2SO3溶液重复实验Ⅱ,产生的现象完全相同。由上述实验得出的结论是_______________________。.
若在FeCl3浓溶液中加入Na2CO3浓溶液,观察到红褐色沉淀并且产生无色气体,该反应的化学方程式是_____________________________________________________________。
从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,二者的水溶液与氯化铁溶液反应的现象差别很大,分析其原因可能是:
①_______________________________________________________________;
②_____________________________________________________________。
高二化学实验题困难题查看答案及解析
某化学研究性学习小组讨论Fe3+和SO32—之间发生怎样的反应,提出了两种可能:
一是发生氧化还原反应:2Fe3++SO32—+H2O=2Fe2++SO42—+2H+;
二是发生双水解反应:2Fe3++3SO32—+6H2O=2Fe(OH)3(胶体)+3H2SO3。
为了证明是哪一种反应发生,同学们设计并实施了下列实验,请填写下列空白:
【实验Ⅰ】学生选择的实验用品:Na2SO3浓溶液、BaCl2稀溶液、稀盐酸;试管若干、胶头滴管若干。从选择的药品分析,作者设计这个实验的目的是________。
【实验Ⅱ】取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色。这种红褐色“液体”是________;向红褐色液体中逐滴加入稀盐酸至过量,可以观察到的现象是.________;
将溶液分成两等份,其中一份加入KSCN溶液,溶液变成血红色,另一份加入BaCl2稀溶液,有少量白色沉淀生成。产生血红色现象的离子方程式是________。
【实验Ⅲ】换用稀释的FeCl3和Na2SO3溶液重复实验,Ⅱ、Ⅲ产生的现象完全相同。由上述实验得出的结论是________;
若在FeCl3浓溶液中加入Na2CO3浓溶液,观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是. 。
从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,二者的水溶液与氯化铁溶液反应的现象差别很大,分析其原因可能是:
①________;
②________。
高二化学填空题简单题查看答案及解析
已知:①SO32-+I2+H2O→SO42-+2I-+2H+②2Fe3++2I-→2Fe2++I2某溶液中可能含有少量Na+、NH4+、Fe2+、K+、I−、SO32-、SO42-。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是( )
A.肯定含有SO32- B.肯定不含K+ C.肯定不含I− D.肯定含有NH4+
高二化学单选题中等难度题查看答案及解析
为了探究化学反应速率和化学反应限度的有关问题,某研究小组进行了以下实验:
实验一:
利用如图装置测定化学反应速率(已知:S2O32-+2H+═H2O+S↓+SO2↑)

(1)除如图装置所示的实验用品外,还需要的一种实验用品是________。
A.温度计 B.秒表 C.酒精灯
(2)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H+的反应速率,而该测定值比实际值偏小,其原因是__________。
实验二:
为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表。(已知 I2+2S2O32-═S4O62-+2I-,其中Na2S2O3溶液均足量)
| 实验序号 | 体积V/mL | 时间/s | |||
| Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
| ① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
| ② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
| ③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
(3)表中Vx=____mL,t1、t2、t3的大小关系是________。
实验三:
取5mL0.1mol/L的KI溶液于试管中,滴加0.1 mol·L-1 FeCl3溶液溶液2mL,发生如下反应:2Fe3++2I-==2Fe2++I2.为证明该反应达到一定可逆性且具有限度,他们设计了如下实验:
①取少量反应液,滴加AgNO3溶液,发现有少量黄色(AgI)沉淀;
②再取少量反应液,滴加少量CCl4,振荡,发现CCl4层显浅紫色.
根据①②的现象,他们得出结论:该反应具有一定的可逆性,在一定条件下会达到反应限度.
(4)指导老师指出他们上述实验中①不合理,你认为其原因是__________;改进的方法是_______。
(5)有人认为步骤②适合检验生成I2较多的情况下,还有一种简便方法可以灵敏地检验是否生成了I2,这种方法所用的试剂是____________________。
高二化学填空题简单题查看答案及解析
Ⅰ.测定化学反应速率
某同学利用如图装置测定化学反应速率。
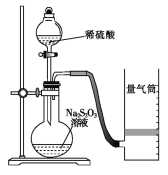
(已知:S2O32-+2H+=H2O+S↓+SO2↑)
(1)为保证实验准确性、可靠性,利用该装置进行实验前应先进行的步骤是__;除如图所示的实验用品、仪器外,还需要的一件实验仪器是__。
(2)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H+的反应速率,而该测定值比实际值偏小,其原因是___。
Ⅱ.为探讨化学反应速率的影响因素
某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。已知:5H2C2O4+2KMnO4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
实验时,通过测定褪色所需时间来判断反应的快慢。限选试剂与仪器:0.20mol/LH2C2O4溶液,0.010mol/L酸性KMnO4溶液,蒸馏水,锥形瓶,恒温水浴槽,量筒,秒表。该小组设计了如下的方案。
| 物理量 | 水 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 体积/mL | 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | ||
| ① | 0 | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
| ② | 0 | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 1.0 | 0.010 | 4.0 | 25 |
(1)已知反应后H2C2O4转化为CO2逸出,KMnO4转化为MnSO4。为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为:n(H2C2O4):n(KMnO4)≥__。
(2)实验③测得KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=__mol·L-1·min-1。
(3)请完成表格内二处空白__、__。
(4)已知50℃时c(MnO4-)~反应时间t的变化曲线如图。其中反应速率最快的阶段是__,原因是___。
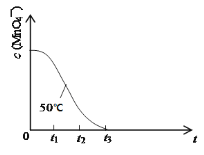
高二化学实验题中等难度题查看答案及解析
往含 Fe3+、H+、NO3-的混合液中加入少量 SO32-,下列表示该反应的离子方程式正确的是( )
A.2Fe3++SO32-+H2O=2Fe2++SO42-+2H+
B.2H++2NO3-+3SO32-=3 SO42-+2NO↑+H2O
C.2H++SO32-=H2O+SO2↑
D.2Fe3++3 SO32-+3H2O=2Fe(OH)2↓+3SO2↑
高二化学单选题中等难度题查看答案及解析
下面是某同学测定化学反应速率并探究其影响因素的实验。
Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率。
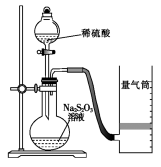
(已知:S2O32-+2H+ = H2O+S↓+SO2↑)
(1)除如图所示的实验用品、仪器外,还需要的一件实验仪器是__________________。
(2)若在2 min时收集到224 mL(已折算成标准状况)气体,可计算出该2 min内H+的反应速率,而该测定值比实际值偏小,其原因是 。
(3)试简述测定该反应的化学反应速率的其他方法: (写一种)。
Ⅱ.为探讨化学反应速率的影响因素,设计的实验方案如下表。
(已知 I2+2S2O32- = S4O62-+2I-,其中Na2S2O3溶液均足量)
| 实验序号 | 体积V/mL | 时间/s | |||
| Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
| ① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
| ② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
| ③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
(4)该实验进行的目的是 ,淀粉溶液的作用是 ,表中Vx= mL,通过比较t1、t2、t3大小,试推测该实验结论:
高二化学实验题困难题查看答案及解析
已知铅蓄电池的工作原理为Pb+PbO2+2H2SO42PbSO4+2H2O。现用如图装置进行电解实验,测得当铅蓄电池中转移0.4mol电子时,铁电极的质量减少11.2g.(铁的相对原子质量:56)请回答下列问题:
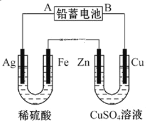
①A是铅蓄电池的__________极,
②Ag电极的电极反应式是__________,该电极的电极产物有__________g.
③Cu电极的电极反应式是__________,CuSO4溶液的浓度__________(填“减小”“增大”或“不变”)。
④如图表示电解进行过程中某个物理量x随时间t的变化曲线,其中曲线Ⅰ表示左侧U形管中的变化,曲线Ⅱ表示右侧U形管中的变化,则x表示(_______)
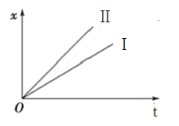
A.U形管中产生的气体的体积 B.U形管中阳极质量的减少量C.U形管中阴极质量的增加量
高二化学填空题简单题查看答案及解析
某研究组设想以如图所示装置用电化学原理生产硫酸。关于该装置的叙述正确的是
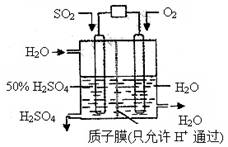
A.该装置为原电池,通入O2的电极是负极
B.该装置中,通入SO2的电极的电极反应式为:SO2+O2-+H2O -2e- =2H++SO42-
C.该装置中,H+通过质子膜向左侧移动
D.在标准状况下,理论上每消耗11.2L SO2,则可产生0.5mol H2SO4
【解析】氧气是得电子得,所以氧气在正极通入。SO2在反应中失去电子,在负极通入,所失去得电子经导线传递到正极上,所以溶液中得阳离子向正极移动。因为交换膜只允许氢离子通过,所以负极得电极反应式为SO2+2H2O -2e-=4H++SO42-。所以正确的答案是D。
高二化学选择题简单题查看答案及解析