-
甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
i CO2(g)+ 3H2(g)
CH3OH(g)+ H2O(g) ∆H1=Q kJ·mol-1
ii. CO2(g)+ H2(g)
CO(g)+H2O(g) ∆H2=+41 kJ·mol-1
iii. CO(g)+2H2(g)
CH3OH(g) ∆H3=− 99 kJ·mol-1
回答下列问题:
(1)Q=_________
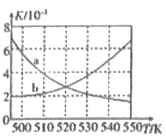
(2)图中能正确反映平衡常数K3(反应iii的平衡常数)随温度变化关系的曲线为__(填字母)
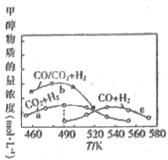
(3)如图为单位时间内CO2+H2、CO+ H2、CO/CO2+H2三个条件下生成甲醇的物质的量浓度与温度的关系(三个条件下通入的CO、CO2和H2的物质的量浓度相同)。490K时,根据曲线a、c判断合成甲醇时主要发生的反应为________(填“i”或“iii”);由曲线a可知,甲醇的量先增大后减小,其原因是_________________________________。
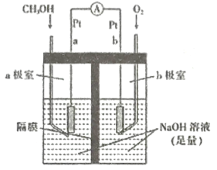
(4)如图是以NaOH溶液为电解质溶液的甲醇燃料电池:电极a的反应式为____________,若隔膜为阳离子交换膜,则每转移6mol电子,溶液中有_______mol Na+向____________(填“正极区”或“负极区")移动。
(5)CO2经催化加氢也可以生成低碳烃,主要有两个竞争反应:
反应I:CO2(g)+4H2(g)
CH4(g)+2H2O(g)
反应II :2CO2(g)+6H2(g)
C2H4(g)+4H2O(g)
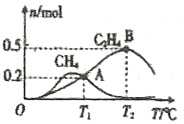
在1L恒容密闭容器中充入2molCO2和4molH2测得平衡时有关物质的物质的量随温度变化如图所示。T1℃时,CO2的转化率为______。T1℃时,反应I的平衡常数K=_________(保留三位有效数字)。
高三化学综合题简单题查看答案及解析
-
(1)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)
CH3OH(g) ΔH1
②CO2(g)+3H2(g)
CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g)
CO(g)+H2O(g) ΔH3
回答下列问题:
已知反应①中相关的化学键键能数据如下:
化学键
H—H
C—O
C≡O
H—O
C—H
E/(kJ·mol-1)
436
343
1 076
465
413
由此计算ΔH1=________kJ·mol-1;已知ΔH2=-58 kJ·mol-1,则ΔH3=________kJ·mol-1。
(2)烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
NO(g)+O3(g)===NO2(g)+O2(g) ΔH=-200.9 kJ·mol-1
NO(g)+
O2(g)===NO2(g) ΔH=-58.2 kJ·mol-1
SO2(g)+O3(g)===SO3(g)+O2(g) ΔH=-241.6 kJ·mol-1
则反应3NO(g)+O3(g)===3NO2(g)的ΔH=________kJ·mol-1。
高三化学填空题中等难度题查看答案及解析
-
甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
①CO2(g)+3H2(g)
CH3OH(g)+H2O(g) ΔH1
②CO2(g)+H2(g)
CO(g)+H2O(g) ΔH2
③CH3OH(g)
CO(g)+2H2(g) ΔH3
(1)已知反应②中相关化学键键能数据如下:
化学键
H-H
C=O
C≡O
H-O
E/kJ·mol-1
436
803
1076
465
由此计算ΔH2=____kJ·mol-1。已知ΔH3=+99kJ·mol-1,则ΔH1=____kJ·mol-1。
(2) 一定比例的合成气在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图所示。
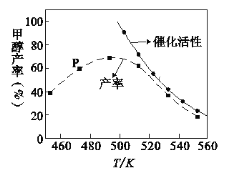
①温度为470K时,图中P点____(填“是”或“不是”)处于平衡状态,490K之后,甲醇产率随温度升高而减小的原因除了升高温度使反应①平衡逆向移动以外,还有___________________________________________________________、______________________________________________________________________。
②一定能提高甲醇产率的措施是______。
A.增大压强 B.升高温度 C.选择合适催化剂 D.加入大量催化剂
(3)如图为一定比例的CO2+H2,CO+H2、CO/CO2+H2条件下甲醇生成速率与温度的关系。
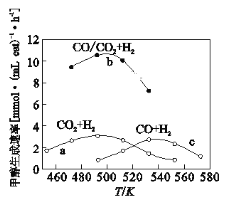
①490K时,根据曲线a、c判断合成甲醇的反应机理是______(填I或II)
Ⅰ.CO2
CO
CH3OH
II.CO
CO2
CH3OH+H2O
②490K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,从平衡移动的角度,结合反应①、②分析原因___________________________。
高三化学综合题困难题查看答案及解析
-
甲醇是重要的化工原料,又可称为燃料。工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)
CH3OH(g) △H
②CO2(g)+3H2(g)
CH3OH(g)+H2O(g) △H2=-58kJ•mol-1
③CO2(g)+H2(g)
CO(g)+H2O(g) △H3=+41kJ•mol-1
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:

则x=____________;
(2)若T℃时将6molCO2和8molH2充入2L密闭容器中发生反应②,测得H2的物质的量随时间变化关系如图中状态I(图中实线)所示。图中数据A(1,6)代表在1min时H2的物质的量是6mol。
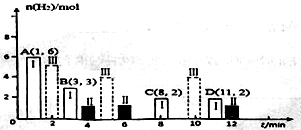
①T℃时状态I条件下,0~3min内CH3OH的平均反应速率v=_______mol/(L·min),平衡常数K=_____;
②其他条件不变时,仅改变某一条件后测得H2的物质的量随时间变化如图中状态Ⅱ所示,则改变的条件可能是_____;
③其他条件不变,仅改变温度时,测得H2的物质的量随时间变化如图中状态Ⅲ所示,则状态Ⅲ对应的温度_______(填“>”、“<”或“=”)T℃;
④若状态Ⅱ的平衡常数为K2,状态Ⅲ的平衡常数为K3,则K2_______(填“>”、“<”或“=”)K3;
⑤一定温度下同,此反应在恒容容器中进行,能判断该反应达到化学平衡依据的是_______。
a.容器中压强不变
b.甲醇和水蒸汽的体积比保持不变
c.v正(H2)=3v逆CH3OH)
d.2个C=O断裂的同时有6个H—H断裂
高三化学填空题困难题查看答案及解析
-
甲醇既是重要的化工原料,又可作为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)
CH3OH(g) ΔH1
②CO2(g)+3H2(g)
CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g)
CO(g)+H2O(g) ΔH3
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
化学键
H﹣H
C﹣O
C≡O
H﹣O
C﹣H
E/( kJ•mol-1)
436
343
1076
465
413
由此计算ΔH1=______。已知ΔH2=﹣58 kJ•mol-1,则ΔH3=______。
(2)合成气中的氢气是发展中的新能源,它的利用包括制备、储存和应用三个环节。与汽油相比,氢气作为燃料的优点是__________________________________________________________(写出两点),缺点是______________________________________________________________________(写出两点)。
高三化学填空题简单题查看答案及解析
-
甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
i. CO2(g)+3H2(g)
CH3OH(g)+H2O(g) △H1
ii. CO2(g)+ H2(g)
CO(g)+H2O(g) △H2
iii. CH3OH(g)
CO(g) +2H2(g) △H3
回答下列问题:
(1)已知反应ⅱ中相关化学键键能数据如下:
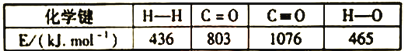
由此计算△H2=__________kJ·mol-1。已知△H3=99kJ·mol-1,则△H1=_________kJ·mol-1。
(2)一定比例的合成气在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图1所示。
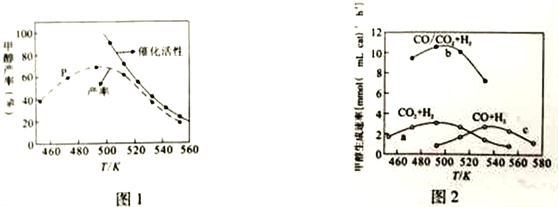
①温度为470K时,图中P点_______ (填“是”或“不是”)处于平衡状态。在490K之前,甲醇产率随着温度升高而增大的原因是_______;490K之后,甲醇产率下降的原因是_______。
②一定能提高甲醇产率的措施是______________。
A.增大压强 B,升高温度 C.选择合适催化剂 D.加入大量催化剂
(3)图2为一定比例的CO2/H2,CO/H2、CO/CO2/H2条件下甲醇生成速率与温度的关系。
①490K时,根据曲线a、c判断合成甲醇的反应机理是_________ (填“I”或“II")。

②490K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,从热力学与动力学角度,并结合反应i、ⅱ分析原因_________。
高三化学综合题困难题查看答案及解析
-
甲醇是重要的化工原料。利用合成气(主要成分为(CO,CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
i:CO2(g)+3H2(g)
CH3OH(g)+H2O(g) ΔH1
ii:CO2(g)+H2(g)
CO(g)+H2O(g) ΔH2
iii:CH3OH(g)
CO(g)+2H2(g) ΔH3
回答下列问题:
(1)已知反应2中相关化学键键能数据如下:
化学键
H—H
C=O
C≡O
H—O
E/KJ·mol-1
436
803
1076
465
由此计算ΔH2=___kJ·mol-1。已知ΔH1=-63kJ·mol-1,则ΔH3=___kJ·mol-1。
(2)对于反应1,不同温度对CO2的平衡转化率及催化剂的效率影响如图所示,请回答下列问题:
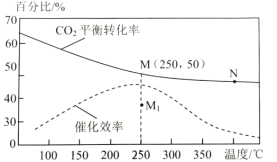
①下列说法不正确的是(__________)
A.M点时平衡常数比N点时平衡常数大
B.温度低于250℃时,随温度升高甲醇的平衡产率降低
C.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于M1
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
②若在刚性容器中充入3molH2和1molCO2发生反应1,起始压强为4MPa,则图中M点CH3OH的体积分数为___,250℃时反应的平衡常数Kp=___(MPa)-2(保留三位有效数字);
③若要进一步提高甲醇产率,可采取的措施有___(写两条即可)
(3)相同条件下,一定比例CO/CO2/H2混合气体甲醇生成速率大于CO2/H2混合气体甲醇生成速率,结合反应1、2分析原因:___。
(4)以二氧化钛表面覆盖Cu2A12O4为催化剂,可以将CO2和CH4直接转化成乙酸,CO2(g)+CH4(g)
CH3COOH(g),在不同温度下催化剂的催化效率与乙酸的生成速率如图所示:
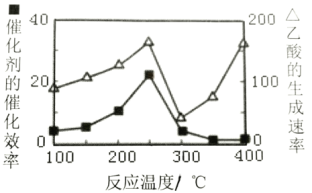
250~300℃时,乙酸的生成速率降低的主要原因是___。
300~400℃时,乙酸的生成速率升高的主要原因是___。
高三化学综合题困难题查看答案及解析
-
甲醇是重要的化工原料,又可做为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
Ⅰ CO(g)+2H2(g)
CH3OH(g) ∆H1
Ⅱ CO2(g)+3H2(g)
CH3OH(g)+H2O(g) ∆H2=-58kJ/mol
Ⅲ CO2(g)+H2(g)
CO(g)+H2O(g) ∆H3
回答下列问题:
(1)物质的标准生成热是常用的化学热力学数据,可以用来计算化学反应热。即化学反应热:∆H=生成物标准生成热总和-反应物标准生成热总和。
已知四种物质的标准生成热如下表:
物质
CO
CO2
H2
CH3OH(g)
标准生成热(kJ/mol)
-110.52
-393.51
0
-201.25
A.计算∆H1=_______kJ/mol B.∆H3______0(填=、<、>)
(2)由甲醇在一定条件下制备甲醚。一定温度下,在三个体积均为1.0L的恒容密闭容器中发生反应:2CH3OH(g)
CH3OCH3(g)+H2O(g)。实验数据见下表:
容器编号
温度(℃)
起始物质的量(mol)
平衡物质的量(mol)
CH3OH(g)
CH3OCH3(g)
H2O(g)
CH3OCH3(g)
H2O(g)
a
387
0.20
0
0
0.080
0.080
b
387
0.40
0
0
c
207
0.20
0
0
0.090
0.090
下列说法正确的是__________
A.该反应的正反应为放热反应
B.达到平衡时,容器a中的CH3OH体积分数比容器b中的小
C.容器a中反应到达平衡所需时间比容器c中的长
D.若起始时向容器a中充入CH3OH 0.15mol、CH3OCH30.15mol和H2O 0.10mol,则反应将向正反应方向进行
(3)合成气的组成n(H2)/n(CO+CO2)=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图所示。

①α(CO)值随温度升高而______________(填“增大”或“减小”),其原因是_________。
②图中P1、P2、P3的大小关系为___________,其判断理由是________________。
(4)甲醇可以制成燃料电池,与合成气制成燃料电池相比优点是:__________;若以硫酸作为电解质其负极反应为:_________。
高三化学填空题困难题查看答案及解析
-
利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO2(g)+3H2(
g)⇌CH3OH(g)+H2O(g) △H1=﹣58kJ.mol﹣
1,
②CO(g)+2H2(g)⇌CH3OH(g) △H2
③CO2(g)+H2(g)⇌CO(g)+H2O(g) △H3,
已知反应中一些相关物质的化学键键能数据如下:
化学键
C﹣O
C﹣H
H﹣H
H﹣O
C≡O
E/(kJ·mol﹣1)
343
413
436
465
1076
则△H2和△H3分别为
A.-99kJ·mol﹣1,+41kJ·mol﹣1
B.-99kJ·mol﹣1,-41kJ·mol﹣1
C.+99kJ·mol﹣1,-41kJ·mol﹣1
D.+99kJ·mol﹣1,+41kJ·mol﹣1
高三化学选择题简单题查看答案及解析
-
利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H1=﹣58kJ.mol﹣1,
②CO(g)+2H2(g)⇌CH3OH(g) △H2
③CO2(g)+H2(g)⇌CO(g)+H2O(g) △H3,
已知反应中一些相关物质的化学键键能数据如下:
化学键
C﹣O
C﹣H
H﹣H
H﹣O
C≡O
E/(kJ·mol﹣1)
343
413
436
465
1076
则△H2和△H3分别为
A.-99kJ·mol﹣1,+41kJ·mol﹣1
B.-99kJ·mol﹣1,-41kJ·mol﹣1
C.+99kJ·mol﹣1,-41kJ·mol﹣1
D.+99kJ·mol﹣1,+41kJ·mol﹣1
高三化学单选题中等难度题查看答案及解析