将0.2 mol·L-1的KOH溶液与0.1 mol·L-1的H2SO3溶液等体积混合后,溶液中各粒子浓度大小关系正确的是( )
A.c(K+)+c(H+)=c(OH-)+c()+c(
)
B.2c(K+)=c()+c(
)+c(H2SO3)
C.c(K+)>c()>c(
)>c(H2SO3)
D.c()+c(
)+c(H2SO3)=0.1 mol·L-1
高二化学单选题中等难度题
将0.2 mol·L-1的KOH溶液与0.1 mol·L-1的H2SO3溶液等体积混合后,溶液中各粒子浓度大小关系正确的是( )
A.c(K+)+c(H+)=c(OH-)+c()+c(
)
B.2c(K+)=c()+c(
)+c(H2SO3)
C.c(K+)>c()>c(
)>c(H2SO3)
D.c()+c(
)+c(H2SO3)=0.1 mol·L-1
高二化学单选题中等难度题
将0.2 mol·L-1的KOH溶液与0.1 mol·L-1的H2SO3溶液等体积混合后,溶液中各粒子浓度大小关系正确的是( )
A.c(K+)+c(H+)=c(OH-)+c()+c(
)
B.2c(K+)=c()+c(
)+c(H2SO3)
C.c(K+)>c()>c(
)>c(H2SO3)
D.c()+c(
)+c(H2SO3)=0.1 mol·L-1
高二化学单选题中等难度题查看答案及解析
将0.2 mol•L-1NaHCO3溶液与0.1 mol•L-1KOH溶液等体积混合,下列粒子浓度关系正确的是( )
A.c(K+)=c(HCO3-)+c(CO32-)+c(H2CO3)
B.c(Na+)>c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
C.c(OH-)+c(CO32-)=c(H+)+c(H2CO3)+0.1mol•L-1
D.3c(K+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
高二化学选择题困难题查看答案及解析
高二化学选择题中等难度题查看答案及解析
常温下的下列溶液中,微粒浓度关系正确的是
A. 0.2 mol/L NaHCO3溶液与0.1 mol/L KOH溶液等体积混合:3c(K+) + c(H+) = c(OH-) + c(HCO3-) + 2(CO32-)
B. 只含有NH4+、Cl-、H+、OH-的溶液中,其离子浓度可能是:c(Cl-) > c(NH4+) > c(OH-) > c(H+)
C. 0.1 mol/L的NaHA溶液,其pH=4,则其中离子浓度最大与最小的差值为(0.1-10-4) mol/L
D. c(NH4+)相等的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2溶液,则c[(NH4)2SO4] > c[(NH4)2CO3] > c[(NH4)2Fe(SO4)2]
高二化学单选题中等难度题查看答案及解析
下列各种溶液中,粒子物质的量浓度关系正确的是( )
A.0.1mol·L-1的NH4Cl溶液与0.1mol·L-1氨水等体积混合:
c(Cl-)> c(NH4+)>c(H+)>c(OH-)
B.0.2mol·L-1Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3)
C.0.1mol·L-1(NH4)2SO4溶液:c(SO42-)>c(NH4+)>c(H+)>c(OH-)
D.0.2mol·L-1NaHCO3溶液:c(H+)+c(Na+)=c(OH-)+c(HCO3-)+c(CO32-)
高二化学选择题简单题查看答案及解析
常温下,下列所述有关离子浓度之间的关系错误的是
A. 将0.2mol/L NaHCO3溶液与0.1mol/L KOH溶液等体积混合:3c(K+)+c(H+)=c(OH-) +c(HCO3-)+2c(CO32-)
B. 浓度均为0.1mol/L 的CH3COOH 与CH3COONa溶液等体积混合后pH=5,则混合溶液中:c(CH3COO-)-c(CH3COOH)=2×(10-5-10-9) mol/L
C. 将CO2通入0.1 mol/L Na2CO3溶液至中性,溶液中2c (CO32-) +c (HCO3-)=0.1mol/L
D. 0.1 mol/L Na2CO3溶液中存在:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
高二化学单选题中等难度题查看答案及解析
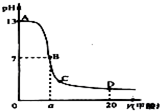
室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化)
| 实验编号 | 起始浓度/(mol·L-1) | 反应后溶 液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
下列判断不正确的是( )
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)= mol/L
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1 mol/L
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+)
高二化学选择题困难题查看答案及解析
室温下,将0.4mol/L一元酸HA溶液和0.2mol/LNaOH溶液等体积混合(忽略混合时溶液体积的变化),测得混合液的pH=5,则下列说法或粒子浓度关系式正确的是( )
A.混合液中由水电离出的c(H+)=1×10-8mol/L
B.c(A-)+c(HA)=2c(Na+)=0.4mol/L
C.HA溶液中与混合液中
相等
D.c(A-)-c(HA)=2c(OH-)-2c(H+)
高二化学选择题困难题查看答案及解析
常温下,下列关于粒子浓度大小比较正确的是( )
A. 0.1mol/L的HF溶液和0.1mol/L的NaOH溶液等体积混合:c(Na+)+c(OH-)>c(H+)+c(F-)
B. 向0.10mol/LNaHSO3溶液中通入NH3至溶液pH=7 (体积变化可忽略):c(Na+)>c(NH4+)>c(SO32-)
C. 0.3mol的SO2通入1L0.4mol/L的NaOH溶液中:4c(Na+)=3c(HSO3-)+3c(SO32-)+3c(H2SO3)
D. pH=4的CH3COOH溶液和pH=10的KOH溶液等体积混合:2c(K+)+c(H+)= c(OH-)+ c(CH3COOH)+ 2c(CH3COO-)
高二化学选择题困难题查看答案及解析
下列溶液中粒子的物质的量浓度关系正确的是( )
A. 0.1 mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)
B. 20 mL 0.1 mol/L CH3COONa溶液与10 mL 0.1 mol/L HCl溶液混合后溶液呈酸性,所得溶液中c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)
C. 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-)
D. 0.1 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH)
高二化学单选题困难题查看答案及解析