-
铬镍基合金的性质稳定,抗高温燃气腐蚀能力强,广泛应用于舰船和工业的燃气轮机。某种铬镍基合金由Fe、Cr、Ni、C四种元素组成。
(1)Fe、Cr、Ni的基态原子核外电子占据的最高能层为________(填符号)。
(2)基态Cr原子价层电子的电子排布式为________,与Cr同周期且基态原子最外层电子数相同的元素,位于周期表的________区。
(3)Fe3+与SCN-反应生成红色的K3Fe(SCN)6,K3Fe(SCN)6内部的作用力有________。写出一种与SCN-互为等电子体的分子的化学式________。
(4)已知FeO、NiO的晶体结构均为NaCl型,且NiO的熔点高于FeO,其理由是________。
(5)由于晶体缺陷,Ni的某种氧化物的化学式为Ni0.88O,则该晶体中Ni2+和Ni3+最简整数比为________。
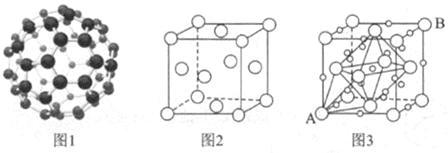
(6)C60分子结构及其晶胞结构如图1和图2所示。若在C60晶体的空隙中插入K+,该晶体在一定条件下具有超导能力,其结构如图3所示。

①C60分子中碳原子的杂化方式为________。
②该超导体晶胞中,K+填充在由C60围成的________空隙和________空隙中。
③若晶胞中A的坐标参数为(0,0,0),B的坐标为(1,1,1),则与A距离最近的K+的坐标参数为________。
-
铬镍基合金的性质稳定,抗高温燃气腐蚀能力强,广泛应用于舰船和工业的燃气轮机。某种铬镍基合金由Fe、Cr、Ni、C四种元素组成。
(1)Fe、Cr、Ni的基态原子核外电子占据的最高能层为________ 填符号
填符号 。
。
(2)基态Cr原子价层电子的电子排布式为________,与Cr同周期且基态原子最外层电子数相同的元素,位于周期表的________区。
(3)Fe3+与SCN-反应生成红色的K3Fe(SCN)6,K3Fe(SCN)6内部的作用力有________。写出一种与SCN-互为等电子体的分子的化学式________。
(4)已知FeO、NiO的晶体结构均为NaCl型,且NiO的熔点高于FeO,其理由是________。
(5)C60分子结构及其晶胞结构如图1和图2所示。若在C60晶体的空隙中插入K+,该晶体在一定条件下具有超导能力,其结构如图3所示。
①C60分子中碳原子的杂化方式为________。
②该超导体晶胞中,K+填充在由C60围成的________空隙和________空隙中。
③若晶胞中A的坐标参数为(0,0,0),B的坐标参数为(1,1,1),则与A距离最近的K+的坐标参数为________。
-
化学与生产、生活密切相关,下列有关说法中正确的是
A. 使用含钙离子浓度较大的地下水洗衣服,肥皂去污能力减弱
B. 铝及其合金广泛应用,是因为铝的性质稳定,不易被腐蚀
C. 塑料的老化是因为其主要成分在空气中发生了缓慢的加成反应
D. 硅太阳能电池利用的是原电池原理
-
化学在生活中有着广泛的应用,下列物质性质与应用对应关系错误的是
A. 硅胶吸水能力强,可作食品干燥剂
B. CaO能与SO2反应,可作工业废气脱硫剂
C. 聚四氟乙烯耐高温、耐腐蚀、不粘附、无毒害,可用于厨具表面涂层
D. Na2S具有还原性,可作废水中Cu2+和Hg2+的沉淀剂
-
建造舰船需要大量的新型材料,舰船的甲板也要耐高温且外壳要耐腐蚀,而镍铬铁合金就是具有高强度、耐高温、耐腐蚀等优良性能的特种钢,这类特种钢中含有碳、硅、氧、氮、磷等元素。
(1)保铬钢抗腐蚀性能强, 基态原子的价电子排布_________,为铬元素在周期表中_________区。
基态原子的价电子排布_________,为铬元素在周期表中_________区。
(2) 能形成多种配离子,如
能形成多种配离子,如 、
、 和
和 等,
等, 中心原子的配位数是_________,与
中心原子的配位数是_________,与 互为等电子体的分子为_________。
互为等电子体的分子为_________。
(3)舰船甲板涂有一层耐高温的材料聚硅氧烷结构如图所示,其中 原子杂化方式为________杂化。
原子杂化方式为________杂化。

(4)碳和硅可化合成碳化硅, 晶体具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的,但是碳化硅的熔点低于金刚石,原因是_________。
晶体具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的,但是碳化硅的熔点低于金刚石,原因是_________。
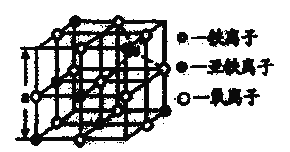
(5)铁的氧化物之一是 ,从
,从 中取出的能体现其晶体结构的一个立方体,则晶体中的离子是否构成了面心立方最密堆积?________(填“是”或“否”);该立方体是不是
中取出的能体现其晶体结构的一个立方体,则晶体中的离子是否构成了面心立方最密堆积?________(填“是”或“否”);该立方体是不是 的晶胞?_________(填“是”或“否”);立方体中铁离子处于氧离子围成的_________(填空间结构)空隙;根据上图计算
的晶胞?_________(填“是”或“否”);立方体中铁离子处于氧离子围成的_________(填空间结构)空隙;根据上图计算 晶体的密度为_________
晶体的密度为_________ 。(图
。(图 ,计算结果保留两位有效数字)
,计算结果保留两位有效数字)
-
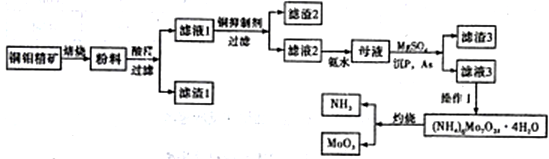
钼是一种稀有金属,为人体及动植物必须的微量元素,纯金属钼和钼合金具有强度大、耐高温、耐磨损、耐腐蚀等多种有点,广泛应用于冶金、机械、化工、军工、电光源、润滑剂、航空航天等领域。某化学兴趣小组在实验室模拟了从铜钼精矿(主要含有Cu2S、MoS2,SiO2,P,As等)中提取分离得到氧化钼的过程:
已知:MoO3在869.9K温度下开始升华,而到969.9温度下激烈升华,在溶液中以H2MoO4形式存在
(1)滤渣1的主要成分为_________________________。
(2)铜钼矿中的钼元素在过量的空气中,于一定温度下,很容易氧化成MoO3,其方程式为___________________________________,
焙烧过程中应控制在800-870K左右,其原因为____________________________。
(3)①向滤液1中加入的铜抑制剂有多种,如氰化钠,向含重金属离子的溶液中添加氰化钠,会立即生成沉淀,但是若继续添加氰化钠,沉淀继续与CN-反应,生成[Me(CN)4]2-稳定的配离子,因此需要控制氰化钠的用量,试写出向滤液中加入过量氰化钠的离子方程式_______________________________;
②由干氰化钠有剧毒,所以需要对剩余的氰化钠进行处理,通常选用深漂白粉或漂白液在酸性条件下将其氧化为两种空气中常见无毒气体,试写出漂白液与氰化钠反应的离子方程式_____;
③除氰化钠外,常用的抑制剂还有亚铁氰化钠,Na4[Fe(CN)6]可与重金属阳离子反应,生成溶度积较小的沉淀,已知Cu2Fe(CN)6的Ksp=1.00×10-16;滤液中的Cu2+的浓度为为0.5mol/L、.当溶液中离子浓度小于等于1.00×10-16mol/L时可认为沉淀完全,则欲处理IL滤液的Na4[Fe(CN)6]体积为_________(体积变化忽略不计,保留两位小数)。
(4)当NH3∶MoO3等于或稍大于6∶7时,可从氨溶液中结晶出分子式为(NH4)6Mo7O24• 4H2O的盐。蒸发溶液(把氨除去)或中和溶液(化合部分氨)都可以达到这一比例。则操作I为_______。
-
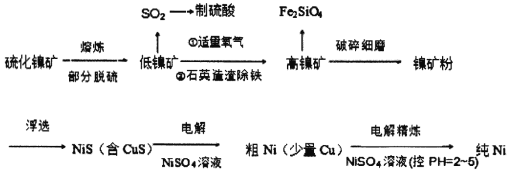
元素周期表中的28号元素Ni有重要的用途,它有良好的耐高温、耐腐蚀、防锈功能,在电池、催化剂方面也有广泛应用。工业上以硫化镍矿(含少量杂质硫化铜、硫化亚铁)为原料制备并精制镍的基本流程如下:
已知:电极电位(E)能体现微粒的氧化还原能力强弱,如:
H2-2e-=2H+ E=0.00V Cu-2e-=Cu2+ E=0.34V
Fe-2e-=Fe2+ E=-0.44V Ni-2e-=Ni2+ E=-0.25V
(1)镍在周期表中的位置为_______________________________。
(2)高镍矿破碎细磨的作用______________________________________。
(3)焰色反应实验可以用光洁无锈的镍丝代替铂丝蘸取化学试剂灼烧,原因是______________________。
(4)造渣除铁时发生的化学反应方程式___________________________________(产物以氧化形式表示)。
(5)电解制粗镍时阳极发生的主要电极反应式_____________________________________。
(6)工业上由NiSO4溶液制得Ni(OH)2后,再滴加NaC1O溶液,滴加过程中发生反应的离子方程式为_________________________________________________________。
(7)电解精炼镍的过程需控制pH为2~5,试分析原因______________________________,阳极泥的成分为________________(写名称)。
-
元素周期表中的28号元素Ni有重要的用途,它有良好的耐高温、耐腐蚀、防锈功能,在电池、催化剂方面也有广泛应用。工业上以硫化镍矿(含少量杂质硫化铜、硫化亚铁)为原料制备并精制镍的基本流程如下:
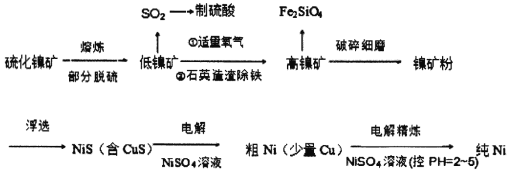
已知:电极电位(E)能体现微粒的氧化还原能力强弱,如:
H2-2e-=2H+ E=0.00V Cu-2e-=Cu2+ E=0.34V
Fe-2e-=Fe2+ E=-0.44V Ni-2e-=Ni2+ E=-0.25V
(1)镍在周期表中的位置为_______________________________。
(2)高镍矿破碎细磨的作用______________________________________。
(3)焰色反应实验可以用光洁无锈的镍丝代替铂丝蘸取化学试剂灼烧,原因是______________________。
(4)造渣除铁时发生的化学反应方程式___________________________________(产物以氧化形式表示)。
(5)电解制粗镍时阳极发生的主要电极反应式_____________________________________。
(6)工业上由NiSO4溶液制得Ni(OH)2后,再滴加NaC1O溶液,滴加过程中发生反应的离子方程式为_________________________________________________________。
(7)电解精炼镍的过程需控制pH为2~5,试分析原因______________________________,阳极泥的成分为________________(写名称)。
-
下列对应关系正确的是
| 化学性质 | 实际应用 |
| A | 钠钾的合金具有强还原性 | 用于原子反应堆的导热剂 |
| B | FeCl3能水解生成Fe(OH)3 | 用于脱除燃气中的H2S |
| C | MnO2其有催化作用 | 用作干电池正极的话性物质 |
| D | N2H4常温下能与O2反应 | 用于脱除高压锅炉水中的O2 |
A. A B. B C. C D. D
-
钴基合金中含少量镁、镍和铁元素,在化工、航空航天和机械工业应用广泛。现有钴基废合金需要回收再利用,设计流程如图:
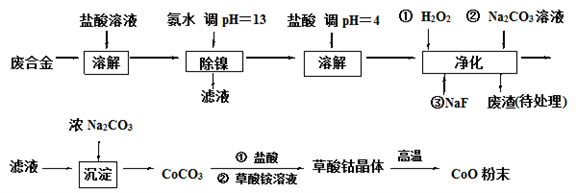
已知:1)有关钴、镍、镁、铁化合物的性质见下表:
| 化学式 | 沉淀开始时的pH | 沉淀完全时的pH | 有关性质 |
| Co(OH)2 | 7.2 | 9.4 | Co+2HCl=CoCl2+H2↑ Co2++2NH3·H2O=Co(OH)2↓+2NH4+ Co2++2H2O Co(OH)2+2H+ Co(OH)2+2H+ Ni+2HCl=NiCl2+H2↑ Ni2++6NH3·H2O=[Ni(NH3)6]2++6H2O |
| Fe(OH)2 | 7.1 | 9.6 |
| Fe(OH)3 | 2.3 | 3.7 |
| Mg(OH)2 | 10.8 | 12.4 |
2)25℃ Ksp(MgF2)=7.4×10—11、Ksp(MgCO3)=3.5×10—3
请回答:
(1)“除镍”步骤必须控制在一定时间内完成,否则沉淀中将有部分Co(OH)2转化为Co(OH)3,此反应的化学方程式为________________。
(2)在“盐酸调pH=4”步骤中,加入盐酸的作用是______________________。
(3)“净化”步骤中加入H2O2的作用是_____________________(请用离子方程式表示)。废渣的成分___________________(请用化学式表示)。
(4)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O Fe(OH)3+3H+的平衡常数K=_________________________。
Fe(OH)3+3H+的平衡常数K=_________________________。
(5)二水合草酸钴晶体(CoC2O4·2H2O)中C元素的化合价为________,在空气中高温反应的化学方程式为_______________________。
填符号
。







