如图是工业利用菱镁矿(主要含MgCO3,还含有Al2O3、FeCO3杂质)制取氯化镁的工艺流程。
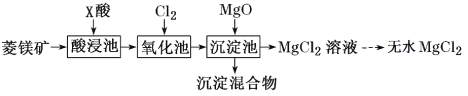
下列说法不正确的是( )
A.酸浸池中加入的X酸是硝酸
B.氧化池中通入氯气的目的是将Fe2+氧化为Fe3+
C.沉淀混合物为Fe(OH)3和Al(OH)3
D.在工业上常利用电解熔融氯化镁的方法制取金属镁
高三化学单选题中等难度题
如图是工业利用菱镁矿(主要含MgCO3,还含有Al2O3、FeCO3杂质)制取氯化镁的工艺流程。

下列说法不正确的是( )
A.酸浸池中加入的X酸是硝酸
B.氧化池中通入氯气的目的是将Fe2+氧化为Fe3+
C.沉淀混合物为Fe(OH)3和Al(OH)3
D.在工业上常利用电解熔融氯化镁的方法制取金属镁
高三化学单选题中等难度题
如图是工业利用菱镁矿(主要含MgCO3,还含有Al2O3、FeCO3杂质)制取氯化镁的工艺流程。

下列说法不正确的是( )
A.酸浸池中加入的X酸是硝酸
B.氧化池中通入氯气的目的是将Fe2+氧化为Fe3+
C.沉淀混合物为Fe(OH)3和Al(OH)3
D.在工业上常利用电解熔融氯化镁的方法制取金属镁
高三化学单选题中等难度题查看答案及解析
镁及其化合物有广泛用途.工业上以菱镁矿(主要成分为MgCO3,含SiO2以及少量FeCO3等杂质)为原料制备纳米氧化镁的实验流程如下
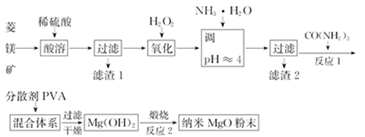
回答下列问题:
(1)滤渣1为____________(填化学式),CO(NH2)2的电子式为______。
(2)在实验室煅烧滤渣2制得的金属氧化物为______(填化学式),需要的仪器除酒精灯、三脚架以外,还需要______(填名称)。
(3)在一定条件下CO(NH2)2可与H2O反应生成CO2和一种弱碱,反应的化学方程式为__________。
(4)室温时,加入CO(NH2)2,产生沉淀。当 Mg2+沉淀完全时,溶液中的c(OH-)=_______(离子浓度小于1.0×10-5 mol•L-1时,即可认为该离子沉淀完全;室温时,Ksp[Mg(OH)2]=1.96×10-11)
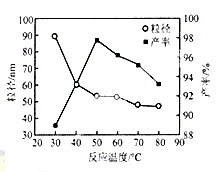
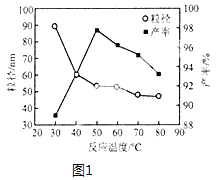
(5)工业上还可用氯化镁和碳酸铵为原料,采用直接沉淀法制务纳米MgO。如图为反应温度对纳米MgO产率和粒径的影响,据图分析反应的最佳温度为__________。
高三化学简答题困难题查看答案及解析
镁及其化合物有广泛用途。工业上以菱镁矿(主要成分为MgCO3,含SiO2以及少量FeCO3等杂质)为原料制备纳米氧化镁的实验流程如下:
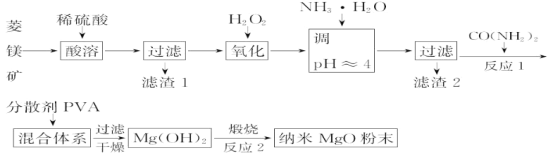
(1)加入H2O2氧化时,发生反应的离子方程式为___。
(2)在实验室煅烧滤渣2制得的金属氧化物为___(填化学式),需要的仪器除酒精灯、三脚架以外,还需要___(填序号)。
①蒸发皿 ②坩埚 ③泥三角 ④石棉网
(3)在一定条件下CO(NH2)2可与H2O反应生成CO2和一种弱碱,反应的化学方程式为___。
(4)25℃时,加入CO(NH2)2至开始产生沉淀,溶液的pH=10时,c(Mg2+)=___mol⋅L-1(已知25℃,Ksp[Mg(OH)2]=1.8×10-11)。
(5)工业上还可用氯化镁和碳酸铵为原料,采用直接沉淀法制备纳米MgO。如图1为反应温度对纳米MgO产率和粒径的影响,据图分析反应的最佳温度为___。
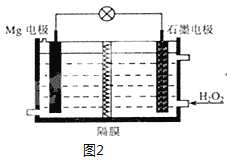
(6)Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图2如。该电池工作时,石墨电极发生的电极反应为___。
高三化学工业流程中等难度题查看答案及解析
如图是工业制取菱镁矿MgCO3(含杂质Al2O3、FeCO3)制取镁的工艺流程
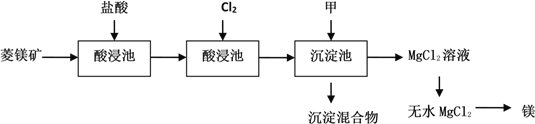
请回答有关问题:
(1)菱镁矿进入酸浸池前需要粉碎,目的是 __________________________。
(2)氧化池通入Cl2的目的是氧化 _________________________(填化学式),工业上不选用硝酸做氧化剂的原因是_________________和_________________________。
(3)物质甲可以是_____________
A、MgO B、Mg(OH)2 C、NaOH溶液 D、稀氨水
(4)由MgCl2溶液制取无水MgCl2的操作方法 __________________________。
(5)当Fe3+完全沉淀时,求最小pH__________。已知:氢氧化铁ksp=1.0×10-38,离子浓度小于1×10-5 mol/L认为沉淀完全
高三化学简答题困难题查看答案及解析
如图是工业制取菱镁矿MgCO3(含杂质Al2O3、FeCO3)制取镁的工艺流程
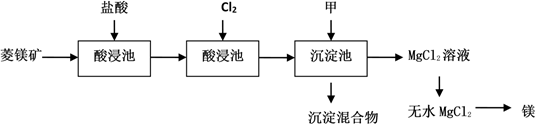
请回答有关问题:
(1)菱镁矿进入酸浸池前需要粉碎,目的是 __________________________。
(2)氧化池通入Cl2的目的是氧化 _________________________(填化学式),工业上不选用硝酸做氧化剂的原因是_________________和_________________________。
(3)物质甲可以是_____________
A、MgO B、Mg(OH)2 C、NaOH溶液 D、稀氨水
(4)由MgCl2溶液制取无水MgCl2的操作方法 __________________________。
(5)当Fe3+完全沉淀时,求最小pH__________。已知:氢氧化铁ksp=1.0×10-38,离子浓度小于1×10-5 mol/L认为沉淀完全
高三化学简答题困难题查看答案及解析
镁及其化合物有着广泛用途。工业上以菱镁矿(主要成分为MgCO3,含SiO2以及少量FeCO3等杂质)为原料制备纳米氧化镁的实验流程如下:
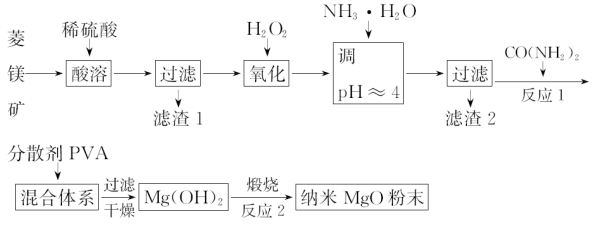
(1)滤渣1为______________________。
(2)加入H2O2氧化时,发生反应的离子方程式为______________________。
(3)在实验室煅烧滤渣2制得的金属氧化物为____________(填化学式),需要的仪器除酒精灯、三脚架、泥三角以外,还需要______________(填名称)。
(4)在一定条件下CO(NH2)2可与H2O反应生成CO2和一种弱碱,该反应中反应物的质量之比为________。
(5)25℃时,加入CO(NH2)2至开始产生沉淀,当Mg2+全部沉淀时溶液的c(OH-)=__________(已知25℃,Ksp[Mg(OH)2]=1.96×10-11)。
(6)工业上还可用氯化镁和碳酸铵为原料,采用直接沉淀法制备 纳米MgO。取少量制得的该物质溶于某种液体溶剂中(两者不反应),能说明是纳米MgO存在的简单方法是____________。如图为反应温度对纳米MgO产率和粒径的影响,据图分析反应的最佳温度为____________。
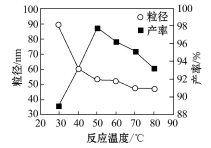
高三化学实验题极难题查看答案及解析
六氨氯化镁(MgCl2·6NH3)具有极好的可逆吸、放氨特性,是一种优良的储氨材料。某研究小组在实验室以菱镁矿(主要成分MgCO3,含少量FeCO3等杂质)为原料制备氨氯化镁,实验流程图如下
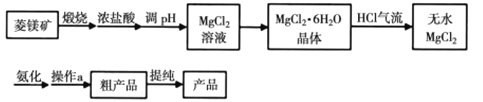
其中氨化过程装置示意图如下:
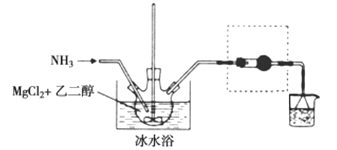
已知:①与Mg2+结合能力:H2O>NH3>HOCH2CH2OH>CH2OH②相关物质的性质见下表
| NH3的溶解性 | MgCl2的溶解性 | MgCl2·6NH3的溶解性 | |
| 水 | 易溶 | 易溶 | 易溶 |
| 甲醇(沸点65℃) | 易溶 | 易溶 | 难溶 |
| 乙二醇(沸点197℃) | 易溶 | 易溶 | 难溶 |
(1)调pH适合的物质是___________(填化学式)。
(2)在空气中直接加热MgCl2·6H2O晶体得不到纯的无水MgCl2,原因是___________(用化学方程式表示)。
(3)虚框内装置的作用是___________,操作a的名称是___________。
(4)提纯操作中,下列洗涤剂最合适的是___________。
A.冰浓氨水 B.乙二醇和水的混合液
C.氨气饱和的甲醇溶液 D.氨气饱和的乙二醇溶液
(5)制得产品后,该科研小组对产品的成分进行测定,其中氯离子含量检测方法如下:
a.称取1.420g样品,加足量硫酸溶解,配制成250mL溶液;
b.量取25.00mL待测液于锥形瓶中;
c.用0.2000mol· L-1 AgNO3标准溶液滴定至终点,记录消耗AgNO3标准溶液的体积;
d.重复b、e操作2~3次,平均消耗AgNO3标准溶液10.00mL
①配制样品溶液时加硫酸的目的是___________。
②该样品中氯离子百分含量为___________。
③将氯离子百分含量实验值与理论值(36.04%)相比较,请分析造成此结果的可能原因有___________(已知滴定操作正确、硫酸根离子对检测无影响)
高三化学实验题困难题查看答案及解析
(15分)氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下:

(1)MgCO3与稀硫酸反应的离子方程式为 。
(2)加入H2O2氧化时,发生反应的化学方程式为 。
(3)滤渣2的成分是 (填化学式)。
(4)煅烧过程存在以下反应:
2MgSO4+C2MgO+2SO2↑+CO2↑ MgSO4+C
MgO+SO2↑+CO↑
MgSO4+ 3CMgO+S↑+3CO↑
利用右图装置对煅烧产生的气体进行分步吸收或收集。
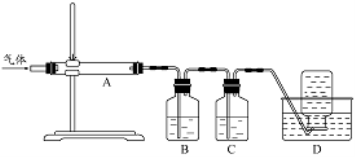
①D中收集的气体可以是 (填化学式)。
②B中盛放的溶液可以是 (填字母)。
A.NaOH溶液 B.Na2CO3溶液 C.稀硝酸 D.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中硫元素最高价态为+4,写出该反应的离子方程式: 。
高三化学填空题困难题查看答案及解析
由菱镁矿(主要成分为MgCO3、CaCO3、FeCO3、SiO2)制备高纯Mg(OH)2的一种工艺如下:
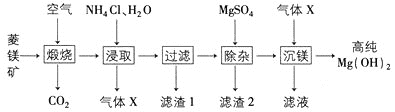
下列说法不正确的是
A.“煅烧”时FeCO3发生反应为4FeCO3+O22Fe2O3+4CO2
B.“浸取”产生的气体X为NH3
C.“滤渣1”“滤渣2”分别为SiO2、CaSO4
D.“沉镁”所得的固体是否洗涤干净可用BaCl2溶液检验
高三化学单选题中等难度题查看答案及解析
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
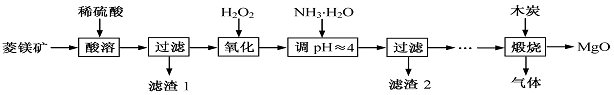 (1)MgCO3与稀硫酸反应的离子方程式为。
(1)MgCO3与稀硫酸反应的离子方程式为。
(2)加入H2O2氧化时,发生反应的化学方程式为。(3)滤渣2的成分是 (填化学式)。
(4)煅烧过程存在以下反应:2MgSO4+C2MgO+2SO2↑+CO2↑、MgSO4+C
MgO+SO2↑+CO↑、 MgSO4+3C
MgO+S↑+3CO↑。
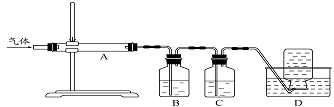
利用上图装置对煅烧产生的气体进行分步吸收或收集。
①D中收集的气体是________(填化学式)。
②B中盛放的溶液可以是(填字母)。
a.NaOH 溶液 b.Na2CO3溶液 c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:。
高三化学填空题极难题查看答案及解析