室温下,将0.1000 mol·L-1盐酸滴入20.00 mL 0.100 0mol·L-1的某一元碱MOH溶液中,溶液的pH随加入盐酸体积变化曲线如下图所示。下列有关说法不正确的是( )
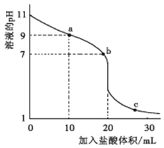
A.该一元碱的电离方程式为MOH = M++OH-
B.a、b、c三点中,b点水的电离程度最大
C.室温下,MOH的电离常数Kb=1×10-5 mol·L-1
D.b点:c (M+)=c (Clˉ)
高二化学单选题中等难度题
室温下,将0.1000 mol·L-1盐酸滴入20.00 mL 0.100 0mol·L-1的某一元碱MOH溶液中,溶液的pH随加入盐酸体积变化曲线如下图所示。下列有关说法不正确的是( )

A.该一元碱的电离方程式为MOH = M++OH-
B.a、b、c三点中,b点水的电离程度最大
C.室温下,MOH的电离常数Kb=1×10-5 mol·L-1
D.b点:c (M+)=c (Clˉ)
高二化学单选题中等难度题
室温下,将0.1000 mol·L-1盐酸滴入20.00 mL 0.100 0mol·L-1的某一元碱MOH溶液中,溶液的pH随加入盐酸体积变化曲线如下图所示。下列有关说法不正确的是( )

A.该一元碱的电离方程式为MOH = M++OH-
B.a、b、c三点中,b点水的电离程度最大
C.室温下,MOH的电离常数Kb=1×10-5 mol·L-1
D.b点:c (M+)=c (Clˉ)
高二化学单选题中等难度题查看答案及解析
室温下,将0.1000 mol·L-1盐酸滴入20.00 mL未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如图所示,下列说法正确的是
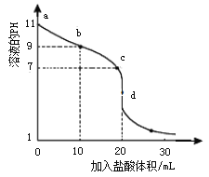
A. b点处的溶液中c(Cl-)>c(M+)>c(OH-)>c(H+)
B. 室温下,MOH的电离平衡常数Kb为1×10-5
C. c点处的溶液中c(M+)=c(Cl-)=c(H+)=c(OH-)
D. d点处的溶液中c(MOH) + c(H+) = c(OH-)
高二化学单选题中等难度题查看答案及解析
常温下,用0.1000mol·L-1盐酸滴定20.00mL未知浓度一元弱碱MOH溶液,滴定曲线如图所示。下列有关说法错误的是( )
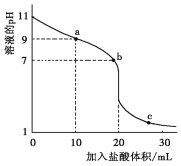
A.该一元碱溶液浓度为0.1000mol·L-1
B.a、b、c点水的电离程度逐渐增大
C.b点:c(M+)=c(Cl-)
D.常温下,MOH的电离常数Kb=1×10-5
高二化学单选题中等难度题查看答案及解析
室温下,用0.100mol/L NaOH溶液分别滴定20.00ml 0.100 mol/L 的盐酸和醋酸,滴定曲线如图所示,下列说法不正确的是( )
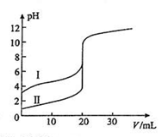
A.Ⅱ表示的是滴定盐酸的曲线
B.pH=7时,滴定盐酸消耗V(NaOH)大于滴定醋酸消耗V(NaOH)
C.V(NaOH)=20ml时,c(Cl-)=c(CH3COO-)
D.V(NaOH)=10ml时,醋酸溶液中:
c(CH3COO- )>c(Na+ )> c(H+ )> c(OH−)
高二化学选择题中等难度题查看答案及解析
室温下,某一元弱酸HA的电离常数K=1.6×10-6。 向20.00 mL 浓度约为0.1 mol·L-1 HA溶液中逐滴加入0.1000 mol·L-1 的标准NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:(已知lg4=0.6)
(1)a点溶液中pH约为________,此时溶液中H2O电离出的c(H+)为________。
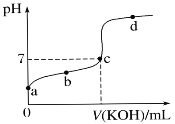
(2)a、b、c、d四点中水的电离程度最大的是________点,滴定过程中宜选用__________作指示剂,滴定终点在________(填“c点以上”或“c点以下”)。
(3)滴定过程中部分操作如下,下列各操作使测量结果偏高的是_________________(填字母序号)。
A.滴定前碱式滴定管未用标准NaOH溶液润洗
B.用蒸馏水洗净锥形瓶后,立即装入HA溶液后进行滴定
C.滴定过程中,溶液出现变色后,立即停止滴定
D.滴定结束后,仰视液面,读取NaOH溶液体积
(4)若重复三次滴定实验的数据如下表所示,计算滴定所测HA溶液的物质的量浓度为_____mol/L。
| 实验序号 | NaOH溶液体积/mL | 待测HA溶液体积/mL |
| 1 | 21.01 | 20.00 |
| 2 | 20.99 | 20.00 |
| 3 | 21.60 | 20.00 |
高二化学综合题中等难度题查看答案及解析
室温下,用0.100 mol·L-1NaOH溶液分别滴定20.00 mL 0.100 mol·L-1的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )
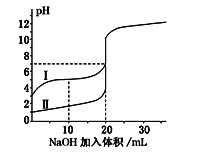
A. Ⅰ表示的是滴定盐酸的曲线
B. pH=7时,滴定醋酸消耗的V(NaOH)小于20mL
C. V(NaOH)=20mL时,两份溶液中c(Cl-)=c(CH3COO-)
D. V(NaOH)=10mL时,醋酸溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
高二化学单选题中等难度题查看答案及解析
室温下,用0.100 mol·L-1NaOH溶液分别滴定20.00 mL 0.100 mol·L-1的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )
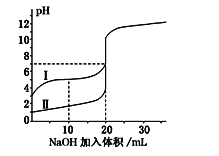
A. Ⅰ表示的是滴定盐酸的曲线
B. pH=7时,滴定醋酸消耗的V(NaOH)小于20mL
C. V(NaOH)=20mL时,两份溶液中c(Cl-)=c(CH3COO-)
D. V(NaOH)=10mL时,醋酸溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
高二化学单选题中等难度题查看答案及解析
室温下,用0.100 mol·L-1NaOH溶液分别滴定20.00 mL 0.100 mol·L-1的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )
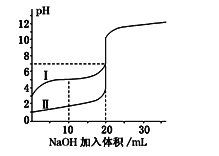
A. Ⅰ表示的是滴定盐酸的曲线
B. pH=7时,滴定醋酸消耗的V(NaOH)小于20mL
C. V(NaOH)=20mL时,两份溶液中c(Cl-)=c(CH3COO-)
D. V(NaOH)=10mL时,醋酸溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
高二化学null中等难度题查看答案及解析
室温下,用0.100 mol·L-1 NaOH溶液分别滴定20.00 mL 0.100 mol·L-1 的盐酸和醋酸,如图所示。
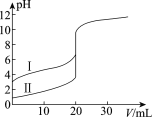
(1)表示滴定盐酸的曲线是________。(填I或II)
(2)当醋酸中滴入10 mL NaOH溶液时,溶液中含有的溶质有:________;溶液中离子浓度由大到小顺序为:________。
(3)当醋酸中滴入20 mL NaOH溶液时,将所得溶液加热,溶液pH随温度变化如图所示。下列说法正确的是________。(填序号)
a. 加热促进水的电离和醋酸钠水解
b. 加热使溶液碱性减弱
c. 加热使溶液中c(H+)/c(OH-)比值减小

高二化学综合题中等难度题查看答案及解析
室温下,用0.100mol/L NaOH溶液分别滴定20.00ml 0.100mol/L 的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是( )
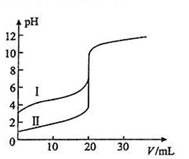
A、Ⅰ表示的是滴定盐酸的曲线
B、PH=7时,滴定醋酸消耗V(NaOH)小于20ml
C、V(NaOH) =20ml时,C(Cl— )== C(CH3COO— )
D、V(NaOH) =10ml时,醋酸溶液中:C(Na+ )> C(CH3COO— )> C(H+ )> C(OH— )
高二化学选择题困难题查看答案及解析