室温下,将0.1000 mol·L-1盐酸滴入20.00 mL未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如图所示,下列说法正确的是
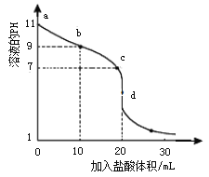
A. b点处的溶液中c(Cl-)>c(M+)>c(OH-)>c(H+)
B. 室温下,MOH的电离平衡常数Kb为1×10-5
C. c点处的溶液中c(M+)=c(Cl-)=c(H+)=c(OH-)
D. d点处的溶液中c(MOH) + c(H+) = c(OH-)
高二化学单选题中等难度题
室温下,将0.1000 mol·L-1盐酸滴入20.00 mL未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如图所示,下列说法正确的是

A. b点处的溶液中c(Cl-)>c(M+)>c(OH-)>c(H+)
B. 室温下,MOH的电离平衡常数Kb为1×10-5
C. c点处的溶液中c(M+)=c(Cl-)=c(H+)=c(OH-)
D. d点处的溶液中c(MOH) + c(H+) = c(OH-)
高二化学单选题中等难度题
室温下,将0.1000 mol·L-1盐酸滴入20.00 mL未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如图所示,下列说法正确的是

A. b点处的溶液中c(Cl-)>c(M+)>c(OH-)>c(H+)
B. 室温下,MOH的电离平衡常数Kb为1×10-5
C. c点处的溶液中c(M+)=c(Cl-)=c(H+)=c(OH-)
D. d点处的溶液中c(MOH) + c(H+) = c(OH-)
高二化学单选题中等难度题查看答案及解析
室温下,将0.1000 mol·L-1盐酸滴入20.00 mL 0.100 0mol·L-1的某一元碱MOH溶液中,溶液的pH随加入盐酸体积变化曲线如下图所示。下列有关说法不正确的是( )
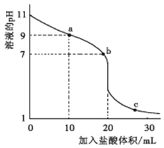
A.该一元碱的电离方程式为MOH = M++OH-
B.a、b、c三点中,b点水的电离程度最大
C.室温下,MOH的电离常数Kb=1×10-5 mol·L-1
D.b点:c (M+)=c (Clˉ)
高二化学单选题中等难度题查看答案及解析
常温下,用0.1000mol·L-1盐酸滴定20.00mL未知浓度一元弱碱MOH溶液,滴定曲线如图所示。下列有关说法错误的是( )
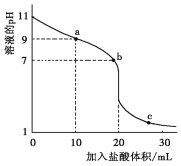
A.该一元碱溶液浓度为0.1000mol·L-1
B.a、b、c点水的电离程度逐渐增大
C.b点:c(M+)=c(Cl-)
D.常温下,MOH的电离常数Kb=1×10-5
高二化学单选题中等难度题查看答案及解析
室温下,将0.100 0 mol·L-1盐酸滴入20.00 mL 未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体 积变化曲线如图所示。下列有关说法不正确的是( )
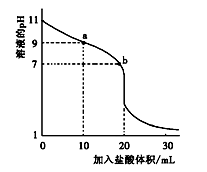
A.b点:c(M+)+c(MOH)=c(Clˉ)
B.a到b点的水溶液导电性依次增强
C.该一元碱溶液浓度为0.100 0 mol·L-1
D.室温下,MOH的电离常数Kb=1×10-5
高二化学选择题中等难度题查看答案及解析
室温下,某一元弱酸HA的电离常数K=1.6×10-6。 向20.00 mL 浓度约为0.1 mol·L-1 HA溶液中逐滴加入0.1000 mol·L-1 的标准NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:(已知lg4=0.6)
(1)a点溶液中pH约为________,此时溶液中H2O电离出的c(H+)为________。
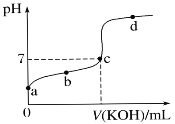
(2)a、b、c、d四点中水的电离程度最大的是________点,滴定过程中宜选用__________作指示剂,滴定终点在________(填“c点以上”或“c点以下”)。
(3)滴定过程中部分操作如下,下列各操作使测量结果偏高的是_________________(填字母序号)。
A.滴定前碱式滴定管未用标准NaOH溶液润洗
B.用蒸馏水洗净锥形瓶后,立即装入HA溶液后进行滴定
C.滴定过程中,溶液出现变色后,立即停止滴定
D.滴定结束后,仰视液面,读取NaOH溶液体积
(4)若重复三次滴定实验的数据如下表所示,计算滴定所测HA溶液的物质的量浓度为_____mol/L。
| 实验序号 | NaOH溶液体积/mL | 待测HA溶液体积/mL |
| 1 | 21.01 | 20.00 |
| 2 | 20.99 | 20.00 |
| 3 | 21.60 | 20.00 |
高二化学综合题中等难度题查看答案及解析
室温下,用0.1000 mol·L-1NaOH溶液滴定20.00 mL未知浓度的盐酸(酚酞作指示剂)的滴定曲线如图所示。下列说法正确的是( )
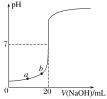
A.溶液中的氢离子浓度:a<b
B.盐酸的物质的量浓度为0.0100mol·L-1
C.指示剂变色时,说明盐酸与NaOH恰好完全反应
D.当滴加NaOH溶液10.00mL时(忽略反应前后体积变化),该混合液的pH=1+lg3
高二化学单选题中等难度题查看答案及解析
(12分)某学生用0.1000 mol·L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
A.取20.00 mL待测盐酸溶液注入洁净的锥形瓶中,并加入2-3滴酚酞试液
B.用标准氢氧化钠溶液润洗滴定管2-3次
C.把盛有标准氢氧化钠溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准氢氧化钠溶液注入碱式滴定管至“0”刻度以上2-3mL处
E.调节液面至“0”或“0”刻度以下,记下读数,为3.10mL
F.把锥形瓶放在滴定管下面,用标准NaOH溶液滴定至终点并记下滴定管的读数。
回答下列问题:
(1)正确的操作顺序是:B、________、F(填序号);
(2)上述B步骤操作的目的是________;
(3)上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则对滴定结果的影响
是________ (填“偏大”或“偏小”或“无影响”);
(4)判断到达滴定终点的实验现象是________;
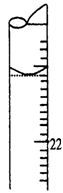
(5)若滴定结束时,滴定管液面如图所示,则终点读数为________mL。
(6)根据读数计算出该待测液的浓度为________。
高二化学填空题简单题查看答案及解析
(12分)某学生用0.1000 mol·L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
A.取20.00 mL待测盐酸溶液注入洁净的锥形瓶中,并加入2-3滴酚酞试液
B.用标准氢氧化钠溶液润洗滴定管2-3次
C.把盛有标准氢氧化钠溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准氢氧化钠溶液注入碱式滴定管至“0”刻度以上2-3mL处
E.调节液面至“0”或“0”刻度以下,记下读数,为3.10mL
F.把锥形瓶放在滴定管下面,用标准NaOH溶液滴定至终点并记下滴定管的读数。
回答下列问题:
(1)正确的操作顺序是:B、________、F(填序号);
(2)上述B步骤操作的目的是________;
(3)上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则对滴定结果的影响
是________ (填“偏大”或“偏小”或“无影响”);
(4)判断到达滴定终点的实验现象是________;
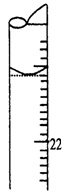
(5)若滴定结束时,滴定管液面如图所示,则终点读数为________mL。
(6)根据读数计算出该待测液的浓度为________。
高二化学填空题简单题查看答案及解析
某学生用0.1000 mol·L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
A.取20.00 mL待测盐酸溶液注入洁净的锥形瓶中,并加入2-3滴酚酞试液
B.用标准氢氧化钠溶液润洗滴定管2-3次
C.把盛有标准氢氧化钠溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准氢氧化钠溶液注入碱式滴定管至“0”刻度以上2-3mL处
E.调节液面至“0”或“0”刻度以下,记下读数,为3.10mL
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管的读数。回答下列问题:

(1)正确的操作顺序是:B、________、F(填序号);
(2)上述B步骤操作的目的是________;
(3)上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则对滴定结果的影响
是________ (填“偏大”或“偏小”或“无影响”);
(4)判断到达滴定终点的实验现象是________;
(5)若滴定结束时,滴定管液面如图所示,则终点读数为________mL。
(6)根据读数计算出该待测液的浓度为________。
高二化学实验题中等难度题查看答案及解析
某学生用0.1000 mol·L-1的NaOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
A.移取20.00 mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准NaOH溶液注入碱式滴定管至刻度0以上2~3 cm;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管液面的刻度。
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)______________________________。
(2)上述B步骤操作的目的是_______________________________________。
(3)实验中用左手控制活塞,眼睛注视___________________,直至滴定终点。判断到达终点的现象是________________________________。
(4)某学生根据3次实验分别记录有关数据如下表:
| 滴定次数 | 待测溶液的体积(mL) | 0.100 0 mol·L-1NaOH的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积(mL) | ||
| 第一次 | 20.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 20.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 20.00 | 0.22 | 26.31 | 26.09 |
依据上表数据列式计算该盐酸溶液的物质的量浓度为__________
(5)用0.1000 mol·L-1 NaOH溶液滴定0.1000 mol·L-1盐酸,如达到滴定的终点时不慎多加了1滴NaOH溶液(1滴溶液的体积约为0.05 mL),继续加水至50 mL,所得溶液的pH等于____________
(6)下列哪些操作会使测定结果偏高(填序号)(_____)
A.锥形瓶中溶液的颜色刚刚由无色变为浅红色即停止滴定 B.碱式滴定管用蒸馏水洗净后立即注入标准液
C.滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失 D.滴定前读数正确,滴定后俯视滴定管读数
E.实验中,用待盛装的溶液润洗锥形瓶
高二化学实验题中等难度题查看答案及解析