-
工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为:
CH2=CH2(g)+ H2O(g) CH3CH2OH(g)△H <0,达到平衡时,要使反应速率加快,同时乙烯的转化率提高,应采取的措施是
CH3CH2OH(g)△H <0,达到平衡时,要使反应速率加快,同时乙烯的转化率提高,应采取的措施是
A.减小压强 B.增大压强 C.分离除乙醇 D.升高温度
【解析】要提高乙烯的转化率,则平衡必须向正反应方向移动。A和C会降低反应速率,升高温度,平衡向逆反应方向移动,所以正确的答案是B。
-
工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为:
CH2=CH2(g)+H2O(g) CH3CH2OH(g)△H <0,达到平衡时,要使反应速率加快,同时乙烯的转化率提高,应采取的措施是
CH3CH2OH(g)△H <0,达到平衡时,要使反应速率加快,同时乙烯的转化率提高,应采取的措施是
A.充入氦气 B.分离除乙醇 C.增大压强 D.升高温度
-
工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为CH2===CH2(g)+H2O(g)  CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等。下图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是:
CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等。下图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是:

A. 合成乙醇的反应一定为吸热反应
B. 目前工业上采用250~300 ℃,主要是因为在此温度下乙烯的转化率最大
C. 目前工业上采用加压条件(7 MPa左右),目的是提高乙醇的产率和加快反应速率
D. 相同催化剂下,在300 ℃ 14.70 MPa乙醇产率反而比300 ℃ 7.85 MPa低得多,是因为加压平衡向逆反应方向移动
-
工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为CH2==CH2(g)+H2O(g) CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等。下图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是
CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等。下图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是
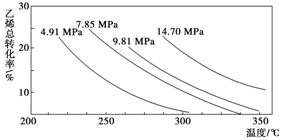
A.合成乙醇的反应一定为吸热反应
B.目前工业上采用250~300 ℃,主要是因为在此温度下乙烯的转化率最大
C.目前工业上采用加压条件(7 MPa左右),目的是提高乙醇的产率和加快反应速率
D.只要给予该反应足够的压强,就可以实现转化率100%
-
工业上,在一定条件下利用乙烯和水蒸气反应制备乙醇。反应原CH2=CH2(g)+H2O(g)=CH3CH2OH(g )△H。已知几种共价键的键能如下:
| 化学键 | C-H | C=C | H-O | C-C | C-O |
| 键能/kJ·mol-1 | 413 | 615 | 463 | 348 | 351 |
下列说法错误的是
A. 上述合成乙醇的反应原子利用率为100%
B. 相同时间段内,用该反应中三种物质表示的该反应的化学反应速率相等
C. 碳碳双键的键能大于碳碳单键键能,但碳碳单键更稳定
D. 上述反应式中,△H=+34kJ·mol-1
-
实验室制取乙烯的反应原理为:CH3CH2OH CH2=CH2↑+H2O,反应时,常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计下列实验确认上述混合气体中有乙烯和二氧化硫。
CH2=CH2↑+H2O,反应时,常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计下列实验确认上述混合气体中有乙烯和二氧化硫。
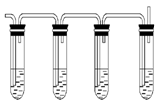
试回答下列问题:
(1)图中①②③④装置盛放的试剂分别是(填选项字母):①_________,④_________。
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(2)能说明SO2存在的现象是___________________________________________________。
(3)确证乙烯存在的现象是_______________________________________________________________。
-
实验室制备1,2-二溴乙烷的反应原理如下所示:
第一步:CH3CH2OH CH2=CH2+H2O;
CH2=CH2+H2O;
第二步:乙烯与溴水反应得到1,2-二溴乙烷。
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃下脱水生成乙醚(CH3CH2OCH2CH3)。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示(部分装置未画出):
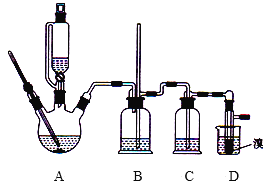
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/(g/cm3) | 0.79 | 2.2 | 0.71 |
| 沸点/(℃) | 78.5 | 132 | 34.6 |
| 熔点/(℃) | -130 | 9 | -116 |
请回答下列问题:
(1)写出乙烯与溴水反应的化学方程式:______。
(2)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_____(填字母代号)。
a.引发反应 b.加快反应速率
c.防止乙醇挥发 d.减少副产物乙醚生成
(3)装置B的作用是______。
(4)在装置C中应加入____ (填字母代号),其目的是吸收反应中可能生成的SO2、CO2气体。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在___ (填“上”或“下”)层。
(6)若产物中有少量副产物乙醚,可用____的方法除去。
-
(10分,每空1分)实验室制乙烯的反应原理为CH3CH2OH  CH2===CH2↑+H2O,制取时常因温度过高而发生副反应,使部分乙醇跟浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和炭黑。
CH2===CH2↑+H2O,制取时常因温度过高而发生副反应,使部分乙醇跟浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和炭黑。
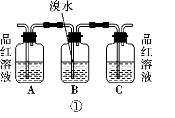


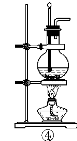
(1)请用图中编号为①、②、③、④的装置设计一个实验,以验证上述反应混合气体中含有CO2、SO2和水蒸气。用装置的编号表示装置的连接顺序(按产物气流从左到右):
→ → → 。(1分)
(2)实验时装置①中A瓶的现象是 ,原因是 。
B瓶中的现象是 ,B瓶溶液的作用是 。
若C瓶中品红溶液不褪色,说明 。
(3)装置③中加的固体药品是 ,以验证混合气体中有 。装置②中盛的溶液是 ,以验证混合气体中的 。
-
由碳的氧化物直接合成乙醇燃料已进入大规模生产。
Ⅰ.目前工业上可以用CO2来生产CH3CH2OH。反应为:2CO2(g)+6H2(g) CH3CH2OH(g)+H2O(g),在一定压强下,该反应的一些实验数据如下表:
CH3CH2OH(g)+H2O(g),在一定压强下,该反应的一些实验数据如下表:
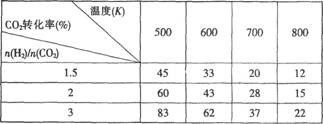
根据表中数据分析:
(1)该反应的正反应是_________(选填“吸热”或“放热”)反应。
(2)提高氢碳比n(H2)/n(CO2),对生成乙醇 _______(选填“不利”、“有利”或“无影响”)。
(3)在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,下列措施中能使c(CH3CH2OH)增大的是_______(填字母,下同)。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出来 D.再充入1molCO2和3molH2
Ⅱ.工业上还采取以CO和H2为原料合成乙醇,其化学反应方程式为:
2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g)
CH3CH2OH(g)+H2O(g)
(4)请写出该反应的化学平衡常数表达式K= ___________。
(5)一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是___________。
A.c(CO)=c(H2) B.v正(CO)=v逆(H2O)
C.容器中的压强不变 D.消耗2molCO的同时生成1molCH3CH2OH
(6)在相同条件下,由CO制取CH3CH2OH的平衡常数远远大于由CO2制取CH3CH2OH的平衡常数。则由CO制取CH3CH2OH的优点是______________________,由CO2制取CH3CH2OH的优点是____________。(写出一点即可)
-
下列关于乙烯说法正确的是
A.乙烯使酸性高锰酸钾溶液及溴的四氯化碳溶液褪色原理相同
B.工业利用乙烯水化法制乙醇,是发生了取代反应
C.水果运输中为延长果实成熟期,常在车厢里放置浸泡过KMnO4溶液的硅藻土
D.乙烯在空气中燃烧,发生火焰明亮并带有浓烟的火焰
CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等。下图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是






