-
在一定条件下,乙烯水化法制备乙醇的热化学方程式:
CH2=CH2(g)+H2O(g)  CH3CH2OH(g) △H= -34 kJ▪mol-1
CH3CH2OH(g) △H= -34 kJ▪mol-1
(1)在密闭容器中投入CH2=CH2(g)、H2O(g)和催化剂发生反应,乙烯的平衡转化率与温度、压强的关系如图所示。
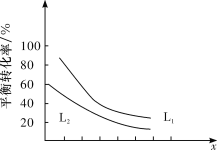
①横坐标x代表_______(填“温度”或“压强”);
②相同条件下L1与L2的大小关系是L1______(填“>”“<”或“=”L2);
③温度升高,上述反应的平衡常数K_____(填“增大”“减小”或“不变”)。
(2)某恒温恒容条件下,有甲、乙体积相同的容器。已知向甲中充入1molCH2=CH2(g)和1mol H2O(g),充分反应后,测得CH2=CH2(g)转化率为40%。乙在相同条件下充入1molCH3CH2OH(g)为起始反应物,充分反应后的热量变化为_____(填字母代号)。
A.放热13.6kJ B.吸热13.6kJ C.放热20.4kJ D.吸热20.4kJ
-
工业上,在一定条件下利用乙烯和水蒸气反应制备乙醇。反应原CH2=CH2(g)+H2O(g)=CH3CH2OH(g )△H。已知几种共价键的键能如下:
| 化学键 | C-H | C=C | H-O | C-C | C-O |
| 键能/kJ·mol-1 | 413 | 615 | 463 | 348 | 351 |
下列说法错误的是
A. 上述合成乙醇的反应原子利用率为100%
B. 相同时间段内,用该反应中三种物质表示的该反应的化学反应速率相等
C. 碳碳双键的键能大于碳碳单键键能,但碳碳单键更稳定
D. 上述反应式中,△H=+34kJ·mol-1
-
实验室中制备乙烯的方法是使乙醇脱水,反应可以简单地表示为CH3CH2OH―→CH2=CH2↑+H2O。已知CH2=CH2(g)和C2H5OH(l)的燃烧热分别是1 411.0 kJ·mol-1和1 366.8 kJ·mol-1。则实验室用C2H5OH(l)制备CH2=CH2(g)生成1 mol液态水的ΔH为( )
A.-44.2 kJ·mol-1
B.+44.2 kJ·mol-1
C.-2 777.8 kJ·mol-1
D.+2 777.8 kJ·mol-1
-
下列有机化合物的说法正确的是( )
A.用浓硫酸和乙醇在加热条件下制备乙烯,应该迅速升温到140℃
B. 与
与  互为同系物
互为同系物
C.冬天汽车里用的防冻液是乙醇
D. CH3CH2OH CH3CH2CH3三者沸点、溶解度依次降低
CH3CH2OH CH3CH2CH3三者沸点、溶解度依次降低
-
以下化学用语表述正确的是( )
A.乙烯的结构简式:CH2CH2 B.H2O2的电子式:
C.乙醇的分子式:CH3CH2OH D.溴乙烷的比例模型:
-
根据乙烯和乙醇的知识填空。
(1)完成下列化学方程式:CH2= CH2+________  CH3CH2OH;
CH3CH2OH;
(2)乙醇跟乙酸在浓硫酸催化且加热的条件下反应,制取的是________。
-
CO 和H2在一定条件下可以合成乙醇:2CO(g) + 4H2(g)⇌CH3CH2OH(g) + H2O(g),下列叙述中,能说明上述反应在一定条件下一定达到最大限度的是( )
A.CO 全部转化为乙醇
B.断 4NA个H-H 键的同时,生成 46g 乙醇
C.若反应在恒温密闭容器中进行,容器中气体密度不再改变
D.若反应在绝热密闭容器中进行,容器中温度不再改变
-
CO和H2在一定条件下可以合成乙醇:2CO(g)+4H2(g)  CH3CH2OH(g)+H2O(g),
CH3CH2OH(g)+H2O(g),
下列叙述中能说明上述反应在一定条件下一定达到最大限度的是
A.CO全部转化为乙醇
B.正反应和逆反应的化学反应速率均为零
C.CO和H2以1∶2的物质的量之比反应生成乙醇
D.反应体系中乙醇的物质的量浓度不再变化
-
CO和H2在一定条件下可以合成乙醇:2CO(g) +4H2(g)  CH3CH2OH(g) +H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是
CH3CH2OH(g) +H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是
A. CO全部转化为乙醇
B. 正反应和逆反应的化学反应速率均为零
C. CO和H2以1∶2的物质的量之比反应生成乙醇
D. 反应体系中乙醇的物质的量浓度不再变化
-
工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为:
CH2=CH2(g)+ H2O(g) CH3CH2OH(g)△H <0,达到平衡时,要使反应速率加快,同时乙烯的转化率提高,应采取的措施是
CH3CH2OH(g)△H <0,达到平衡时,要使反应速率加快,同时乙烯的转化率提高,应采取的措施是
A.减小压强 B.增大压强 C.分离除乙醇 D.升高温度
【解析】要提高乙烯的转化率,则平衡必须向正反应方向移动。A和C会降低反应速率,升高温度,平衡向逆反应方向移动,所以正确的答案是B。
CH3CH2OH(g) △H= -34 kJ▪mol-1

 与
与  互为同系物
互为同系物