某研究性学习小组为了测定某品牌铝合金中铝的含量,现设计了如下实验:
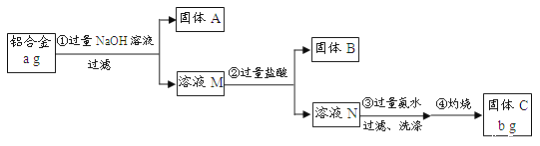
已知:该铝合金的主要成分为Al2O3、MgO、CuO、SiO2;2NaOH+SiO2=Na2SiO3+H2O;Na2SiO3+
2HCl=2NaCl+H2SiO3↓。
请回答下列问题:
(1)固体A的成分是_______;
(2)步骤③中生成沉淀的离子方程式为_____;
(3)检验步骤③中沉淀是否洗涤干净的实验操作为______;
(4)该样品中铝的质量分数是______。(用a、b表示)
高一化学工业流程简单题
某研究性学习小组为了测定某品牌铝合金中铝的含量,现设计了如下实验:

已知:该铝合金的主要成分为Al2O3、MgO、CuO、SiO2;2NaOH+SiO2=Na2SiO3+H2O;Na2SiO3+
2HCl=2NaCl+H2SiO3↓。
请回答下列问题:
(1)固体A的成分是_______;
(2)步骤③中生成沉淀的离子方程式为_____;
(3)检验步骤③中沉淀是否洗涤干净的实验操作为______;
(4)该样品中铝的质量分数是______。(用a、b表示)
高一化学工业流程简单题
某研究性学习小组为了测定某品牌铝合金中铝的含量,现设计了如下实验:
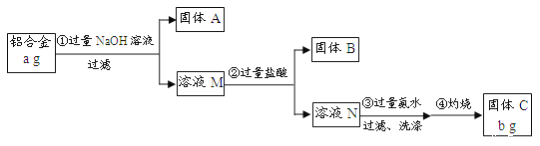
已知:该铝合金的主要成分为Al2O3、MgO、CuO、SiO2。
请回答下列问题:
(1)固体A的成分是_______;
(2)生成固体B的化学方程式为_____;步骤③中生成沉淀的离子方程式为_____;
(3)检验步骤③中沉淀是否洗涤干净的实验操作为______;
(4)该样品中铝的质量分数是______;(用a、b表示)
高一化学综合题中等难度题查看答案及解析
某研究性学习小组为了测定某品牌铝合金中铝的含量,现设计了如下实验:

已知:该铝合金的主要成分为Al2O3、MgO、CuO、SiO2;2NaOH+SiO2=Na2SiO3+H2O;Na2SiO3+
2HCl=2NaCl+H2SiO3↓。
请回答下列问题:
(1)固体A的成分是_______;
(2)步骤③中生成沉淀的离子方程式为_____;
(3)检验步骤③中沉淀是否洗涤干净的实验操作为______;
(4)该样品中铝的质量分数是______。(用a、b表示)
高一化学工业流程简单题查看答案及解析
(12分)某研究性学习小组为了测定某品牌合金中铝的含量,现设计了如下实验:
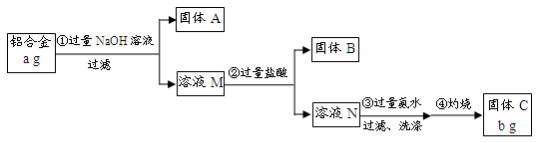
已知:(1)该铝合金的主要成分为铝、镁、铜、硅。
(2)常温下,硅能和NaOH发生反应:Si+2NaOH+H2O===Na2SiO3+2H2↑。
请回答下列问题:
(1)固体A的成分是 ;
(2)生成固体B的离子方程式为 ;
步骤③中生成沉淀的离子方程式为 ;
(3)检验步骤③中沉淀是否洗涤干净的实验操作为
;
(4)该样品中铝的质量分数是 ;(用a、b表示)
(5)下列因操作不当,会使测定结果偏大的是 ;
A.第①步中加入NaOH溶液不足 B.第②步中加入盐酸不足时
C.第③步中沉淀未用蒸馏水洗涤 D.第④步对沉淀灼烧不充分
高一化学填空题中等难度题查看答案及解析
某研究性学习小组为了测定某品牌合金中铝的含量,现设计了如下实验:
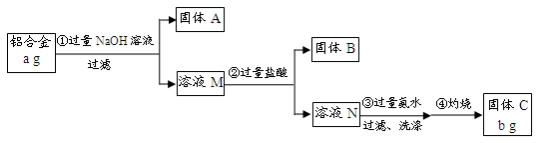
已知:(1)该铝合金的主要成分为铝、镁、铜、硅。
(2)常温下,硅能和NaOH发生反应:Si+2NaOH+H2O===Na2SiO3+2H2↑。
(3)硅酸不溶于水
(4)固体C为Al2O3
请回答下列问题:
(1)固体A在潮湿的空气中久置可能会发生一个明显的变化,这个变化是 ;发生反应的化学方程式为 ;
(2)步骤③中洗涤沉淀的实验操作为 ;
(3)该样品中铝的质量分数是 (用a、b表示);
(4)下列因操作不当,会使测定结果偏大的是 ;
A.第③步中沉淀未用蒸馏水洗涤
B.第①步中加入NaOH溶液不足
C.第④步对沉淀灼烧不充分
高一化学填空题中等难度题查看答案及解析
某铝合金中含有铁、铝、镁、铜、硅。为了测定该合金中铝的含量,现设计了如下实验:
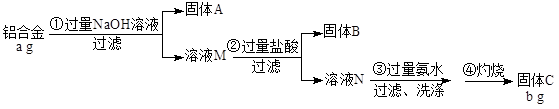
已知:Si+2NaOH+ H2O =Na2SiO3+2
H2↑,H2SiO3是不溶于水的弱酸。
(1)固体A的成分是:____________,溶液M中的阴离子有:____________________
(2)步骤①②③中,过滤时玻璃棒的作用是 ,步骤④中,用到的仪器有三脚架、酒精灯以及
(3)步骤③中生成沉淀的离子方程式为:____________________________
(4)在空气中将NaOH溶液滴入FeCl2溶液中,观察到的现象是 ,反应的化学方程式是
(5)该样品中铝的质量分数是:_____________________(用a、b表示)。
(6)第④步中的沉淀需用蒸馏水洗涤,若未洗涤会使测定结果___________(填偏大或偏小)。
高一化学实验题困难题查看答案及解析
(20分)某铝合金中含有铁、铝、镁、铜、硅。为了测定该合金中铝的含量,现设计了如下实验:
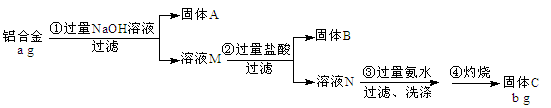
已知:Si+2NaOH+ H2O =Na2 Si O3+2H2↑,H2Si O3是不溶于水的弱酸。
(1)固体A的成分是:____________,溶液M中的阴离子有:____________________
(2)步骤③中生成沉淀的离子方程式为:_____________________________________
(3)步骤④中,用到的仪器有三脚架、酒精灯以及
(4)在空气中将NaOH溶液滴入FeCl2溶液中,观察到的现象是 ,反应的化学方程式是 ,
(5)该样品中铝的质量分数是:_______________________________(用a、b表示)。
(6)下列因操作不当,会使测定结果偏大的是___________
A.第①步中加入NaOH溶液不足 B.第②步中加入盐酸不足时
C.第④步中的沉淀未用蒸馏水洗涤 D.第④步对沉淀灼烧不充分
高一化学填空题中等难度题查看答案及解析
(14分)某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物。某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究:
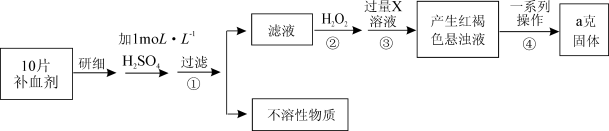
请回答下列问题:
Ⅰ.(1)实验时用10mol·L-1的浓硫酸配制100 mL 1 mol·L-1 H2SO4溶液,所需浓硫酸的体积为 mL。
(2)容量瓶所具备的功能是 (填序号)。
A.配制一定体积准确浓度的溶液
B.长期贮存溶液
C.常用来代替量筒量取一定体积的液体
D.用来溶解固体溶质
(3)在下列配制过程示意图中,错误的有(填序号) 。
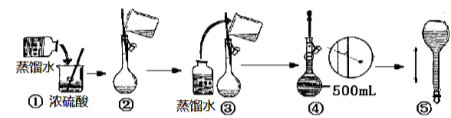
(4)下列说法正确的是 。
A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差
B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察, 所配溶液浓度会偏低
Ⅱ.(1)步骤③中产生的红褐色物质是(填化学式) 。
(2)从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:
a. , b.洗涤, c.灼烧, d.冷却
(3)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为 g。
高一化学实验题极难题查看答案及解析
某铝合金中含有单质铝、镁、铜、硅,为了测定该合金中铝的含量,设计了如下实验流程,请回答有关问题:
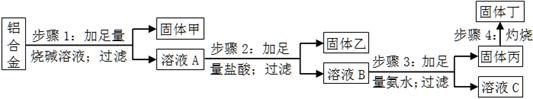
(1)步骤1所得固体甲的成分为________。
(2)步骤2中加足量盐酸,而不采用通入足量二氧化碳的原因为________。
(3)步骤3中生成固体丙的离子方程式为________;溶液C中所含有的阳离子符号为________。
(4)步骤4所发生反应的化学方程式为________。
(5)现用托盘天平称取10.0g铝合金进行上述流程图所示操作,所得固体丁质量为15.3g,则该铝合金中铝的质量分数为________;并判断以下操作对铝质量分数测定的影响(填“偏大”、“偏小”或“无影响”)。
a.步骤1中烧碱量不足,则________;
b.步骤4中灼烧不充分,则________。
高一化学实验题中等难度题查看答案及解析
某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物。某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究:
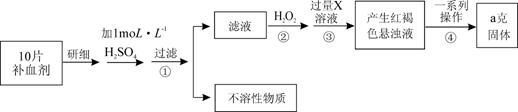
请回答下列问题:
Ⅰ.(1)实验时用18.4 mol·L-1的浓硫酸,配制100 mL 1 mol·L-1 H2SO4溶液,所需浓硫酸的体积为________。(计算结果精确到小数点后一位)
(2)下列操作中,容量瓶所具备的功能有________(填序号)。
A.配制一定体积准确浓度的标准溶液 B.长期贮存溶液
C.用来溶解固体溶质 D.常用来代替量筒量取一定体积的液体
(3)在下列配制过程示意图中,有错误的是(填写序号)________。
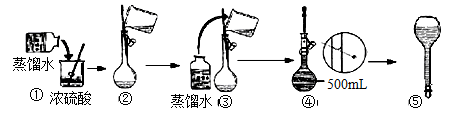
(4)下列说法正确的________
A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差
B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察, 所配溶液浓度会偏低
D.容量瓶使用前先要检查是否漏液,具体操作是向容量瓶中加蒸馏水,倒置不漏液即可
Ⅱ.(1)步骤②加入过量H2O2的目的:________。
(2)从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:
a.________,b. 洗涤,c. 灼烧,d. 冷却
(3)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为________。
Ⅲ.已知人体不能很好地吸收利用Fe3+,科学研究表明服用含硫酸亚铁的补血剂时,同时服用维生素C,以利于铁元素的吸收。试分析维生素C在这一过程中的作用是________。
高一化学实验题简单题查看答案及解析
某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物。某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究:
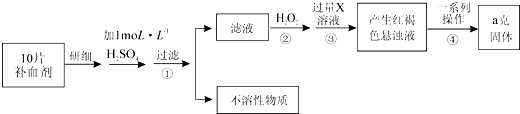
请回答下列问题:
Ⅰ.(1)实验时用10mol•L-1的浓硫酸,配制100mL 1mol•L-1 H2SO4溶液,所需浓硫酸的体积为_________mL;
(2)下列操作中,容量瓶所具备的功能有(填序号);
A.配制一定体积准确浓度的标准溶液
B.长期贮存溶液
C.常用来代替量筒量取一定体积的液体
D.用来溶解固体溶质
(3)在下列配制过程示意图中,有错误的是__________(填写序号);
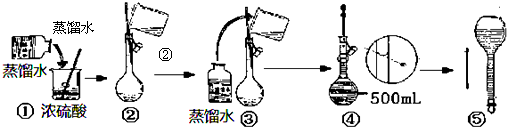
(4)下列说法正确的__________
A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差
B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察,所配溶液浓度会偏低
Ⅱ.(1)步骤②加入过量H2O2后,溶液中主要存在的金属阳离子是_____________;
(2)从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:
a.__________,b.洗涤,c.灼烧,d.冷却
(3)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为__________g。
高一化学实验题极难题查看答案及解析