-
冶金工业、硝酸工业的废气废液中含氮化合物污染严重,必须处理达标后才能排放。
Ⅰ.用活性炭处理工厂尾气中的氮氧化物。
(1)已知:①4NH3(g)+5O2(g) =4NO(g)+6H2O(l) ΔH1=a kJ·mol−1
②4NH3(g)+3O2(g) =2N2(g)+6H2O(l) ΔH2=b kJ·mol−1
③C(s)+O2(g) =CO2(g) ΔH3=c kJ·mol−1
则反应C(s)+2NO(g) N2(g)+CO2(g)的ΔH=________。
N2(g)+CO2(g)的ΔH=________。
(2)在容积不变的密闭容器中,一定量的NO与足量的C发生反应:C(s)+2NO(g) N2(g) + CO2(g) ΔH= Q kJ·mol−1,平衡时c(NO)与温度T的关系如图1所示,下列说法正确的是________。
N2(g) + CO2(g) ΔH= Q kJ·mol−1,平衡时c(NO)与温度T的关系如图1所示,下列说法正确的是________。
A.其他条件不变,改变活性炭的用量,平衡一定不移动
B.该反应的Q>0,所以T1、T2、T3对应的平衡常数:K1<K2<K3
C.温度为T2时,若反应体系处于状态D,则此时 υ(正)>υ(逆)
D.若状态B、C、D体系的压强分别为p(B)、p(C)、p(D),则p(D)=p(C)>p(B)


(3)已知某温度时,反应C(s)+2NO(g) N2(g)+CO2(g)的平衡常数K=
N2(g)+CO2(g)的平衡常数K= ,在该温度下的2L密闭容器中投入足量的活性炭和2.0 mol NO发生反应,t1时刻达到平衡,请在图2中画出反应过程中c(NO)随时间t的变化曲线。_________________
,在该温度下的2L密闭容器中投入足量的活性炭和2.0 mol NO发生反应,t1时刻达到平衡,请在图2中画出反应过程中c(NO)随时间t的变化曲线。_________________
Ⅱ.用纳米铁粉或电解法处理废水中的硝酸盐。
(4)纳米铁粉处理污水中NO3−的离子方程式为:4Fe+NO3–+10H+=4Fe2++NH4++3H2O。
实验证实,pH偏低将会导致NO3−的去除率下降,其原因是________________。相同条件下,纳米铁粉去除不同水样中NO3−的速率有较大差异(见下图),产生该差异的可能原因是________________________。

(5)电解法处理水中硝酸盐的原理是:以金属Pt作电极,用质子交换膜把溶液分为阴阳两极区,阴极区为含硝酸盐的工业废水,接通直流电源进行电解,产物为N2。请写出阴极的电极反应式____________。
-
硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放。某校化学兴趣小组欲测定某硫酸工厂排放尾气中二氧化硫的含量,分别采用以下方案:
[甲方案]:如右图所示,图中气体流量计B用于准确测量通过的尾气体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。

(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是___________________________________。
(2)洗气瓶C中溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量_________(填“偏高”、“偏低”或“无影响”)。
[乙方案]:实验步骤如下面流程图所示:

(3)步骤①中过量H2O2的作用是________
(4)写出步骤②中反应的化学方程式______________________________________
(5)步骤②中Ba(OH)2是否足量的判断方法是_______________________________
___________________________________________________________________。
(6)通过的尾气体积为V L(已换算成标准状况)时,该尾气中二氧化硫的含量(体积分数)为_____________________________(用含有V、m的代数式表示)。
-
硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时必需经处理后才能排放。某校化学兴趣小组欲测定某硫酸工厂排放尾气中二氧化硫的含量,分别采用以下方案:
【甲方案】如下图所示,图中气体流量计B用于准确测量通过的尾气体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。

(1)洗气瓶C中导管末端连接一个多孔球泡D,其目的是______________________________。
(2)洗气瓶C中的溶液还可以用其他试剂代替,如酸性高锰酸钾溶液,你认为选择酸性高锰酸钾溶液的理由有________________________________________________________。
(3)洗气瓶C中溶液蓝色消失后,若没有及时关闭活塞A,则测得的SO2含量____________(填“偏高”、“偏低”或“无影响”)。若某实验小组同学测得的SO2含量总是偏低,可能的原因是__________________________________________________。(假设实验装置、测量仪器、药品和实验操作程序均合理)
【乙方案】:实验步骤如下面流程图所示:

(4)写出步骤②中反应的化学方程式____________________________________________。
(5)步骤③中判断沉淀已经洗涤干净的方法是_______________________________________。
(6)实验中若通过的尾气体积为33.6L (已换算成标准状况),最终所得固体质量为0.233g,试通过计算确定该尾气中二氧化硫的含量是否达到排放标准(写出计算过程)。
-
要减轻大气污染,必须加强对工业废气和汽车尾气等的治理.根据所学知识回答下列问题:
(1)控制燃煤产生的SO2排放,能够减少_________型酸雨的形成.燃煤排放的烟气中还古有其他大气污染物,请列举两种:__________________.
(2)煤的气化和液化是实现能源清洁化的重要途径.将焦炭在高温下与水蒸气反应,得到CO和H2,就是煤的气化过程,该反应的化学方程式为__________________________.
(3)在汽车尾气排放口加装“三效催化净化器”,在催化剂的作用下,可将尾气中的CO、NO转化为空气中的两种无毒气体,该反应的化学方程式为_______________________.
(4)室内空气污染物包括CO、C02、甲醛、苯等,在这四种污染物中,由家用燃料燃烧产生的是_________;由建筑和装修产生的是_________.
-
防治环境污染,改善生态环境己成为全球的共识。
(1)垃圾应分类收集。导致“白色污染”的生活垃圾应放置于贴有 (填字母)标志的垃圾筒内。

(2)工业废水需处理达标后才能排放。下列废水处理的方法合理的是 (填字母)。
a.用中和法除去废水中的酸 b.用混凝法除去废水中的重金属离子
c.用氯气除去废水中的悬浮物 d.用氧化还原法除油类、氰化物
(3)为了减少煤燃烧产生的SO2对大气造成的污染,可向煤中加入适量石灰石。石灰石与煤燃烧时产生的SO2及空气中的O2反应,生成CaSO4和CO2,写出该反应的化学方程 。
(4)为了改善空气质量,必须控制大气中二氧化硫、氮氧化物、烟尘等污染物的排放量。为控制大气中二氧化硫的排放,常采取的措施是对化石燃料进行 。对汽车加装尾气催化净化装置,使其中的有害气体NO、CO转化为无害气体,该反应的化学方程式为 。
-
工业含铬(Ⅵ)污水能污染水源,被人体吸收后易积累而导致器官癌变,必须经无害化处理后才能排放。青岛某污水处理厂的工艺流程如图:

回答下列问题:
(1)CrO42-氧化性较弱,酸性条件下转化为具有较强氧化性的Cr2O72-的离子方程式为__。
(2)已知N2H4与Cr2O72-反应生成无毒气体。若要处理Cr2O72-浓度为0.01mol·L-1的废水1m3,至少需要加入N2H4__kg。
(3)含有SO32-的废水可以代替N2H4处理酸性含铬(Ⅵ)废水,用离子方程式表示其反应原理__。
(4)Cr(OH)3的化学性质与Al(OH)3相似。上述流程中“②加入废碱调pH”时要控制溶液的pH不能过高,原因是__。
(5)含铬(Ⅵ)污水也可用电解法处理。用铁和石墨作电极电解污水,Cr2O72-在阳极区转化为Cr3+,随着电解的进行,溶液pH逐渐增大,Cr3+转化为Cr(OH)3沉淀除去。
①该电解装置中用___作阳极,阳极区除生成Cr(OH)3外还有_沉淀(写化学式)。
②阴极电极反应式为__。
-
(1)含苯酚的工业废水必须处理达标后才能排放,苯酚含量在1 g·L-1以上的工业废水应回收苯酚。某研究性学习小组设计下列流程,探究废水中苯酚的回收方法。







①可用____________________为试剂检验水样中是否含有苯酚。
②操作Ⅰ的名称为________________,试剂a的化学式为_________________________。
③通入CO2发生反应生成苯酚的化学方程式为____________________________________。
(2)某有机物的分子式为C3H6O3。
①1 mol该有机物充分燃烧消耗的O2在标准状况下的体积为________________ L。
②若两分子该有机物能生成六元环状结构,写出该反应的化学方程式:_______________________。
-
化学和环境保护、食品营养、材料应用等密切相关。
(1)防治环境污染、改善生态环境已成为全人类的共识。工业废水需处理达标后才能排放。轧钢厂排出的废水主要是含盐酸的酸性废水,处理此废水可采用的方法是____________(填字母)。
a.沉淀法 b.中和法 c.氧化还原法
(2)营养平衡、合理用药是保证人体健康和生活质量的重要途径。
①人体需要的营养素主要有糖类、______________、蛋白质、无机盐、维生素和水。在氢、钠、铁这三种元素中,属于人体生命活动必需微量元素的是_____________。
②下列物质中,具有解热镇痛疗效的是______________(填字母)。
a.氨基酸 b.阿斯匹林 c.青霉素
③有些药片常用淀粉作为黏合剂,淀粉进入人体后在人体内酶的催化作用下逐步水解,最终转化为___________ (填物质的名称)。维生素C能防治坏血病并具有还原性,验证维生素C有还原性可以使用淀粉溶液和____________试剂共同完成。
(3)材料是人类社会发展的物质基础,材料科学的发展离不开化学。
①陶瓷、水泥和普通玻璃都是生活中最常见的材料,它们属于___________ (填字母)。
a.金属材料 b.无机非金属材料 c.有机高分子材料
制造普通玻璃时,需要的主要原料有纯碱、石灰石和___________ (填化学式)。
②钢铁制品在潮湿的空气中发生___________ (填“化学”或“电化学”)腐蚀是造成钢铁腐蚀的主要原因。硬铝(一种铝合金)是制造飞机和宇宙飞船的理想材料,和纯铝相比,硬铝的强度___________ (填“低”、“高”或“无法确定”),具有较强的抗腐蚀能力。
③在尼龙、棉花、涤纶这三种物质中,属于天然纤维的是___________。橡胶是制造轮胎的重要原料,天然橡胶通过____________ (填“硫化”、“氧化”或“老化”)措施可增大其强度、弹性和化学稳定性等。“白色污染”已成为当今社会的一大公害,“白色污染”主要是___________ (填“废塑料制品”、“废橡胶制品”或“生活垃圾”)造成的。
-
“低碳”在工业生产中意义重大,充分利用原材料,不排放或减少排放“三废”,不同工厂联合生产等都是很好的“低碳”生产方式。下面是几家工厂利用废气、废液、废渣联合生产化肥硫酸铵的工艺:
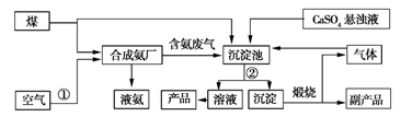
请回答下列问题:
(1)操作②为 。
(2)工业合成氨的化学方程式为 。
(3)沉淀池中生成硫酸铵的化学方程式为 。
(4)在实验室中检验氨气的方法是 。
(5)副产品的化学式为 。该联合生产工艺中可以循环使用的物质是 。
-
硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放。某校兴趣小组欲测定硫酸工业尾气中二氧化硫含量,采用以下方案:
甲方案:如下图所示,图中气体流量计B用于准确测量通过尾气的体积。将尾气通入一定体积已知浓度的碘水中测定二氧化硫的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。

(1)洗气瓶C中发生反应的化学方程式为:_______________;
(2)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验准确度,其理由是:___________________;
(3)洗气瓶C溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量将_________(填“偏高”、“偏低”或“无影响”);
(4)下列试剂中,可以用来替代洗气瓶C中溶液的是_________。(选填字母编号)
a.NaOH溶液 b.品红溶液
c.酸性高锰酸钾溶液 d.Na2CO3溶液
乙方案:实验步骤如以下流程图所示:

(5)写出步骤②中反应的离子方程式;_________________________
(6)通过的尾气体积为VL(已换算成标准状况)时,该尾气中二氧化硫含量(体积分数)为________________(用含V、m的代数式表示)
N2(g)+CO2(g)的ΔH=________。
N2(g) + CO2(g) ΔH= Q kJ·mol−1,平衡时c(NO)与温度T的关系如图1所示,下列说法正确的是________。


N2(g)+CO2(g)的平衡常数K=
,在该温度下的2L密闭容器中投入足量的活性炭和2.0 mol NO发生反应,t1时刻达到平衡,请在图2中画出反应过程中c(NO)随时间t的变化曲线。_________________









