-
常温下某一元碱BOH溶液与0.01mol/L的一元强酸HA溶液等体积混合后所得溶液的pH为7,下列说法中正确的是
①反应前,0.01mol/L的一元强酸HA溶液中水电离出的H+的浓度为1×10-12mol/L
②反应前,一元碱BOH其溶液中溶质物质的量浓度一定大于0.01mol/L
③反应后,溶液中离子浓度大小排列顺序一定是c(B+)=c(A-)>c(H+)=c(OH-)
④反应后,混合溶液中HA与A﹣的浓度总和等于0.01mol/L.
A.①② B.①③ C.②④ D.①②④
高三化学单选题中等难度题查看答案及解析
-
常温下某一元碱
溶液与0.01mol/L的一元强酸HA溶液等体积混合后所得溶液的pH为7。下列说法中正确的是( )
①反应前,0.01mol/L的一元强酸HA溶液中水电离出的
的浓度为
②反应前,一元碱
其溶液中溶质物质的量浓度一定大于0.01mol/L
③反应后,溶液中离子浓度大小排列顺序一定是c(B+)=c(A-)>c(H+)=c(OH-)
④反应后,混合溶液中HA与A-的浓度总和等于0.01mo/L
A.①② B.①③ C.②④ D.①②④
高三化学单选题中等难度题查看答案及解析
-
室温下,一元酸HA溶液与一元碱BOH溶液等体积混合,下列有关判断正确的是
A.若混合后所得溶液呈中性,则HA肯定是强酸、BOH肯定是强碱
B.若混合前酸、碱pH之和等于14,混合后所得溶液呈碱性,则BOH肯定是弱碱
C.若混合前酸、碱物质的量浓度相同,混合后所得溶液呈酸性,则HA肯定是弱酸
D.若混合后所得溶液呈酸性,则混合溶液中离子浓度一定满足
c(B+)>c(A-)>c(H+)>c(OH-)
高三化学选择题中等难度题查看答案及解析
-
室温下,一元酸HA溶液与一元碱BOH溶液等体积混合,下列有关判断正确的是( )
A.若混合后所得溶液呈中性,则HA肯定是强酸、BOH肯定是强碱
B.若混合前酸、碱物质的量浓度相同,混合后所得溶液呈酸性,则HA肯定是弱酸
C.若混合前酸、碱pH之和等于14,混合后所得溶液呈碱性,则BOH肯定是弱碱
D.若混合后所得溶液呈酸性,则混合溶液中离子浓度一定满足:C(B+)>C(A-)>C(H+)>C(OH-)高三化学选择题中等难度题查看答案及解析
-
常温下,向l00 mL 0.01 mol/LHA溶液中逐滴加入0.02 mol/LMOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中,正确的是
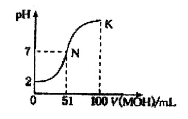
A.HA为一元强酸,MOH为一元强碱
B.K点所示溶液中c(A-)>c(M+)
C.N点水的电离程度小于K点水的电离程度
D.K点对应的溶液的pH=10,则有c(MOH)+c(OH-)-c(H+)=0.005mol/L
高三化学选择题困难题查看答案及解析
-
常温下,向100 mL 0.01 mol/L HA溶液中逐滴加入0.02 mol/L MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。下列说法中,不正确的是
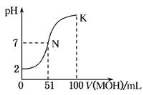
A.HA为一元强酸
B.MOH 为一元弱碱
C.N点水的电离程度小于K点水的电离程度
D.若K点对应溶液的pH=10,则有c(MOH)+c(OH-)-c(H+)=0.005 mol/L
高三化学选择题中等难度题查看答案及解析
-
常温下,向l00mL 0.01mol•L﹣1HA溶液中逐滴加入0.02mol•L﹣1MOH溶液,如图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中,正确的是
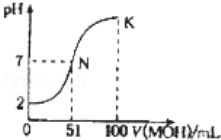
A.HA为一元强酸,MOH为一元强碱
B.K点所示溶液中c(A﹣)>c(M+)
C.N点水的电离程度小于K点水的电离程度
D.K点溶液的pH=10,则有c(MOH)+c(OH﹣)﹣c(H+)=0.005mol•L﹣1
高三化学选择题困难题查看答案及解析
-
常温下,向l00mL 0.01mol/L HA的溶液中逐滴加入0.02mol/L MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是
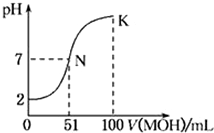
A.HA为一元强酸
B.N点水的电离程度小于K点水的电离程度
C.随着MOH溶液的滴加,比值
不变
D.若K点对应的溶液的pH=10,则有c(MOH)+c(OH-)-c(H+)=0.005mol/L
高三化学选择题困难题查看答案及解析
-
常温下,已知0.01mol/L某酸HA的
,若在其中加入等体积0.01mol/L的某碱BOH,充分反应后所得溶液的pH值( )
A.pH≤7
B.pH=7
C.pH≥7
D.无法确定高三化学选择题中等难度题查看答案及解析
-
常温下,0.2mol/L的一元碱BOH与等浓度的HCl溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
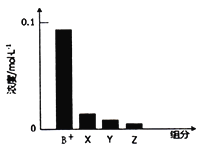
A. BOH 为强碱 B. 该混合液pH=7
C. 图中X表示BOH,Y表示H+,Z表示OH- D. 该混合溶液中: c(Cl-)=c(Y)+c(B+)
高三化学单选题中等难度题查看答案及解析