-
化学实验和查阅资料有助于我们进一步加强对所学知识的巩固,某班同学在老师的指导下展开了对铁及其化合物的延伸学习
(1)实验组同学分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol•L﹣1的溶液。在配制FeCl2溶液时需加入少量铁屑,其目的是_____
(2)甲组同学取2 mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯气反应的离子方程式为_____
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_____
(4)丙组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为_____
(5)丁组同学在完成实验后又对高铁酸钠(Na2FeO4)是一种高效多功能水处理剂产生了兴趣,查阅资料获得如下知识:
Ⅰ.高铁酸钠具有很强的氧化性;
Ⅱ.高铁酸钠投入水中的反应为:4Na2FeO4+10H2O═8NaOH+4Fe(OH)3+3O2↑
Ⅲ.湿法制备的主要离子反应为:2Fe(OH)3+3ClO﹣+4OH﹣═2FeO42﹣+3Cl﹣+H2O
干法制备的主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑
①湿法中的还原剂为_____。
②干法中每生成1moNa2FeO4,转移电子的物质的量为_____
③高铁酸钠能作为高效多功能水处理剂的原因_____、_____
高一化学实验题中等难度题查看答案及解析
-
(12分)某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动。
【提出问题】这种淡黄色粉末是什么?有什么性质和用途?
【查阅资料】①硫是淡黄色粉末,不溶于水;②过氧化钠(Na2O2)是淡黄色粉末,在常温下能与水反应生成碱和一种气体;在呼吸面具中和潜水艇里常用作供氧剂。
【猜想与探究】猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物。
探究:过氧化钠与水反应的生成物的成分。
【实验与结论】
实验操作
实验现象
实验结论
猜想
在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水
_____________________
猜想a、c不成立,猜想b成立。
探究
①用带火星的木条伸入过氧化钠与水反应的试管中
木条复燃
生成物有___________
②往①试管内的溶液中滴加___________
______________
_____________________
生成物有氢氧化钠
【继续探究】小组对过氧化钠能作为供氧剂也很感兴趣,大家讨论认为可能是CO2在常温下能与过氧化钠反应有关,
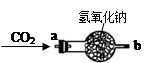
于是设计上图所示的装置继续实验探究。
实验操作
实验现象
实验结论
①将CO2从a口处通入装置内,再把带火星的木条放在装置b口处
木条复燃
CO2在常温下能与过氧化钠反应,该反应的化学方程式为:
____________________________
②取出充分反应后的固体生成物于试管中,往试管内滴加稀盐酸,将生成的氢气通入澄清石灰水中
有气泡产生
石灰水变浑浊
【交流与比较】与我们学过的制氧气方法相比,常选用过氧化钠作为呼吸面具和潜水艇的供氧剂的一个理由是: ________________________________。
高一化学实验题中等难度题查看答案及解析
-
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力。
(1)查阅资料可知:2KMnO4+16HCl(浓)═ 2MnCl2 + 2KCl + 5Cl2↑ + 2H2O。某同学设计图1所示装置来制备纯净、干燥的氯气,其中实验装置或试剂有错误的是(_____)
A.①② B.② C.②③ D.①③
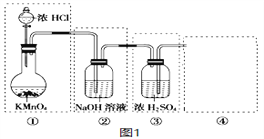
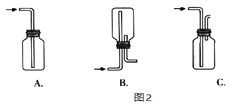
(2)将图1装置修改正确后,虚框④是收集Cl2的装置,请从图2中选用合适的装置__。
(3)将制得的Cl2进行性质实验,装置如图3所示(加热装置省略),请回答以下问题。

①装置E中可观察到________________;反应的化学方程式_____________________。
②装置F在反应中的作用是_____________。
A.收集Cl2 B.防止倒吸 C.混合气体
③装置G所得的溶液中具有漂白性的分子是____,将G所得饱和溶液置于光照下一段时间,溶液中大量减少的粒子有(除H2O分子外)______。(至少写2种)
④装置H的作用_______________。
(4)工业漂白粉常用Cl2与石灰乳反应制得,反应方程式为_________________。家庭使用漂白粉时,为了增强漂白性可滴加的用品是____________。
高一化学实验题中等难度题查看答案及解析
-
氢化钙(CaH2)固体是一种储氢材料,是登山运动员常用的能源提供剂,某化学小组的同学在老师的指导下制备氢化钙。
【查阅资料】
Ⅰ、金属Ca的部分性质有:
① 常温或加热条件下Ca都能与氧气反应;;
② Ca常温遇水立即发生剧烈反应生成氢氧化钙和氢气,并放出大量的热;
③ Ca+H2
CaH2(固体)
Ⅱ、固体CaH2的部分性质有:
①常温:CaH2+2H2O=Ca(OH)2+2H2↑;②CaH2要密封保存。
【进行实验】
该小组同学设计的制取装置如图所示(固定装置略).
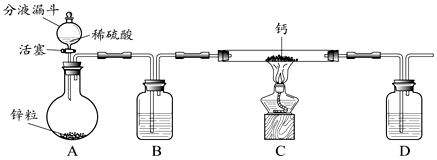
回答下列问题:
(1)写出Ca常温遇水发生反应的化学方程式: 。
(2)B、D中所盛试剂相同,该试剂为 (填名称);D中该试剂的作用是 。
(3)实验时先打开A中活塞,一段时间后,再点燃C中酒精灯,其目的是: 。
【实验反思】
该小组同学通过反思提出问题:上述制得的CaH2是否纯净?
他们再次设计实验进行检验,实验步骤如下:
步骤1:检查装置气密性,装入足量的水和已称好质量为m g的CaH2 样品,按图所示连接仪器(固定装置略)。

步骤2:将Y形管倾斜,使A中的水全部进入B中,样品全部反应后,冷却至室温,读取量筒读数为V mL。
(4)若该实验条件下的气体摩尔体积为Vm L/mol,当V= mL时(用m、Vm表示),表明制得的CaH2样品是纯净的。
高一化学实验题困难题查看答案及解析
-
氢化钙(CaH2)固体是一种储氢材料,是登山运动员常用的能源提供剂,某化学小组的同学在老师的指导下制备氢化钙.
[查阅资料]
氢化钙通常用氢气与钙加热制得.
氢化钙要密封保存,遇水反应生成氢氧化钙和氢气.
钙遇水立即发生剧烈反应生成氢氧化钙和氢气,并放出大量的热.
标准状况下氢气的密度为0.09g/L.
[进行实验]小组同学设计的制取装置如图所示(固定装置略).

回答下列问题:
(1)写出A中发生反应的化学方程式______________________________.
(2)B、D中所盛试剂相同,该试剂为_____________,其作用分别是____________________、___________________________.
(3)实验时先打开A中活塞,一段时间后,再点燃C中酒精灯,其目的是__________________.
(4)装置C中制取氢化钙的化学方程式是______________________.
[实验反思]小组同学通过反思提出问题:上述制得的氢化钙是否纯净?
他们再次设计实验进行检验,实验步骤如下:
步骤1:检查装置气密性,装入足量的水和已称好质量的氢化钙样品,按图所示连接仪器(固定装置略).
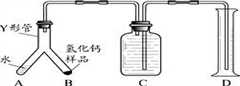
步骤2:将Y形管倾斜,使A中的水全部进入B中,完全反应后,冷却至室温,读取量筒读数.
(5)通过上述实验可分析出制得的氢化钙是否纯净,其依据是______________________________.
高一化学填空题困难题查看答案及解析
-
(11分)物质结构和元素周期律是化学的重要理论知识,通过学习这部分知识,可以对所学元素化合物等知识从理论角度进一步加深理解。有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍, C燃烧时呈现黄色火焰, C的单质在点燃条件下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述完成下列问题:
(1)元素名称:A_________, B__________, C__________, D_________。
(2)写出B元素在周期表中的位置,第______周期,第________族。
(3)A与B可形成多种化合物,其中会引起温室效应的这一者的电子式为____________
(4)C单质在点燃条件下与B单质充分反应所得固体的化学为______________,该固体化合物类型为_______________,存在的作用力有________________。
(5) 用电子式表示化合物C2D的形成过程_____________________________________。
高一化学填空题简单题查看答案及解析
-
某小组同学做“硫在氧气中燃烧”的实验时,老师建议在集气瓶底部放少量NaOH溶液吸收生成的SO2。这种做法引起了同学们的思考:SO2与NaOH是否发生反应。
【查阅资料】通常状况下,1体积水约能溶解40体积SO2。
【实验方案】同学们向充满SO2的软塑料瓶中迅速倒入一定量NaOH溶液,拧紧瓶盖,振荡,发现塑
料瓶变瘪,他们认为SO2与NaOH发生了反应。
【反思与改进】甲同学认为上述实验不够严谨,理由是_________________。于是同学们设计了如下两
个改进方案。
方案一:
实验操作
实验现象
向两个充满SO2的200 mL软塑料瓶中分别注入10 mL水和NaOH溶液,振荡,对比。
两个瓶子变瘪的程度完全相同
乙同学认为由于两个瓶子变瘪的程度完全相同,因此无法证明SO2与NaOH是否发生了反应。试分析导致两个瓶子变瘪的程度完全相同的原因是_____________________。他认为若改变注入水和NaOH溶液的体积便可达到实验目的,注入液体的体积可以是__________(填序号)。
a.15 mL b.8 mL c.5 mL d.3 mL
方案二:
实验操作
实验现象
利用如图所示装置进行实验:
向两个充满SO2的300 mL集气瓶
中分别加入6 mL水和NaOH溶液,
一段时间后,打开止水夹,对比。
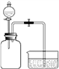
倒吸入两个集气瓶中的液体体积完全相同
丙同学认为上述方案也无法证明SO2与NaOH是否发生反应。你认为导致吸入液体的体积完全相同的原因是___________________。
丁同学思考后,将上述装置进行了改进,便达到实验目的。改进装置如下图所示,你认为装置B的作用是_______________。

高一化学填空题中等难度题查看答案及解析
-
某研究性学习小组得到一块软锰矿样品,其主要成分为二氧化锰( MnO2)和石英(SiO2)。为了制取Cl2和探究氯及其化合物的相关性质,进行如下实验。
【查阅资料】MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑
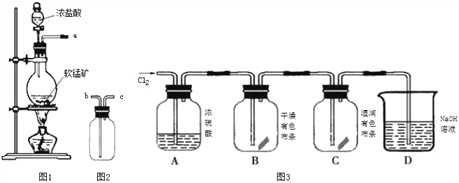
【制取气体】
(1)取适量矿样置于烧瓶中,加入足量浓盐酸并加热,充分反应后烧瓶中残留的固体是____。
(2)收集氯气应将图1导管的a接口与图2导管的_____________接口连接(填“b”或“c)。
(3)已知氯气中含有HCl杂质,可用______________除去。
【实验探究】
(4)把红热的铁丝伸入盛有氯气的集气瓶中,铁丝燃烧产生棕褐色的烟。反应的化学方程式是_______________________________________________________________________。
(5)按图3进行实验,观察到B中的有色布条不褪色,C中的有色布条褪色。由此得出的结论是_____________________________________________________________________。
(6)写出C中反应的化学方程式:_________________________________________________。
【联系实际】
(7)某氯碱工厂的氯气管道发生泄漏,以下采取的措施正确的是______________ (双项选择,填序号)。
A.将人群向高处疏散
B.将人群向低处疏散
C.关闭氯气管道,用碱液浸泡过的棉布覆盖泄漏部位
D.关闭氯气管道,用饱和NaCl溶液浸泡过的棉布覆盖泄漏部位
高一化学实验题困难题查看答案及解析
-
某研究性学习小组得到一块软锰矿样品,其主要成分为二氧化锰(MnO2)和石英(SiO2)。为了制取Cl2和探究氯及其化合物的相关性质,进行如下实验。
【查阅资料】MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
【制取气体】
(1)取适量矿样置于烧瓶中,加入足量浓盐酸并加热,充分反应后,烧瓶中残留的固体是 。
(2)收集氯气应将图1导管的a接口与图2的导管的 接口连接(填“b”或“c”)
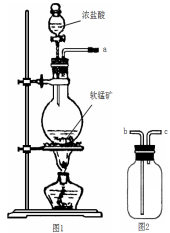
(3)若生成标准状况下11.2LCl2,则参加反应的MnO2的质量为 g。
【实验探究】
(4)把红热的铁丝伸入盛有氯气的集气瓶中,铁丝燃烧产生棕褐色的烟。反应的化学方程式是
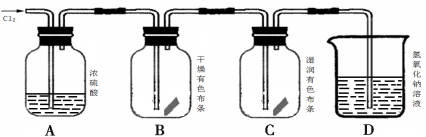
(5)按图3进行实验,观察到B中的有色布条不退色,C中的有色布条退色。由此得出的结论是:
(6)写出D中反应的化学方程式: 。
【知识拓展】
(7)某同学查阅资料得知:高锰酸钾与浓盐酸在常温正好生反应也可以生成氯气(反应的化学方程式为:2KMnO4 + 16HCl(浓) = 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O),该反应的氧化剂是 。.
高一化学实验题极难题查看答案及解析
-
某研究性学习小组学生用图中所示装置(部分夹持装置略)探究NO与Na2O2反应的情况,提出假设并进行相关实验。
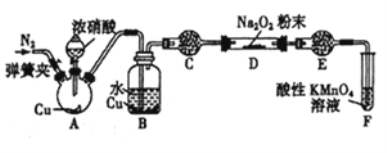
该研究性学习小组同学认为NO 易与O2发生反应,应该更易被Na2O2氧化。查阅资料:2NO+Na2O2=2NaNO2;2NaNO2+2HCl=2NaCl+NO2↑+NO↑+H2O; 酸性条件下,NO 能与MnO4-反应生成NO3-和Mn2+。
(1)在反应前,打开弹簧夹,通入一段时间N2,目的是__________________________。
(2)A 中反应的氧化剂与还原剂的物质的量之比为______________。
(3)B 中观察到的主要现象是____________(填字母编号)。
a.铜片逐渐溶解,溶液变为蓝色 b.有红棕色气泡产生 C.有无色气泡产生
(4)C、E 中所盛装的试剂不能是________(填字母编号)。
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
(5)F 中反应的离子方程式是_________________________________________。
(6)充分反应后,检验D装置中产物的方法是: _____________________________ ,则产物是NaNO2。
高一化学综合题中等难度题查看答案及解析