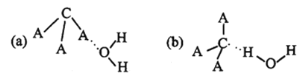-
现有A、B、C、D、E五种元素,原子序数依次增大,且不超过36.A元素的基态原子最外层电子数是次外层的三倍;B元素的基态原子核外有13种不同运动状态的电子;C与B同一周期,原子中未成对电子数是同周期中最多的;D2-的核外电子排布与氩原子相同;E元素的基态原子价电子排布式为3d104s1.请根据相关信息,回答下列问题:
(1)在A、B、C、D四种元素中第一电离能最小的是___________,电负性最大的是___________ (用相应的元素符号表示)
(2)写出DA2的水化物在水中的电离方程式___________.DA3是___________分子(填“极性”或“非极性”)
(3)A、C的简单氢化物中,哪种物质的沸点高,原因是什么? ___________________________
(4)若[E(NH3)4]2+具有对称的空间构型,且当[E(NH3)4]2+中的两个NH3分子被两个Cl-取代时,能得到两种不同结构的产物,则[E(NH3)4]2+的空间构型为_________ (填序号)
a.正四面体 b.平面正方形 c.三角锥形 d.V形
(5)单质E晶胞如图所示,已知E元素相对原子质量为M,原子半径为a pm,密度为dg·cm-3(1pm=10-10cm)写出阿伏加德罗常数NA的表达式___________.(用M、a、d表示)
-
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1;元素Y基态原子的3p轨道上有5个电子;元素Z的原子最外层电子数是其内层电子数的3倍;元素W基态原子的核外电子共有16种运动状态。

(1)①在元素周期表中,元素X位于 区,元素Y在周期表中的位置是 。
②Z所在周期中,第一电离能最大的元素是 (填元素名称)。
③X+的核外电子排布式为 。
④Y和W两元素最高价氧化物对应的水化物酸性较强的是 (填化学式)。
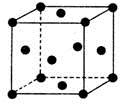
(2)X与Y所形成化合物晶体的晶胞如右图所示。在1个晶胞中,X离子的数目为 ;该化合物的化学式为 。
(3)①在乙醇中的溶解度:Z的氢化物(H2Z)大于H2W,其主要原因是 。
②稳定性:H2Z H2W(填“>”、“<”或“=”),其主要原因是 。
-
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1;元素Y基态原子的3p轨道上有5个电子;元素Z的原子最外层电子数是其内层的3倍;元素W基态原子的核外电子共有16种运动状态。
(1)①在元素周期表中,元素X位于 区,元素Y位于第 周期第 族。
②Z所在周期中,第一电离能最大的元素是 (填元素名称)。
③X+的核外电子排布式为 。
④Y和W两元素最高价氧化物对应的水化物酸性较强的是 (填化学式)。
(2)X与Y所形成化合物晶体的晶胞如图所示。在1个晶胞中,X离子的数目为 ;该化合物的化学式为 。

(3)①在乙醇中的溶解度:Z的氢化物(H2Z)大于H2W,其主要原因是 。
②稳定性: H2Z H2W(填“>”、“<”或“=”),其主要原因是 。
-
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1;元素Y基态原子的3p轨道上有5个电子;元素Z的原子最外层电子数是其内层的3倍;元素W基态原子的核外电子共有16种运动状态。
(1)①在元素周期表中,元素X位于 区,元素Y位于第 周期第 族。
②Z所在周期中,第一电离能最大的元素是 (填元素名称)。
③X+的核外电子排布式为 。
④Y和W两元素最高价氧化物对应的水化物酸性较强的是 (填化学式)。
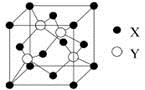
(2)X与Y所形成化合物晶体的晶胞如图所示。在1个晶胞中,X离子的数目为 ;该化合物的化学式为 。
(3)①在乙醇中的溶解度:Z的氢化物(H2Z)大于H2W,其主要原因是 。
②稳定性: H2Z H2W(填“>”、“<”或“=”),其主要原因是 。
-
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1。元素Y基态原子的3p轨道上有5个电子。元素Z的原子最外层电子数是其内层的3倍。元素W基态原子核外电子共有16种运动状态。
⑴①在元素周期表中,元素Y位于第___________周期第___________族,元素X位于___________区;
②Z所在周期中,第一电离能最大的元素是___________;(填元素名称)
③X+的核外电子排布式为___________;与X同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有___________(填元素符号)
④Y和W两元素所形成的最高价氧化物对应的水化物酸性较强的是___________(填化学式)
⑵X与Y所形成化合物晶体的晶胞如图所示。
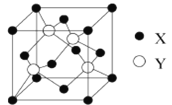
①在1个晶胞中,X离子的数目为___________
②该化合物的化学式为___________
⑶X与W的最高价含氧酸的浓溶液反应的化学方程式为___________
⑷①在乙醇中的溶解度:Z的氢化物(H2Z)大于H2W,其主要原因是___________
②稳定性:H2Z___________H2W(填“<”、“>”或“=”),其主要原因是___________
-
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1。元素Y基态原子的3p轨道上有5个电子。元素Z的原子最外层电子数是其内层的3倍。元素W基态原子核外电子共有16种运动状态。
⑴①在元素周期表中,元素Y位于第___________周期第___________族,元素X位于___________区;
②Z所在周期中,第一电离能最大的元素是___________;(填元素名称)
③X+的核外电子排布式为___________;与X同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有___________(填元素符号)
④Y和W两元素所形成的最高价氧化物对应的水化物酸性较强的是___________(填化学式)
⑵X与Y所形成化合物晶体的晶胞如图所示。

①在1个晶胞中,X离子的数目为___________
②该化合物的化学式为___________
⑶X与W的最高价含氧酸的浓溶液反应的化学方程式为___________
⑷①在乙醇中的溶解度:Z的氢化物(H2Z)大于H2W,其主要原因是___________
②稳定性:H2Z___________H2W(填“<”、“>”或“=”),其主要原因是___________
-
元素X、Y、Z为前四周期元素,X的基态原子核外电子有21种运动状态,元素Y的原子最外层电子数是其内层的3倍,Z与X、Y不在同一周期,且Z原子核外p电子比s电子多5个。
(1)X基态原子的核外电子排布式为______。
(2)X是石油化工中重要的催化剂之一,如催化异丙苯( )裂化生成苯和丙烯。
)裂化生成苯和丙烯。
①1 mol异丙苯分子中含有σ键的数目为________mol。
②异丙苯分子中碳原子轨道的杂化类型为________。
(3)与Y3分子互为等电子体的阴离子为________。
(4)XZ3易溶于水,熔融状态下能够导电,据此可判断XZ3晶体属于________(填晶体类型)。
(5)元素Ce与Y形成的化合物晶体的晶胞结构如下图,该化合物的化学式为________。
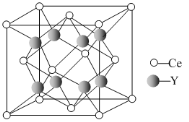
-
若某原子在处于能量最低状态时,价电子层排布为4d25s2,则下列说法正确的是
A. 该元素原子最外层共有4个电子
B. 该元素原子核外第N层上共有10个不同运动状态的电子
C. 该元素处于第五周期IVA族
D. 该元素原子第四电子层上有4个空轨道
-
W、X、Y、Z为原子序数依次增大的前四周期元素,元素W是宇宙中最丰富的元素,元素X的原子的最外层电子数是其内层的3倍,元素Z的基态原子核外电子有24种运动状态,Y、X、Z不在同一周期,且元素Y的基态原子核外电子p电子比s电子多5个。
(1)Z的基态原子的核外电子排布式为_____________。
(2)Z的氧化物是石油化工中重要的催化剂之一,如催化异丙苯()裂化生成苯和丙烯。
①1 mol丙烯分子中含有σ键与π键数目之比为_____________。
②苯分子中碳原子的杂化轨道类型为_____________。
③Z的一种氧化物ZO5中,Z的化合价为+6价,则其中过氧键的数目为_________个。
(3)W、X、Y三种元素的电负性由小到大的顺序为_______(请用元素符号回答)。
(4)ZY3的熔点为1 152 ℃,其在熔融状态下能够导电,据此可判断ZY3晶体属于_________(填晶体类型)。
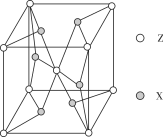
(5)ZX2晶体的晶胞结构如图所示,每个Z原子周围最近的X原子数目为________。若该化合物的相对分子质量为M,晶胞边长为a pm,阿伏加德罗常数的值为NA,则该晶体的密度为_____________g/cm3。
-
周期表前四周期的元素A、B、C、D、E、F,原子序数依次增大,A是周期表中原子半径最小的元素,B的基态原子中只有1个未成对电子,C基态原子中有7种不同运动状态的电子,D的最外层电子数是其所处周期数的3倍,E与D同主族,F的一价阳离子最外层有18个电子。回答下列问题:
(1)F在周期表中的位置是_____________,它的基态原子的电子排布式为_____________
(2)A元素与其他元素形成的含氧酸中,酸根呈三角锥结构的酸是_________,该酸的中心原子的杂化方式为_________
(3)CA3极易溶于水,试从下图中判断CA3溶于水后形成CA3·H2O的合理结构为_____(填字母代号),推理依据是___________
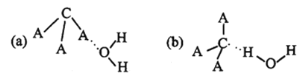
(4)元素B可形成H3BO3,已知H3BO3的电离方程式为H3BO3+2 H2O [B(OH)4]一+H3O+
[B(OH)4]一+H3O+
①基态B、D原子的第一电离能由小到大的顺序为__________(用元素符号表示)
②[B(OH)4]一中B原子的杂化类型为_______________
③写出一种与H3O+互为等电子体的分子的化学式:___________
④H3BO3晶体在热水中的溶解度大于冷水中的溶解度的原因为__________________
)裂化生成苯和丙烯。