线型PAA()具有高吸水性,网状PAA在抗压性、吸水性等方面优于线型PAA。网状PAA的制备方法是:将丙烯酸用NaOH中和,加入少量交联剂a,再引发聚合。其部分结构片段如图:下列说法不正确的是
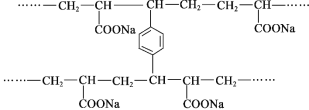
A. 线型PAA的单体不存在顺反异构现象
B. 形成网状结构的过程发生了加聚反应
C. 交联剂a的结构简式是
D. PAA的高吸水性与—COONa有关
高三化学单选题中等难度题
线型PAA()具有高吸水性,网状PAA在抗压性、吸水性等方面优于线型PAA。网状PAA的制备方法是:将丙烯酸用NaOH中和,加入少量交联剂a,再引发聚合。其部分结构片段如图:下列说法不正确的是

A. 线型PAA的单体不存在顺反异构现象
B. 形成网状结构的过程发生了加聚反应
C. 交联剂a的结构简式是
D. PAA的高吸水性与—COONa有关
高三化学单选题中等难度题
线型 PAA( )具有高吸水性,网状 PAA 在抗压性、吸水性等方面优于线型 PAA。网状 PAA 的制备方法是:将丙烯酸用 NaOH 中和,加入少量交联剂 a,再引发聚合。其部分结构片段 如图所示,列说法错误的是
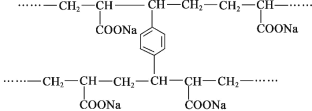
A.线型 PAA 的单体不存在顺反异构现象
B.形成网状结构的过程发生了加聚反应
C.交联剂 a 的结构简式是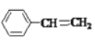
D.PAA 的高吸水性与—COONa 有关
高三化学单选题中等难度题查看答案及解析
线型 PAA( )具有高吸水性,网状 PAA 在抗压性、吸水性等方面优于线型 PAA。网状 PAA 的制备方法是:将丙烯酸用 NaOH 中和,加入少量交联剂 a,再引发聚合。其部分结构片段 如图所示,列说法错误的是
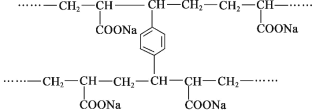
A.线型 PAA 的单体不存在顺反异构现象
B.形成网状结构的过程发生了加聚反应
C.交联剂 a 的结构简式是
D.PAA 的高吸水性与—COONa 有关
高三化学单选题中等难度题查看答案及解析
线型PAA()具有高吸水性,网状PAA在抗压性、吸水性等方面优于线型PAA。网状PAA的制备方法是:将丙烯酸用NaOH中和,加入少量交联剂a,再引发聚合。其部分结构片段如图:下列说法不正确的是

A. 线型PAA的单体不存在顺反异构现象
B. 形成网状结构的过程发生了加聚反应
C. 交联剂a的结构简式是
D. PAA的高吸水性与—COONa有关
高三化学单选题中等难度题查看答案及解析
化学与生产、生活密切联系。下列有关说法不正确的是( )
A.网状结构的聚丙烯酸钠是高吸水性树脂,可用于制造“尿不湿”
B.光导纤维应避免在强碱性环境中使用
C.利用超临界CO2流体作为萃取溶剂符合绿色化学
D.船体镀锌或锡均可保护船体,镀层破损后将立即失去保护作用
高三化学选择题中等难度题查看答案及解析
甘油具有吸水保湿性能。工业上由丙烯制备甘油的流程之一如下:

下列说法中正确的是
A. ①②③均为取代反应
B. CH2ClCHClCH2Cl的同分异构体有5种(不含立体异构)
C. 流程中4种有机物均可使溴的CCl4溶液褪色
D. CH2=CHCH2Cl、CH3CH=CH2分子均至少有6 个原子共平面
高三化学单选题中等难度题查看答案及解析
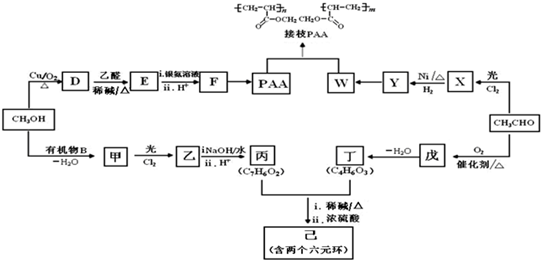
吸水性高分子材料PAA、接枝PAA、用于化妆品的化合物己的合成路线如图:
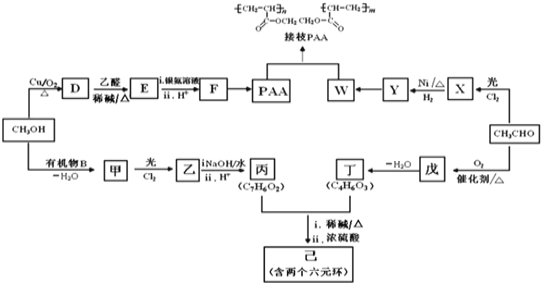
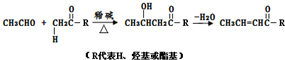
已知:
Ⅰ.连在同一个碳原子上的两个羟基之间容易失去一分子水
Ⅱ.两个羧酸分子的羧基之间能失去一分子水
Ⅲ.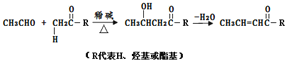
请回答:
(1)D中的官能团是______________
(2)D→E的化学方程式是_____________________________________
(3)F→PAA的化学方程式是___________________________
(4)①X的结构简式是_________
②Y→W所需要的反应条件是______________________
(5)B为中学常见有机物,甲与FeCl3溶液发生显色反应,丙中的两个取代基互为邻位.
①甲→乙的化学方程式是________________________________________
②关于丙的说法正确的是________
a.能与银氨溶液发生银镜反应
b.与有机物B互为同系物
c.不存在芳香醇类的同分异构体
(6)丁的核磁共振氢谱只有一种峰,在酸性条件下能水解,水解产物能与NaHCO3反应产生CO2.己的结构简式是______________________________
高三化学推断题中等难度题查看答案及解析
高三化学填空题中等难度题查看答案及解析
碘化钠在医疗及食品方面有重要的作用。实验室用NaOH、单质碘和水合肼(N2H·H2O)为原料制备碘化钠。已知:水合肼具有还原性。回答下列问题:
(1)水合肼的制备有关反应原理为:CO(NH2)2(尿素)+NaClO+2NaOHN2H4·H2O+NaCl+Na2CO3
①制取次氯酸钠和氧氧化钠混合液的连接顺序为__________(按气流方向,用小写字母表示)。
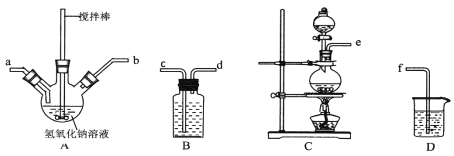
若该实验温度控制不当,反应后测得三颈瓶内ClO-与ClO3-的物质的量之比为5:1,则氯气与氢氧化钠反应时,被还原的氯元素与被氧化的氯元素的物质的量之比为________。
②制备水合肼时,应将___________滴到 __________ 中(填“NaClO溶液”或“尿素溶液”),且滴加速度不能过快。
(2)碘化钠的制备采用水合肼还原法制取碘化钠固体,其制备流程如图所示:
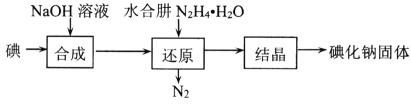
在“还原”过程中,主要消耗反应过程中生成的副产物IO3-,该过程的离子方程式为______________________________________。工业上也可以用硫化钠或铁屑还原碘酸钠制备碘化钠,但水合肼还原法制得的产品纯度更高,其原因是_________________________________。
(3)测定产品中NaI含量的实验步骤如下:
a.称取10.00g样品并溶解,在500mL容量瓶中定容;
b.量取25.00mL待测液于锥形瓶中,然后加入足量的FeCl3溶液,充分反应后,再加入M溶液作指示剂:
c.用0.2100mol·L-1的Na2S2O3标准溶液滴定至终点(反应方程式为;2Na2S2O3+I2=Na2S4O6+2NaI),重复实验多次,测得消耗标准溶液的体积为15.00mL。
①M为____________(写名称)。
②该样品中NaI的质量分数为_______________。
高三化学实验题中等难度题查看答案及解析
碘化钠在医疗及食品方面有重要的作用。实验室用NaOH、单质碘和水合肼(N2H·H2O)为原料制备碘化钠。已知:水合肼具有还原性。回答下列问题:
(1)水合肼的制备有关反应原理为:CO(NH2)2(尿素)+NaClO+2NaOHN2H4·H2O+NaCl+Na2CO3
①制取次氯酸钠和氧氧化钠混合液的连接顺序为__________(按气流方向,用小写字母表示)。
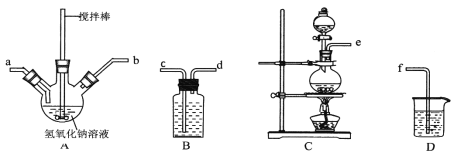
若该实验温度控制不当,反应后测得三颈瓶内ClO-与ClO3-的物质的量之比为5:1,则氯气与氢氧化钠反应时,被还原的氯元素与被氧化的氯元素的物质的量之比为________。
②制备水合肼时,应将___________滴到 __________ 中(填“NaClO溶液”或“尿素溶液”),且滴加速度不能过快。
(2)碘化钠的制备采用水合肼还原法制取碘化钠固体,其制备流程如图所示:

在“还原”过程中,主要消耗反应过程中生成的副产物IO3-,该过程的离子方程式为______________________________________。工业上也可以用硫化钠或铁屑还原碘酸钠制备碘化钠,但水合肼还原法制得的产品纯度更高,其原因是_________________________________。
(3)测定产品中NaI含量的实验步骤如下:
a.称取10.00g样品并溶解,在500mL容量瓶中定容;
b.量取25.00mL待测液于锥形瓶中,然后加入足量的FeCl3溶液,充分反应后,再加入M溶液作指示剂:
c.用0.2100mol·L-1的Na2S2O3标准溶液滴定至终点(反应方程式为;2Na2S2O3+I2=Na2S4O6+2NaI),重复实验多次,测得消耗标准溶液的体积为15.00mL。
①M为____________(写名称)。
②该样品中NaI的质量分数为_______________。
高三化学实验题中等难度题查看答案及解析
碘化钠在医疗及食品方面有重要的作用。实验室用NaOH、单质碘和水合肼(N2H·H2O)为原料制备碘化钠。已知:水合肼具有还原性。回答下列问题:
(1)水合肼的制备有关反应原理为:CO(NH2)2(尿素)+NaClO+2NaOHN2H4·H2O+NaCl+Na2CO3
①制取次氯酸钠和氧氧化钠混合液的连接顺序为__________(按气流方向,用小写字母表示)。

若该实验温度控制不当,反应后测得三颈瓶内ClO-与ClO3-的物质的量之比为5:1,则氯气与氢氧化钠反应时,被还原的氯元素与被氧化的氯元素的物质的量之比为________。
②制备水合肼时,应将___________滴到 __________ 中(填“NaClO溶液”或“尿素溶液”),且滴加速度不能过快。
(2)碘化钠的制备采用水合肼还原法制取碘化钠固体,其制备流程如图所示:
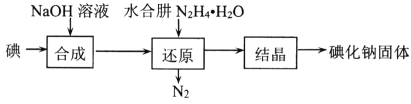
在“还原”过程中,主要消耗反应过程中生成的副产物IO3-,该过程的离子方程式为______________________________________。工业上也可以用硫化钠或铁屑还原碘酸钠制备碘化钠,但水合肼还原法制得的产品纯度更高,其原因是_________________________________。
(3)测定产品中NaI含量的实验步骤如下:
a.称取10.00g样品并溶解,在500mL容量瓶中定容;
b.量取25.00mL待测液于锥形瓶中,然后加入足量的FeCl3溶液,充分反应后,再加入M溶液作指示剂:
c.用0.2100mol·L-1的Na2S2O3标准溶液滴定至终点(反应方程式为;2Na2S2O3+I2=Na2S4O6+2NaI),重复实验多次,测得消耗标准溶液的体积为15.00mL。
①M为____________(写名称)。
②该样品中NaI的质量分数为_______________。
高三化学实验题中等难度题查看答案及解析