-
叶蜡石的化学式为X2 [Y4 Z10](ZW)2,短周期元素W、Z、X、Y的原子序数依次增大,X与Y为同一周期相邻元素,Y的最外层电子数为次外层的一半,X的离子与ZW-含有相同的电子数。下列说法错误的是 ( )
A.X的最高价氧化物可作耐火材料
B.常温常压下,Z和W形成的常见化合物均为液体
C.原子半径:X > Y > Z > W
D.可用NaOH溶液分离X单质和Y单质的混合物
高三化学单选题中等难度题查看答案及解析
-
叶蜡石是一种重要的化工原料,化学式为X2[Y4Z10](ZW)2,短周期元素W、Z、X、Y的原子序数依次增大,Y的最外层电子数为次外层的一半,X为地壳中含量最多的金属元素,X的离子与ZW-含有相同的电子数。下列说法不正确的是
A.原子半径:X>Y>Z>W B.最简单氢化物的沸点:Y>Z
C.Y的氧化物可作光导纤维的材料 D.常温常压下,Z和W形成的常见化合物均为液体
高三化学单选题简单题查看答案及解析
-
叶蜡石是一种重要的化工原料,化学式为X2[Y4Z10](ZW)2,X、Y、Z、W均为短周期元素,X与Y为同一周期相邻元素,Y的最外层电子数为次外层的一半,X 为地壳中含量最多的金属元素,X的离子与ZW-含有相同的电子数。下列说法正确的是
A. 原子半径:Y>X>Z>W
B. 最简单氢化物的沸点:Y>Z
C. X 与W形成的[XW4]-具有较强的还原性
D. 可用NaOH 溶液分离X、Y的最高价氧化物的混合物
高三化学单选题中等难度题查看答案及解析
-
叶蜡石是一种重要的化工原料,化学式为X2[Y4Z10](ZW)2,X、Y、Z、W均为短周期元素,X与Y为同一周期相邻元素,Y的最外层电子数为次外层的一半,X 为地壳中含量最多的金属元素,X的离子与ZW-含有相同的电子数。下列说法正确的是
A. 原子半径:Y>X>Z>W
B. 最简单氢化物的沸点:Y>Z
C. X 与W形成的[XW4]-具有较强的还原性
D. 可用NaOH 溶液分离X、Y的最高价氧化物的混合物
高三化学单选题中等难度题查看答案及解析
-
寿山石{X4[Y4Z10](ZW)8}的组成元素均为短周期元素,X的最高价氧化物对应水化物常用于治疗胃酸过多,X的简单离子与ZW- 含有相同的电子数,Y的单质是制造芯片的基础材料。下列说法正确的是( )
A. 简单氢化物的热稳定性:Y>Z B. 原子半径:Y>X >Z>W
C. 最高价氧化物水化物的酸性:X >Y D. NaW与水反应时作还原剂
高三化学单选题中等难度题查看答案及解析
-
寿山石{X4[Y4Z10](ZW)8}的组成元素均为短周期元素,X的最高价氧化物对应水化物常用于治疗胃酸过多,X的简单离子与ZW-含有相同的电子数,Y的单质是制造芯片的基础材料。下列说法正确的是()
A. 原子半径:Y>X >Z>W B. 最高价氧化物水化物的酸性:X >Y
C. NaW与水反应时作还原剂 D. 简单氢化物的热稳定性:Y>Z
高三化学单选题中等难度题查看答案及解析
-
[化学——物质结构与性质]前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A 元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2。
(1)六种元素中第一电离能最小的是 (填元素符号,下同),电负性最大的是 。
(2)黄血盐是由A、B、C、D四种元素形成的配位化合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式 ,1 mol AB-中含有π键的数目为 ,黄血盐晶体中各种微粒间的作用力不涉及 (填选项字母)。
a.离子键 b.共价键 c.配位键 d.金属键 e.氢键 f.分子间的作用力
(3)E2+的价层电子排布图为 ,很多不饱和有机物在E催化下可与H2发生加成反应:如①CH2=CH2、②HC≡CH、③
、④HCHO。其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明加成产物是何物质) 。

(4)金属C、F晶体的晶胞结构如图(请先判断对应的图),C、F两种晶体晶胞中金属原子的配位数之比为 。金属C的晶胞中,若设该晶胞的密度为a g/cm3,阿伏加德罗常数的值为NA,C原子的摩尔质量为M,则表示C原子半径的计算式为 cm。
高三化学简答题困难题查看答案及解析
-
[化学——选修3:物质结构与性质](15分)前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2。
(1)六种元素中第一电离能最小的是 (填元素符号,下同),电负性最大的是 。
(2)黄血盐是由A、B、C、D四种元素形成的配位化合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式 ,1 mol AB-中含有π键的数目为 ,黄血盐晶体中各种微粒间的作用力不涉及 (填序号)。
a.离子键
b.共价键
c.配位键
d.金属键
e.氢键
f.分子间的作用力
(3)E2+的价层电子排布图为 ,很多不饱和有机物在E催化下可与H2发生加成反应:如①CH2=CH2、②HC≡CH、③
、④HCHO。其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明加成产物是何物质) 。
(4)金属C、F晶体的晶胞结构如图(请先判断对应的图),C、F两种晶体晶胞中金属原子的配位数之比为 。金属C的晶胞中,若设该晶胞的密度为a g/cm3,阿伏加德罗常数的值为NA,C原子的摩尔质量为M,则表示C原子半径的计算式为 。
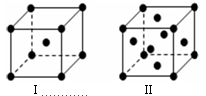
高三化学填空题极难题查看答案及解析
-
【化学–选修3:物质结构与性质】(15分)前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2。
(1)六种元素中第一电离能最小的是 (填元素符号,下同),电负性最大的是 。
(2)黄血盐是由A、B、C、D四种元素形成的配位化合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式 ,1 mol AB-中含有π键的数目为 ,黄血盐晶体中各种微粒间的作用力不涉及 (填序号)。
a.离子键
b.共价键
c.配位键
d.金属键
e.氢键
f.分子间的作用力
(3)E2+的价层电子排布图为 ,很多不饱和有机物在E催化下可与H2发生加成反应:如①CH2=CH2、②HC≡CH、③
、④HCHO。其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明加成产物是何物质) 。
(4)金属C、F晶体的晶胞结构如图(请先判断对应的图),C、F 两种晶体晶胞中金属原子的配位数之比为 。金属C的晶胞中,若设该晶胞的密度为a g/cm3,阿伏加得罗常数为NA,C原子的摩尔质量为M,则表示C原子半径的计算式为 。
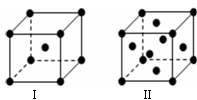
高三化学填空题极难题查看答案及解析
-
[化学——选修3:物质结构与性质] X、Y、Z、M、W、R是元素周期表中1~36号元素,且原子序数依次增大,X、Y、Z是位于同一周期的相邻元素,Y元素基态原子的2p轨道处于半充满状态;M为元素周期表1~36号元素中电负性最小的元素,W元素基态原子的价电子构型为3d74s2;R位于周期表第11列。回答下列问题(若需表示具体元素必须用相应的元素符号):
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是_____________(用元素符号表示),Y的最简单气态氢化物在水中的溶解度远大于X的最简单气态氢化物,主要原因是____________。
(2)R元素基态原子的电子排布式为_______。Z、M形成化合物M2Z2的电子式为_________。
(3)X、Z、W三种元素可以形成橘红色易升华的固体配合物W2(XZ)8,该配合物中提供空轨道的是_________,提供孤对电子的是__________________(填化学式)。
(4)已知某化合物部分结构如图(a)所示,该化合物由X、Y两元素组成,硬度超过金刚石。该化合物的化学式为_____,其晶体类型为______,晶体中X、Y两种元素原子的杂化方式均为___________。
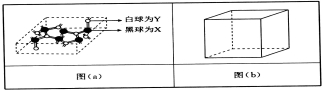
(5)在图(b)中标出R晶体中R原子的位置,该晶体中R原子直径为a pm,R的相对原子质量为M,阿伏加德罗常数为NA,该晶胞密度表达式为___________g·cm-3(用a,M,NA表示)。
高三化学简答题困难题查看答案及解析