-
(1)明矾净水原理___________________________________(离子方程式表示),胶体具有________________性。
(2)在25℃时,将pH=13的强碱与pH=2的强酸溶液混合,所得混合液的pH=11,则强碱与强酸的体积比为___________
(3)NH4Cl溶液显______________(填“酸性”、“中性”或“碱性”),理由是_________(用离子方程式或必要的文字说明).
(4)NaHCO3溶液中,下列表述正确的是_______
A.c(Na+) + c(H+)= c(HCO3﹣)+ c(CO32﹣)+ c(OH﹣)
B. c(OH﹣)= c(H2CO3)+ c(H+)-c(CO32﹣)
C.c(OH﹣)= c(HCO3﹣)+ c(H+)+c(H2CO3)
D.c (Na+)= c(HCO3﹣)+ c(CO32﹣) + c(H2CO3)
高二化学综合题中等难度题查看答案及解析
-
(5分)日常生活中,可用明矾作为净水剂,这是因为:明矾溶于水发生水解反应,生成氢氧化铝胶体。
(1)该反应的离子方程式为: ________。为更好地表示溶液的酸碱性,科学家提出了酸度(AG)的概念,
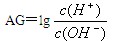 。
。(2)中性溶液的AG=________________ 。
(3)常温下,测得用明矾净化过的净水溶液PH=6,则溶液的 AG= ________ ,由水电离的c(H+)=________。
高二化学填空题简单题查看答案及解析
-
(5分)日常生活中,可用明矾[KAl(SO4)2·12H2O]作为净水剂,这是因为:明矾溶于水发生水解反应,生成氢氧化铝胶体。
(1)该反应的离子方程式为: ①。
为更好地表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG=lg[c(H+)/c(OH-)]。
(2)中性溶液的AG= ② 。
(3)常温下,测得用明矾净化过的净水溶液PH=6,则溶液的 AG=③,由水电离的c(H+)=④。
高二化学填空题中等难度题查看答案及解析
-
下列有关物质的应用与性质相对应的说法正确的有几个
①明矾能用于净水是因为铝离子水解生成的氢氧化铝胶体具有强氧化性
②氯化铁溶液可用于制作印刷电路板是因为其能氧化单质铜
③浓硫酸可用作干燥剂是因为其具有脱水性
④光导纤维可用作通讯材料是因为其具有导电性
⑤MgO、Al2O3的熔点很高,可制作耐高温材料
⑥NaHCO3能与碱反应,因此食品工业上用作焙制糕点的膨松剂
⑦Al具有良好的延展性和抗腐蚀性,可制成铝箔包装物品
A.2个 B.3个 C.4个 D.5个
高二化学选择题中等难度题查看答案及解析
-
化学与社会、生活密切相关。下列有关说法错误的是
A.明矾中铝离子水解产生的胶体具有很强的吸附作用而常用于净水
B.地球上99%以上的溴蕴藏在大海中,因此溴被称为“海洋元素”
C.目前加碘盐中添加的含碘物质是KI,可用氯水和淀粉溶液鉴定食盐是否加碘
D.为减少污染、提高燃烧效率,可将煤气化或液化获得清洁燃料
高二化学单选题简单题查看答案及解析
-
下列有关物质的应用与性质相对应的说法正确的有( )
①明矾能用于净水是因为铝离子水解生成的氢氧化铝胶体具有吸附性
②氯化铁溶液可用于腐蚀印刷电路板是因为其能氧化单质铜
③MgO、Al2O3的熔点很高,可制作耐高温材料
④NaHCO3能与碱反应,因此食品工业上可用作焙制糕点的膨松剂
⑤H2O2、SO2都能使酸性KMnO4褪色,是因为H2O2具有还原性,SO2具有漂白性
A. 2个 B. 3个 C. 4个 D. 5个
高二化学单选题简单题查看答案及解析
-
化学与生产、生活密切相关,下列说法不正确的是
A.用热的纯碱溶液去除油污
B.用Na2S处理废水中的Cu2+、Hg2+等重金属离子
C.明矾水解时产生具有吸附性的胶体粒子,可作净水剂
D.在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀
高二化学单选题简单题查看答案及解析
-
化学平衡移动原理在生产、生活、科研中有重要应用。
(1)生活中明矾[KAl(SO4)2·12H2O]常用作净水剂,其净水的原理是_____(用离子方程式表示)。
(2)工业上在850℃时用钠还原熔融态氯化钾的方法制备金属钾,发生的反应方程式为:Na(l) + KCl(l)
NaCl(l) + K(g),能制备钾的原因是_______。
(3)测得某工厂废水中含Cr2O72–的浓度为3.0×10–4 mol·L−1,常温下,对该有害离子的处理流程如下:{已知:绿矾的化学式为FeSO4·7 H2O, Ksp [Cr(OH)3]=6.0×10–31 }

① 步骤(Ⅰ)中发生反应的离子方程式为_________。
② 若忽略加入各种试剂后的废水体积变化,则Cr3+开始沉淀的pH为_________。
(4)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验。查阅资料:25℃时,Ksp (AgCl)=1.8×10–10,Ksp (AgI)=8.3×10–17。
操作步骤
现象
步骤1:向2 mL 0.1 mol·L−1AgNO3溶液中加入2 mL 0.1 mol·L−1 NaCl溶液,得到浊液a,过滤。
得滤液b和白色沉淀c
步骤2:向滤液b中滴加0.1 mol·L−1 KI溶液。
出现浑浊
步骤3:向白色沉淀c中滴加0.1 mol·L−1 KI溶液。
白色沉淀变为黄色
① 浊液a中存在沉淀溶解平衡(用方程式表示)______________。
② 用化学平衡原理解释步骤3中的实验现象_________。
高二化学综合题中等难度题查看答案及解析
-
弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡.根据要求回答问题
I、铝盐的水解原理在生活中应用广泛,如明矾常作净水剂,其净水的原理是_________(用离子方程式表示);如硫酸铝常作泡沫灭火器原料之一,其原理是________________(用离子方程式表示)。
II、5℃时,将0.01mol CH3COONa和0.002mol HCl溶于水,形成1L混合溶液:
(1)该溶液中存在着三个平衡体系,用电离方程式或离子方程式表示:
①____________________________;②____________________________;③____________________________。
(2)溶液中共有__________种不同的粒子(指分子和离子)。
(3)在这些粒子中,浓度为0.01mol·L-1的是__________,浓度为0.002mol·L-1的是____________。
(4)__________和__________两种粒子物质的量之和等于0.01mol。
(5)在0.5mol·L-1的NaHSO3溶液中滴入石蕊,溶液变红。试回答有关问题:
①该溶液中HSO
的电离程度_________(填“大于”、“小于”或“等于”)HSO
的水解程度。
②溶液中Na+、HSO3-、SO32-、H+、OH-、H2SO3、H2O等粒子的浓度由大到小的顺序为__________。
III、含Cr2O72﹣的废水毒性较大,某工厂废水中含5.0×10-3mol·L﹣1的Cr2O72﹣.为了使废水的排放达标,进行如下处理:
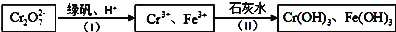
(1)绿矾为FeSO4·7H2O,反应(I)中FeSO4与Cr2O72﹣ 的物质的量之比为_________.
(2)常温下若处理后的废水中c(Cr3+)=6.0×10﹣7mol·L﹣1,则处理后的废水的pH=______.(Ksp[Cr(OH)3]=6.0×10﹣31)
高二化学综合题困难题查看答案及解析
-
(13分)弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。根据要求回答问题
(1)生活中明矾常作净水剂,其净水的原理是 (用离子方程式表示)。
(2)常温下,取0.2 mol·L-1 HCl溶液与0.2 mol·L-1 MOH溶液等体积混合,测得混合溶液后的pH=5。写出MOH的电离方程式: 。
(3)0.1mol/L的NaHA溶液中,测得溶液中的显碱性。则
①该溶液中c(H2A) c(A2-)(填“>”、“<”或“=”)。
②作出上述判断的依据是 (用文字解释)。
(4)含Cr2O
的废水毒性较大,某工厂废水中含5.0×10-3 mol·L-1的Cr2O
。为了使废水的排放达标,进行如下处理:
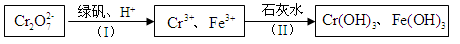
①绿矾为FeSO4·7H2O。反应(I)中Cr2O72-与FeSO4的物质的量之比为 。
②常温下若处理后的废水中c(Cr3+)=6.0×10-7 mol·L-1,则处理后的废水的pH=______。(Ksp[Cr(OH) 3]=6.0×10-31)
高二化学简答题困难题查看答案及解析