-
根据要求计算。
(1)0.5mol NaAlO2含有___mol Na+;_____mol AlO2-;含___个O。
(2)在100 mL 0.2 mol/L NaOH溶液中含溶质的物质的量___mol;配制50 mL 0.2 mol/LFeSO4溶液,需要FeSO4____ g。
(3)1.06 g的Na2CO3的物质的量是___mol;含有的CO32-离子数是___个。
(4)标准状况下,0.3 mol CH4的体积是___;含有碳原子质量是___;含有氢原子物质的量_____。
高一化学计算题中等难度题查看答案及解析
-
某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol·L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。请根据图像推断,下列说法中不正确的是(已知HCO3-与AlO2-在溶液中不能共存)
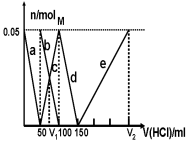
A.M点时生成的CO2为0 mol
B.原混合溶液中的CO32-与AlO2-的物质的量之比为1:2
C.V1:V2=1:4
D.a段表示的离子方程式为:AlO2- +H+ + H2O=Al(OH)3↓
高一化学选择题困难题查看答案及解析
-
设NA表示阿伏加德罗常数的数值,其计算近似值为6.02×1023。按要求完成下列填空:
(1)1 mol Cl2中含有________个氯气分子,约含有________个氯原子。
(2)0.5 mol NH3中含有________个氨分子,共约含有________个原子。
(3)3 mol NO和________mol NO2所含有的原子数相等。
(4)6mol H2O与________mol NH3所含氢子数相等。
(5)某硫酸钠溶液中含有3.01×1022个Na+,则该溶液中SO42-的物质的量是 ________。
(6)1.204×1024个水分子的物质的量是________。1molH2SO4中氧原子数为________。
(7)1molMgCl2中氯离子数为________,离子总数约为________。
(8)1mol CuSO4·5H2O含有________个Cu2+,含有_____mol水分子。
(9)2molCO(NH2)2中含________mol碳原子,________mol氧原子,________mol氮原子,___mol氢原子。
高一化学填空题中等难度题查看答案及解析
-
设用NA表示阿伏加德罗常数的值,其计算近似值为6.02×1023,按要求完成下列填空:
(1)0.5 mol NH3共含有_______________个原子。
(2)6 mol H2O与标准状况下_____________L NH3所含氢原子数相等。
(3)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO42﹣的物质的量是_________________。
(4)标准状况下11.2 L NO和__________________g NO2所含有的氧原子数相等。
(5)8 g某物质含有3.01×1023个分子,该物质的相对分子质量约为__________________。
高一化学计算题中等难度题查看答案及解析
-
向Na2CO3、NaAlO2的混合溶液中逐滴加入1 mol·L-1的盐酸,测得溶液中的HCO3-、CO32-、AlO2-、Al3+离子的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是( )

A.原混合溶液中的CO32-与AlO2-的物质的量之比为1∶2
B.V1∶V2=1∶5
C.M点时生成的CO2为0.05 mol
D.e曲线表示的离子方程式为Al(OH)3+3H+===Al3++3H2O
高一化学选择题极难题查看答案及解析
-
含Na2CO3、NaAlO2的混合溶液中逐滴加入150 mL 1mol·L−1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是

A. a曲线表示的离子方程式为:AlO2-+H++H2O===Al(OH)3↓
B. b和c曲线表示的离子反应是相同的
C. M点时,溶液中沉淀的质量为3.9g
D. 原混合溶液中的CO32-与AlO2-的物质的量之比为1∶2
高一化学单选题困难题查看答案及解析
-
含Na2CO3、NaAlO2的混合溶液中逐滴加入150 mL 1mol·L−1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是

A. a曲线表示的离子方程式为:AlO2-+H++H2O===Al(OH)3↓
B. b和c曲线表示的离子反应是相同的
C. M点时,溶液中沉淀的质量为3.9g
D. 原混合溶液中的CO32-与AlO2-的物质的量之比为1∶2
高一化学单选题困难题查看答案及解析
-
下列溶液中,Na+ 物质的量浓度最大的是( )
A.1mL 0.5mol·L-1的NaAlO2溶液 B.100mL 0.01 mol·L-1的NaCl溶液
C.10mL 0.1mol·L-1的NaOH溶液 D.100mL 0.1mol·L-1的Na2SO3溶液
高一化学选择题中等难度题查看答案及解析
-
按要求填空:
(1)0.5 mol SO2共约含有 个原子,它与 g SO3所含硫原子数相等。
(2)有100mL 0.2 mol/L 的NaOH溶液,将此溶液稀释到200 mL,则稀释后溶液中Na+的物质的量浓度是 。
(3)相同条件下,相同体积的 ①HCl、②NH3、③CO2、④O2四种气体中,含有电子数目由小到大的是(填序号) 。
高一化学填空题中等难度题查看答案及解析
-
按要求填写下列空白(NA表示阿伏德罗常数的值)
(1) 0.5mol SO42- 中的质子数为 _____ ;电子数为 __________含有9.6克SO42- 的(NH4)2SO4固体中,含氢原子数为_________
(2)标准状况下,4.48L NH3的质量是_________,含有电子的个数是_________
(3) 含氢原子为0.2×6.02×1024个的NH4HCO3 ,其质量是___________,其中含氧原子的物质的量为_________
(4) 在200mL 3mol/L 的K2SO4的溶液中,溶质物质的量为________, K+的物质的量浓度为_________
(5)含0.6NA个氧原子的SO2中, SO2的物质的量是_________氧元素的质量为_________
(6)在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,此混合物中CO和CO2物质的量之比是________,混合气体的平均相对分子质量是________
高一化学填空题中等难度题查看答案及解析