-
25 ℃时,几种常见弱酸的Ka如下表所示[已知草酸(H2C2O4)是一种二元弱酸]:
| 弱酸 | H2C2O4 | CH3COOH | HCN | H2CO3 |
| Ka | K1=5.6×10-2 K2=5.4×10-5 | 1.8×10-5 | 6.2×10-10 | K1=4.2×10-7 K2=5.6×10-11 |
(1)25 ℃时,0.1 mol·L-1的Na2C2O4、CH3COONa、NaCN、Na2CO3溶液的pH由大到小的顺序是________________________,中和等体积等pH的CH3COOH和HCN溶液消耗NaOH的物质的量________(填“前者大”或“后者大”)。
(2)KHC2O4溶液呈酸性。向10 mL 0.01 mol·L-1的H2C2O4溶液滴加0.01 mol·L-1KOH溶液V(mL),回答下列问题:
①当V<10 mL时,反应的离子方程式为________________________________。
②当V=10 mL时,溶液中HC2O 、C2O
、C2O 、H2C2O4、H+的浓度从大到小的顺序为_____________________。
、H2C2O4、H+的浓度从大到小的顺序为_____________________。
③当V=amL时,溶液中离子浓度有如下关系:c(K+)=2c(C2O )+c(HC2O
)+c(HC2O );当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(C2O
);当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(C2O )+c(HC2O
)+c(HC2O )+c(H2C2O4);则a________(填“<”“=”或“>”)b。
)+c(H2C2O4);则a________(填“<”“=”或“>”)b。
④当V=20 mL时,再滴入NaOH溶液,则溶液中n(K+)/n(C2O )的值将________(填“变大”“变小”或“不变”)。
)的值将________(填“变大”“变小”或“不变”)。
-
草酸(H2C2O4)是二元弱酸,25℃时,H2C2O4:K1=5.4×10-2,K2=5.4×10-5;H2CO3:K1=4.5×10-7,K2=4.7×10-11。
(1)KHC2O4溶液呈__________性(填“酸”、“中”或“碱”)。
(2)下列化学方程式可能正确的是________。
A.
B.
C.
D.
(3)常温下,向10 mL 0.01 mol·L-1H2C2O4溶液中滴加0.01 mol·L-1的KOH溶液V mL,回答下列问题:
①当V<10时,反应的离子方程式为______________________________________________。
②若溶液中离子浓度有如下关系:c(K+)=2c(C2O42-)+c(HC2O4-),则pH______7(填“>”“<”或“=”),V________10(填“>”“<”或“=”)。
③当溶液中离子浓度有如下关系:c(K+)=c(C2O42-)+c(HC2O4-)+c(H2C2O4),则溶液中溶质为____________,V________10(填“>”、“<”或“=”)。
④当V=20时,溶液中HC2O4-、C2O42-、H2C2O4、OH-的物质的量浓度从大到小的顺序为____________________________________________________________________________________。
-
已知草酸(H2C2O4)是一种二元弱酸,主要用作还原剂和漂白剂。
(1)草酸的电离方程式为 。
(2)将草酸溶液与酸性高锰酸钾溶液混合发生的反应为:
MnO4-+ H2C2O4+ → Mn2+ + CO2↑+ H2O
某合作小组同学在烧杯中进行上述反应时,发现刚开始一段时间,反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。
①配平上述离子方程式
②该实验不久后溶液突然褪色的原因最有可能是 。
A.体系压强增大 B.反应物接触面积增大
C.生成物对反应有催化作用 D.反应物浓度增大
(3)为研究该化学反应速率的影响因素,某同学进行了以下实验:
| 组别 | 温度/℃ | V(H2C2O4) /mL | V(KMnO4) /mL | V(H2O) /mL | KMnO4溶液 褪色时间/s |
| 1 | 30 | 10 | 10 | 20 | 40 |
| 2 | 30 | 20 | 20 | 0 | t |
| 3 | 30 | | | 15 | |
①对比实验1和3要研究改变反应物浓度对化学反应速率的影响,请完成表格中横线。
②实验2中溶液褪色时间t 为
A.>40 B.=40 C.<40 D.无法判断
-
I. 乙二酸俗称草酸,是一种二元弱酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料,常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如下表所示,请填空:
| H2C2O4 | KHC2O4 | K2C2O4 |
| pH | 2.1 | 3.1 | 8.1 |
(1)KHC2O4溶液呈酸性的原因是_____________________________。
(2)向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是___________(填字母代号)。
A. c(K+)=c(HC2O4)+c(H2C2O4)+c(C2O42-) B. c(Na+)=c(H2C2O4)+c(C2O42-)
C. c(K+)+c(Na+)=c(HC2O4-)+c(C2O42-) D. c(K+)>c(Na+)
II.电离平衡常数是衡量弱电解质电离程度的量。已知如下表数据(25℃):
| 化学式 | 电离平衡常数 |
| HCN | K=4.9×10-19 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.4×10-7,K2=4.7×10-11 |
(3)25℃时,等浓度的三种溶液:A. NaCN溶液、B. Na2CO3溶液、C. CH3COONa溶液的pH由大到小的顺序为_________(填写字母代号)。
(4)25℃时,向NaCN溶液中通入少量CO2,所发生反应的离子方程式为_________________。
(5)现有浓度为0.02mol/L的HCN溶液与0.01mol/LNaOH溶液等体积混合之后(忽略混合过程中溶液体积的改变),测得c(Na+)>c(CN-),下列关系正确的是(_______)
A. c(H+)>c(OH-) B. c(H+)<c(OH-)
C. c(H+)+c(HCN)=c(OH-) D. c(HCN)+c(CN-)=0.01mol/L
-
已知草酸为二元弱酸:H2C2O4⇌HC2O4-+H+ Ka1;HC2O4-⇌C2O42-+H+ Ka2。常温下,向某浓度的草酸溶液中逐滴加入一定物质的量浓度的KOH溶液,所得溶液中H2C2O4、HC2O4—、C2O42−三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法不正确的是( )
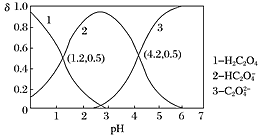
A.pH=1.2的溶液中:c(K+)+c(H+)=c(OH−)+c(H2C2O4)
B.pH=2.7的溶液中: =1000
=1000
C.向pH=1.2的溶液中加KOH溶液,将pH增大至4.2的过程中水的电离度一定增大
D.将相同物质的量的KHC2O4和K2C2O4固体完全溶于水所得混合液的pH为4.2
-
已知草酸为二元弱酸:H2C2O4 HC2O+H+ Ka1、HC2O
HC2O+H+ Ka1、HC2O C2O
C2O +H+ Ka2。常温下,向某浓度的H2C2O4溶液中逐滴加入一定浓度的KOH溶液,所得溶液中H2C2O4、HC2O、C2O
+H+ Ka2。常温下,向某浓度的H2C2O4溶液中逐滴加入一定浓度的KOH溶液,所得溶液中H2C2O4、HC2O、C2O 三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是( )
三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是( )
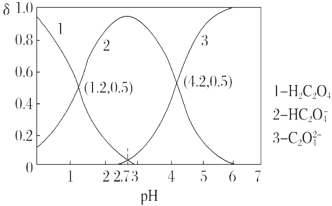
A. Ka1=10-1.2
B. pH=2.7时溶液中: =1000
=1000
C. 将相同物质的量的KHC2O4和K2C2O4固体完全溶于水便是配得pH为4.2的混合液
D. 向pH=1.2的溶液中加KOH溶液,将pH增大至4.2的过程中水的电离程度一直增大
-
已知草酸为二元弱酸:H2C2O4 HC2O+H+ Ka1、HC2O
HC2O+H+ Ka1、HC2O C2O
C2O +H+ Ka2。常温下,向某浓度的H2C2O4溶液中逐滴加入一定浓度的KOH溶液,所得溶液中H2C2O4、HC2O、C2O
+H+ Ka2。常温下,向某浓度的H2C2O4溶液中逐滴加入一定浓度的KOH溶液,所得溶液中H2C2O4、HC2O、C2O 三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是( )
三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是( )
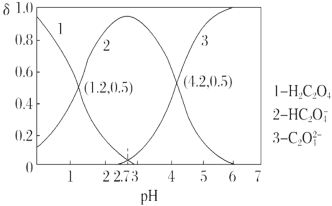
A. Ka1=10-1.2
B. pH=2.7时溶液中: =1000
=1000
C. 将相同物质的量的KHC2O4和K2C2O4固体完全溶于水便是配得pH为4.2的混合液
D. 向pH=1.2的溶液中加KOH溶液,将pH增大至4.2的过程中水的电离程度一直增大
-
已知H2C2O4是二元弱酸,室温下向某浓度的草酸溶液中逐滴加入KOH 溶液,所得溶液中H2C2O4、HC2O4-、C2O42-的组成百分率与pH的关系如图所示,下列说法正确的是
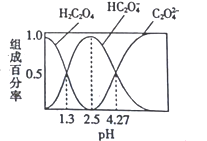
A. pH=4.27的溶液中:c(K+)+c(H+)=c(OH-)+3c(C2O42-)
B. 反应HC2O4-+H2O H2C2O4+OH-的平衡常数为10-4.27
H2C2O4+OH-的平衡常数为10-4.27
C. 向溶液中加入KOH溶液将pH 由1.3 调至4.27 的过程中水的电离程度先增大后减小
D. pH=2.5 的溶液中:c(H+)+2c(H2C2O4)=c(OH-)+c(C2O42-)
-
草酸(H2C2O4)是二元弱酸(K1=5.9×10-2、K2=6.4×10-5)。向10mL稀H2C2O4溶液中滴加等浓度NaOH溶液,H2C2O4、HC2O4-、C2O42-的浓度分数δ随溶液pH变化的关系如下图,以下说法正确的是( )
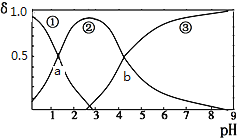
A. HC2O4-的浓度分数随pH增大而增大
B. 交点a处对应加入的NaOH溶液的体积为5mL
C. 交点b处c(H+)=6.4×10-5
D. pH=5时存在c(Na+)+c(H+)=c(C2O42-)+c(HC2O4-)+c(OH-)
-
草酸(H2C2O4)是二元弱酸(K1=5.9×10-2、K2=6.4×10-5)。向10mL稀H2C2O4溶液中滴加等浓度NaOH溶液,H2C2O4、HC2O4-、C2O42-的浓度分数δ随溶液pH变化的关系如下图,以下说法正确的是( )
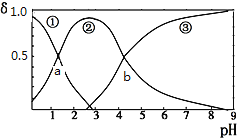
A. HC2O4-的浓度分数随pH增大而增大
B. 交点a处对应加入的NaOH溶液的体积为5mL
C. 交点b处c(H+)=6.4×10-5
D. pH=5时存在c(Na+)+c(H+)=c(C2O42-)+c(HC2O4-)+c(OH-)
、C2O
、H2C2O4、H+的浓度从大到小的顺序为_____________________。
)+c(HC2O
);当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(C2O
)+c(HC2O
)+c(H2C2O4);则a________(填“<”“=”或“>”)b。
)的值将________(填“变大”“变小”或“不变”)。


 =1000
=1000
 =1000
=1000

