-
氨是重要的工业原料,在农业、医药、国防和化工等领域有重要应用。
I.(1)工业上用N2和H2在一定条件下合成氨,下列措施能使正反应速率增大,且使平衡混合物中NH3的体积分数一定增大的是________。
A.降低反应温度 B.压缩反应混合物 C.充入N2 D.液化分离NH3
(2)常温下向100mL0.2mo/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。
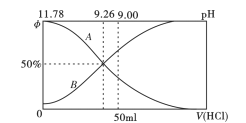
①表示NH3·H2O浓度变化的曲线是__________(填“A”或“B")。
②NH3·H2O的电离常数为_______(已知lg1.8 = 0.26)。
③当加入盐酸体积为50ml时,溶被中c(NH4+)- c(NH3·H2O) =_____mol/L (用数字表示)。
Ⅱ.若液氨中也存在类似水的电离( H2O+H2O H3O+ +OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
H3O+ +OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
(1)写出液氨的电离方程式_________.
(2)写出碳酸钠溶于液氨后第一级氨解的离子方程式__________
(3)写出碳酸钠的液氨溶液中各离子浓度的大小关系____________
-
氨是重要的工业原料,在农业、医药、国防和化工等领域有重要应用。
I(1)工业上用N2和H2在一定条件下合成氨,下列措施能使正反应速率增大,且一定使平衡混合物中NH3的体积分数增大的是________。
A.降低反应温度 B.压缩反应混合物 C.充入N2 D.液化分离NH3
(2)常温下,向100mL0.2mol/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中NH4+和NH3∙H2O的物质的量分数与加入盐酸的体积的关系如图所示,根据图像回答下列问题。
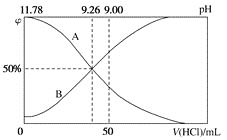
①表示NH3∙H2O浓度变化的曲线是________(填“A”或“B”)。
②NH3∙H2O的电离常数为________(已知lg1.8=0.26)。
③当加入盐酸体积为50mL时,溶液中c(NH4+)-c(NH3∙H2O)=________mol/L(用数字表示)。
II若液氨中也存在类似水的电离(H2O+H2O⇌H2O++OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
(3)写出液氨的电离方程式:____________________________。
(4)写出碳酸钠溶于液氨后第一级氨解的离子方程式:___________________。
(5)写出碳酸钠的液氨溶液中各离子浓度的大小关系:________________。
-
氨是重要的工业原料,在农业、医药、国防和化工等领域有重要应用。
(1)氨气的电子式为___,它的共价键属于___(填“极性”或“非极性”)键,其溶于水显碱性的理由是(用化学方程式表示)___。
(2)工业上用N2和H2在一定条件下合成氨,下列措施能使正反应速率增大,且一定使平衡混合物中NH3的体积分数增大的是___。
A.降低反应温度 B.压缩反应混合物 C.充入N2 D.液化分离NH3
(3)常温下,向100mL0.2mol/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O的物质的量分数与加入盐酸的体积的关系如图所示。

表示NH3·H2O浓度变化的曲线是___(填“A”或“B”)。
(4)当加入盐酸体积为50mL时,溶液中c(NH4+)-c(NH3·H2O)=___mol/L(用数字表示)。若液氨中也存在类似水的电离(H2O+H2O H3O++OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
H3O++OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
①写出液氨的电离方程式:___。
②写出碳酸钠溶于液氨后第一级氨解的离子方程式:___。
③写出碳酸钠的液氨溶液中各离子浓度的大小关系:___。
-
甲醇是有机化工原料合优质燃料,主要应用于精细化工、塑料等领域,也是农药、医药的重要原料之一。回答下列问题。
(1)工业上可用CO2和H2反应合成甲醇。
已知25℃、101kPa下: ①CO(g) +3H2(g)=CH3OH(l) +H2O(1) △H1=-132kJ• mol-1
②2H2(g) +O2(g)==2H2O(g) △H2= -484 kJ• mol-1
③H2O(l)= H2O(g) △H3= + 44 kJ• mol-1写出表示CH3OH燃烧热的热化学方程式:_______________。
(2)合成甲醇所需的H2可由下列反应制取:H2O(g)+CO(g) H2 (g)+CO2(g) △H<0。
H2 (g)+CO2(g) △H<0。
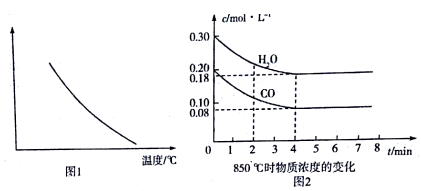
①在恒容密闭容器中.通入一定设的CO和H2O(g)发生上述反应,图1所示的是该反应的相关量值随溫度变化的情况,下列量值符合图示的是_______。
a.平衡常数 b.反应物的平衡转化率 c.逆反应速率 d. H2O(g)的平衡浓度
②850℃时,若通入一定量的CO和H2O(g)发生上述反应,CO和H2O(g)浓度变化如图2所示,达到平衡时H2O(g)的转化率为 ___________,该条件下的平衡常数K=___________。
(3)CO和H2反应也能合成甲醇:CO(g) +2 H2 (g) CH3OH(g) △H = -90 kJ• mol-1。恒容条件下,能使反应体系中增大的措施有_________ (任写两种)。
CH3OH(g) △H = -90 kJ• mol-1。恒容条件下,能使反应体系中增大的措施有_________ (任写两种)。
(4) 甲醇在催化剂条件下可以直接被氧化成甲酸。常温下,甲酸的电离常数Ka =1.0×10-4,20.00mL0.100 0mol·L-1NaOH溶液与等体积一定浓度的甲酸溶液混合,所得溶液中 c(HCOOH) = c(HCOO-) , c(OH-) =_______,溶液中离子浓度由大到小的顺序为_______。
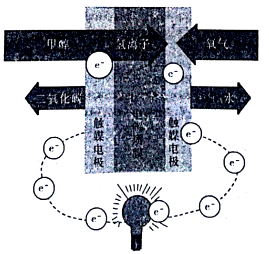
(5)甲醇燃料电池(如图所示)是质子交换膜燃料电池的一种变种,它直接使用甲醇而无须预先重整。写出在该条件下,甲醇燃料电池的负极反应式:_______________。
-
H2O2俗名双氧水,广泛应用于医药、国防、工业、农业、化工等领域中。H2O2易分解,需加入一定量的尿素、乙酰苯胺等有机物作为稳定剂。测定H2O2含量的常用方法有碘量法、高锰酸钾法、硫酸铈法等。回答下列问题:
(1)碘量法是将过量的KI溶液加入H2O2样品中,然后加入指示剂,用0.10mol•L-1Na2S2O3标准溶液滴定(发生反应:I2+2S2O32-=S4O62-+2I-)。滴定时所用指示剂为___;若某次滴定过程中消耗标准溶液12.50mL,则该过程中转移的电子为__mol。
(2)高锰酸钾法是用酸性KMnO4溶液滴定H2O2样品以测定其含量,写出反应的离子方程式:___;高锰酸钾法虽操作简单,但测定误差较大。某科研工作者对大量测定结果进行分析,发现94%的结果超过实际含量,主要原因是__(不考虑KMnO4的分解及实验操作误差)。
(3)硫酸铈法测定H2O2的含量:取H2O2样品1.00mL,稀释为250.00mL,取上述稀释过的H2O2溶液25.00mL于锥形瓶中,加入适量稀硫酸和2~3滴Fe2+-邻菲罗啉混合指示剂,摇匀后,用0.08mol•L-1Ce(SO4)2标准溶液滴定至终点(到达终点时Ce元素显+3价)。重复测定2~3次,平均消耗标准溶液22.08mL,则该H2O2样品的质量浓度为___g•L-1(结果保留1位小数);若未用Ce(SO4)2标准溶液润洗滴定管,会造成测定结果___(填“偏高”或“偏低”)。
-
甲醇是有机化工原料和优质燃料,主要应用于精细化工、塑料等领域,也是农药、医药的重要原料之一。回答下列问题:
(1)工业上利用CO2和H2反应合成甲醇。已知25℃ 101kPa下:
H2(g)+ O2(g)═H2O(g) △H=﹣242kJ•mol﹣1
O2(g)═H2O(g) △H=﹣242kJ•mol﹣1
CH3OH(g)+ O2(g)=CO2(g)+2H2O(g)△H2=﹣676kJ•mol﹣1
O2(g)=CO2(g)+2H2O(g)△H2=﹣676kJ•mol﹣1
①写出CO2和H2反应生成CH3OH(g)与H2O(g)的热化学方程式______
②下列表示该合成甲醇反应的能量变化示意图中正确的是______(填字母)
a. 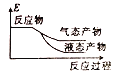 b.
b. 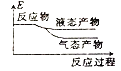 c.
c. 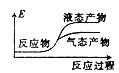 d.
d. 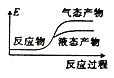
③合成甲醇所需的H2可由下列反应制取:H2O(g)+CO(g)⇌H2(g)+CO2(g),某温度下该反应的平衡常数K=1,若起始时c(CO)=1mol•L﹣1,c(H2O)=2mol•L﹣1,则达到平衡时H2O的转化率为______
(2)CO和H2反应也能合成甲醇:CO(g)+2H2(g)⇌CH3OH(g)△H=﹣90.1kJ•mol﹣1,在250℃下,将一定量的CO和H2投入10L的恒容密闭容器中,各物质浓度(mol•L﹣1)变化如下表所示(前6min没有改变条件)
| 2min | 4min | 6min | 8min | |
| CO | 0.07 | 0.06 | 0.06 | 0.05 | …… |
| H2 | x | 0.12 | 0.12 | 0.2 | …… |
| CH3OH | 0.03 | 0.04 | 0.04 | 0.05 | …… |
①x=______,250℃时该反应的平衡常数K=______
②若6~8min时只改变了一个条件,则改变的条件是______,第8min时,该反应是否达到平衡状态?______(填“是”或“不是”)
③该合成反应的温度一般控制在240~270℃,选择此温度的原因是:
Ⅰ.此温度下的催化剂活性;
Ⅱ.______
(3)甲醇在催化剂条件下可以直接氧化成甲酸,在常温下,20.00mL 0.1000mol•L﹣1NaOH溶液与等体积、等浓度甲酸溶液混合后所得溶液的pH______(填“<”“>”或“=”)原因是______(用离子方程式表示)
-
过氧化尿素是一种新型漂泊、消毒剂,广泛应用与农业、医药、日用化工等领域。用低浓度的双氧水和饱和尿素溶液在一定条件下可以合成过氧化尿素。反应的方程式为:
CO(NH2)2+H2O2 CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
| 分子式 | 外观 | 热分解温度 | 熔点 | 溶解性 |
| CO(NH2)2·H2O2 | 白色晶体 | 45℃ | 75~85℃ | 易溶于水、有机溶剂 |
合成过氧化尿素的流程及反应装置图如图:
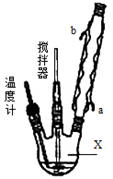
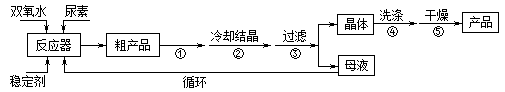
请回答下列问题:
(1)仪器X的名称是__________;冷凝管中冷却水从____(填“a”或“b”)口出来;
(2)该反应的温度控制30℃而不能过高的原因是_______________________。
(3)步骤①宜采用的操作是_____________。
A.加热蒸发 B.常压蒸发 C.减压蒸发
(4)若实验室制得少量该晶体,过滤后需要用冷水洗涤,具体的洗涤操作是_________________。
(5)准确称取1.000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加2mL6mol·L﹣1H2SO4,用0.2000mol·L﹣1KMnO4标准溶液滴定至终点时消耗18.00mL(尿素与KMnO4溶液不反应),则产品中CO(NH2)2·H2O2的质量分数为_____________;若滴定后俯视读数,则测得的过氧化尿素含量________(填“偏高”、“偏低”或“不变”)。
-
过氧化尿素是一种新型漂泊、消毒剂,广泛应用与农业、医药、日用化工等领域。用低浓度的双氧水和饱和尿素溶液在一定条件下可以合成过氧化尿素。反应的方程式为:
CO(NH2)2+H2O2 CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
| 分子式 | 外观 | 热分解温度 | 熔点 | 溶解性 |
| CO(NH2)2·H2O2 | 白色晶体 | 45℃ | 75~85℃ | 易溶于水、有机溶剂 |
合成过氧化尿素的流程及反应装置图如图:
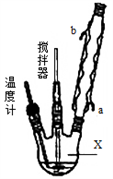
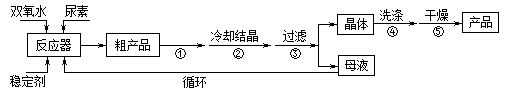
请回答下列问题:
(1)仪器X的名称是__________;冷凝管中冷却水从____(填“a”或“b”)口出来;
(2)该反应的温度控制30℃而不能过高的原因是_______________________。
(3)步骤①宜采用的操作是_____________。
A.加热蒸发 B.常压蒸发 C.减压蒸发
(4)若实验室制得少量该晶体,过滤后需要用冷水洗涤,具体的洗涤操作是_________________。
(5)准确称取1.000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加2mL6mol·L﹣1H2SO4,用0.2000mol·L﹣1KMnO4标准溶液滴定至终点时消耗18.00mL(尿素与KMnO4溶液不反应),则产品中CO(NH2)2·H2O2的质量分数为_____________;若滴定后俯视读数,则测得的过氧化尿素含量________(填“偏高”、“偏低”或“不变”)。
-
过氧化尿素是一种新型漂泊、消毒剂,广泛应用与农业、医药、日用化工等领域。用低浓度的双氧水和饱和尿素溶液在一定条件下可以合成过氧化尿素。反应的方程式为:
CO(NH2)2+H2O2 CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
| 分子式 | 外观 | 热分解温度 | 熔点 | 溶解性 |
| CO(NH2)2·H2O2 | 白色晶体 | 45℃ | 75~85℃ | 易溶于水、有机溶剂 |
合成过氧化尿素的流程及反应装置图如图:
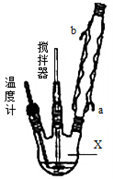
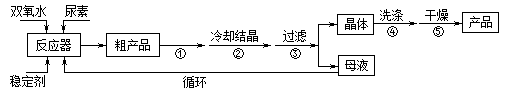
请回答下列问题:
(1)仪器X的名称是__________;冷凝管中冷却水从____(填“a”或“b”)口出来;
(2)该反应的温度控制30℃而不能过高的原因是_______________________。
(3)步骤①宜采用的操作是_____________。
A.加热蒸发 B.常压蒸发 C.减压蒸发
(4)若实验室制得少量该晶体,过滤后需要用冷水洗涤,具体的洗涤操作是_________________。
(5)准确称取1.000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加2mL6mol·L﹣1H2SO4,用0.2000mol·L﹣1KMnO4标准溶液滴定至终点时消耗18.00mL(尿素与KMnO4溶液不反应),则产品中CO(NH2)2·H2O2的质量分数为_____________;若滴定后俯视读数,则测得的过氧化尿素含量________(填“偏高”、“偏低”或“不变”)。
-
过氧化尿素是一种新型漂白、消毒剂,广泛应用于农业、医药、日用化工等领域。用低浓度的双氧水和饱和尿素溶液在一定条件下可以合成过氧化尿素:反应的方程式为:
CO(NH2)2+H2O2 CO(NH)2·H2O2。过氧化尿素的部分性质如下:
CO(NH)2·H2O2。过氧化尿素的部分性质如下:
合成过氧化尿素的流程及反应装置图如下:
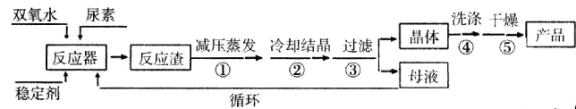
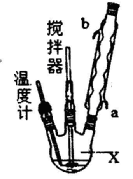
请回答下列问题:
(1)仪器X的名称是____________;冷凝管中冷却水从____________(填“a”或“b”)口进入。
(2)反应器的加热方式是_______________。
(3)搅拌器是否可用铁质材料___________(填“是”或“否”),原因是_______________。
(4)步骤① 采用减压蒸发的原因是___________。
(5)下列选项中,最适合作为步骤④ 的洗涤液是_______。
a.冰水 b.热水 c.饱和NaCl溶液 d.酒精和水的混合液
(6)准确称取0.5000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加1mL 6mol/L H2SO4,用0.1000 mol/L KMnO4标准溶液滴定至终点时消耗20.00mL(尿素与KMnO4溶液不反应)。
① 滴定终点的现象是______________。
② 则产品中CO(NH)2·H2O2的质量分数为______________。
③ 若滴定前仰视,滴定后俯视,则测得的过氧化尿素含量_________(填“偏高”、“偏低”或“不变”)。

H3O++OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。




 b.
b.  c.
c.  d.
d. 








