-
1mol碳在氧气中完全燃烧生成气体,放出393kJ的热量,下列热化学方程式表示正确的是
A.C(s)+O2(g)→CO2(g)+393kJ
B.C + O2→ CO2+393kJ
C.C (s) + O2 (g)→CO2 (g)-393kJ
D.C (s) +1/2O2 (g) → CO(g) +393kJ
高三化学单选题中等难度题查看答案及解析
-
1mol碳在氧气中完全燃烧生成气体,放出393kJ的热量,下列热化学方程式表示正确的是
A. C(s)+O2(g)→CO2(g)+393kJ
B. C + O2→ CO2+393kJ
C. C (s) + O2 (g)→CO2 (g)-393kJ
D. C (s) +1/2O2 (g) → CO(g) +393kJ
高三化学选择题中等难度题查看答案及解析
-
根据能量变化示意图得出的结论正确的是( )
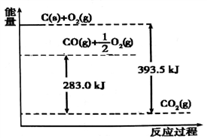
A. 1mol C完全燃烧生成CO2时放出的热量为393.5 kJ/mol
B. 2C(s)+O2(g)=2CO(g) △H=-221.0 kJ/mol
C. 2CO2 (g)=2CO(g)+O2(g) △H=+283.0 kJ/mol
D. C(s)+O2(g)= CO2 (g) △H=+393.5 kJ/mol
高三化学选择题中等难度题查看答案及解析
-
已知w g液态苯(C6H6)完全燃烧生成2 mol CO2气体和1 mol液态水,并放出m kJ的热量,下列能正确表示苯燃烧热的热化学方程式的是( )
A. 2C6H6(l)+15O2(g) ===12CO2(g)+6H2O(l) ΔH=-2m kJ·mol-1
B.
C6H6(l)+
O2(g)===2CO2(g)+H2O(g) ΔH=-m kJ·mol-1
C. C6H6(l)+
O2(g)===6CO2(g)+3H2O(g) ΔH=-m kJ·mol-1
D. C6H6(l)+
O2(g)===6CO2(g)+3H2O(l) ΔH=-3m kJ·mol-1
高三化学选择题中等难度题查看答案及解析
-
已知w g液态苯(C6H6)完全燃烧生成2 mol CO2气体和1 mol液态水,并放出m kJ的热量,下列能正确表示苯燃烧热的热化学方程式的是( )
A. 2C6H6(l)+15O2(g)===12CO2(g)+6H2O(l) ΔH=-2m kJ·mol-1
B.
C6H6(l)+
O2(g)===2CO2(g)+H2O(l) ΔH=-m kJ·mol-1
C. C6H6(l)+
O2(g)===6CO2(g)+3H2O(l) ΔH=-m kJ·mol-1
D. C6H6(l)+
O2(g)===6CO2(g)+3H2O(l) ΔH=-3m kJ·mol-1
高三化学选择题简单题查看答案及解析
-
1mol氢气在氧气中完全燃烧生成水蒸气放出241.8千焦热量,下列热化学方程式正确的是
A. 2H2(g)+O2(g)→2H2O(g)+241.8kJ B. H2(g)+1/2O2(g)→H2O(g)+ 241.8 kJ
C. H2(g)+1/2O2(g)→H2O(g)-241.8 kJ D. H2(g)+1/2O2(g)→H2O(l)+241.8 kJ
高三化学单选题简单题查看答案及解析
-
已知25 ℃、101 kPa下,1 mol石墨完全燃烧生成CO2放出393.51 kJ热量、1 mol金刚石完全燃烧生成CO2放出395.41 kJ热量。据此判断,下列说法正确的是( )
A.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低
B.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的高
C.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低
D.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的高
高三化学选择题简单题查看答案及解析
-
已知2H2(g)+O2(g)=2H2O(g)+483.6kJ。下列说法正确的是( )
A.1mol氢气完全燃烧生成液态水放出的热量小于241.8KJ
B.1mol水蒸气完全分解成氢气与氧气,需吸收241.8kJ热量
C.2mol氢气与1mol氧气的总能量小于2mol 水蒸气的总能量
D.2mol氢氢键和1mol氧氧键拆开所消耗的能量大于4mol氢氧键成键所放出的能量
高三化学单选题简单题查看答案及解析
-
(1)在298K时,1mol C2H6 在氧气中完全燃烧生成CO2和液态水,放出热量1558.3kJ。写出该反应的热化学方程式。
(2)利用该反应设计一个燃料电池:用KOH溶液作电解质溶液,多孔石墨作电极,在电极上分别通入乙烷和氧气。通入乙烷气体的电极应为________极(填“正”或“负”),该电极上发生的电极反应式为________。
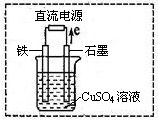
(3)在右图所示实验装置中,石墨棒上的电极反应式为________。如果起始时盛有1L pH=5的CuSO4溶液(25℃,CuSO4足量),一段时间后溶液的pH变为1,此时可观察到的现象是________。若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入________(填物质名称),其质量约为________。
(4)将普通碳钢钉放入“84消毒液”(NaClO溶液)中浸泡一段时间。预期的实验现象是。
(5)为了进一步探究碳钢钉在该消毒液(NaClO)中的腐蚀原理,某同学设计了如图所示实验装置,写出碳(C)极上发生的电极反应式________。

高三化学填空题困难题查看答案及解析
-
已知1 mol CH4气体完全燃烧生成气态CO2和液态H2O,放出890.3 kJ热量,表示该反应的热化学方程式正确的是
A.CH4 (g)+2O2 (g)=CO2 (g)+2H2O(g) ΔH=+890.3 kJ·molˉ1
B.CH4 (g)+2O2 (g)=CO2 (g)+2H2O(l) ΔH=-890.3 kJ·molˉ1
C.CH4 (g)+2O2 (g)=CO2 (g)+2H2O(l) ΔH=+890.3 kJ·molˉ1
D.CH4 (g)+2O2 (g)=CO2 (g)+2H2O(g) ΔH=-890.3 kJ·molˉ1
高三化学选择题简单题查看答案及解析