海水的综合利用可以制备金属钠和镁,其流程如图所示:
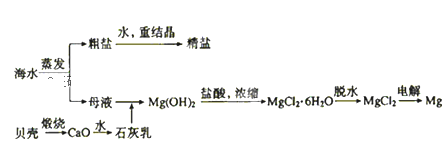
下列说法不正确的是( )
A.要检验母液中是否含氯离子应选用的试剂是:硝酸酸化的硝酸银溶液
B.上述流程中的脱水过程属于分解反应
C.上述流程中涉及的变化都属于化学变化
D.上述流程中生成Mg(OH)2沉淀的离子方程式为:Mg2++Ca(OH)2=Mg(OH)2+Ca2+
高一化学单选题简单题
海水的综合利用可以制备金属钠和镁,其流程如图所示:

下列说法不正确的是( )
A.要检验母液中是否含氯离子应选用的试剂是:硝酸酸化的硝酸银溶液
B.上述流程中的脱水过程属于分解反应
C.上述流程中涉及的变化都属于化学变化
D.上述流程中生成Mg(OH)2沉淀的离子方程式为:Mg2++Ca(OH)2=Mg(OH)2+Ca2+
高一化学单选题简单题
海水的综合利用可以制备金属钠和镁,其流程如图所示:

下列说法不正确的是( )
A.要检验母液中是否含氯离子应选用的试剂是:硝酸酸化的硝酸银溶液
B.上述流程中的脱水过程属于分解反应
C.上述流程中涉及的变化都属于化学变化
D.上述流程中生成Mg(OH)2沉淀的离子方程式为:Mg2++Ca(OH)2=Mg(OH)2+Ca2+
高一化学单选题简单题查看答案及解析
海水的综合利用可以制备金属钠和镁,其流程如下图所示:
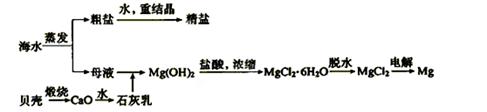
下列说法不正确的是( )
A.要检验母液中是否含氯离子应当用硝酸酸化的硝酸银溶液进行实验
B.上述流程中所有反应都是非氧化还原反应
C.上述流程中生成Mg(OH)2沉淀的离子方程式为:Mg2++Ca(OH)2= Mg(OH)2+Ca2+
D.不用电解MgO来制取镁是因为MgO熔点高,能耗大
高一化学选择题中等难度题查看答案及解析
海水的综合利用可以制备金属钠和镁等,其流程如下图所示:
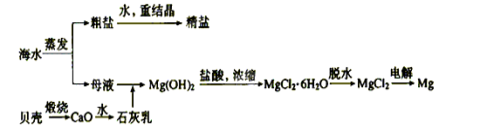
下列说法不正确的是 ( )
A.海水提盐都属于物理变化
B.利用母液可进一步提取溴,但要富集
C.上述流程中生成Mg(OH)2沉淀的离子方程式为:Mg2++Ca(OH)2= Mg(OH)2+Ca2+
D.不用电解MgO来制取镁是因为MgO熔点高,能耗大
高一化学选择题中等难度题查看答案及解析
海水的综合利用可以制备金属镁,其流程如图所示:

(1)写出下列反应的化学方程式。
①石灰乳与母液反应___;
②Mg(OH)2中加入盐酸的离子方程式:__;
③MgCl2Mg:___。
(2)在海水提取镁的过程中,没有涉及的化学反应类型__
A.分解反应 B.化合反应 C.复分解反应 D.置换反应 E.氧化还原反应
高一化学工业流程中等难度题查看答案及解析
海水的综合利用可以制备金属钠和镁,请根据下列工艺生产流程回答问题。
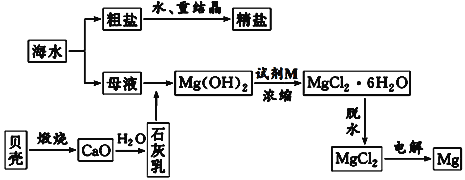
(1)海水提取镁要用到海滩上的贝壳,贝壳煅烧过程中发生反应的化学方程式为___。
(2)母液中加入石灰乳反应的离子方程式为__。
(3)若在空气中加热MgCl2·6H2O生成的是Mg(OH)Cl或MgO,而MgO的熔沸点非常高,达到熔融状态需要消耗很多能源。所以,用电解法制取金属镁时,需要无水氯化镁。写出用电解法制取金属镁的化学方程式___。
(4)在以上提取镁的过程中,没有涉及的化学反应类型是__。
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
高一化学工业流程中等难度题查看答案及解析
海水的综合利用可以制备金属钠和镁等,其流程如图所示。
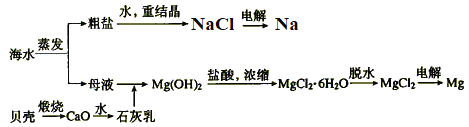
下列说法正确的是
A. 电解NaCl溶液可得到金属钠
B. 上述过程中发生了分解、化合、置换、复分解反应
C. 上述流程中生成Mg(OH)2沉淀的离子方程式为Mg2++2OH-=Mg(OH)2↓
D. 不用电解MgO来制取镁是因为MgO的熔点比MgCl2的高,能耗大
高一化学单选题中等难度题查看答案及解析
海水的综合利用可以制备金属镁,其流程如下图所示:

(1)完成下列方程式:
煅烧贝壳(化学方程式): ;
Mg(OH)2加盐酸(离子方程式):
(2)电解熔融MgCl2的反应化学方程式是 。
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发3个步骤的操作中都要用到玻璃棒,分别说明在这3种情况下使用玻璃棒的目的。
溶解时: 。
过滤时: 。
蒸发时: 。
(4)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl和HCl,写出相应反应的化学方程式: 。
高一化学填空题简单题查看答案及解析
海水的综合利用可以制备金属钠和镁,其流程如下图所示:
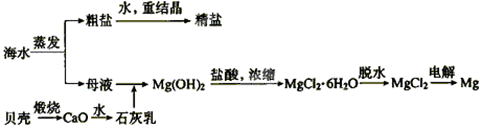
(1)上述流程中生成氢氧化镁沉淀的离子方程式为________。氢氧化镁沉淀和盐酸反应的离子方程式为________。
(2)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明这三种情况下使用玻璃棒的作用:
溶解时:____________;过滤时:____________;蒸发时:______________。
高一化学填空题中等难度题查看答案及解析
综合利用海水可以制备食盐、纯碱、金属镁等物质,其流程如下图所示:

(1)反应①~⑤中,属于氧化还原反应的是 (填编号)。
(2)写出反应②的离子方程式 。
(3)X溶液中的主要阳离子是Na+和 。
(4)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③ ;④加适量盐酸;⑤ 。(请补全缺少的实验步骤);若②步中改为依次加入过量的Na2CO3溶液、NaOH溶液、BaCl2溶液,则产生的后果是 。
(5)检验纯碱样品中是否含NaCl应选用的试剂是 。
高一化学实验题困难题查看答案及解析
综合利用海水可以制备食盐、纯碱、金属镁等物质,其流程如下图所示:
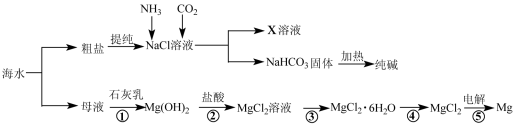
(1)反应①~⑤中,属于氧化还原反应的是 (填编号)。
(2)写出反应②的离子方程式 。
(3)X溶液中的主要阳离子是Na+和 。
(4)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③ ;④加适量盐酸;⑤ (请补全缺少的实验步骤)。
(5)检验纯碱样品中是否含NaCl应选用的试剂是 。
高一化学填空题困难题查看答案及解析