已知:25℃时,Ka(HA)>Ka(HB)。该温度下,用0.100 mol/L盐酸分别滴定浓度均为0. 100 mol/L的NaA溶液和NaB溶液,混合溶液的pH与所加盐酸体积(V)的关系如右图所示。下列说法正确的是
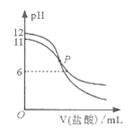
A.滴定前NaA溶液与NaB溶液的体积相同
B.25℃时,Ka(HA)的数量级为l0-11
C.当pH均为6时,两溶液中水的电离程度相同
D.P点对应的两溶液中c(A-)+c(HA)<c(B-)+c(HB)
高三化学单选题中等难度题
已知:25℃时,Ka(HA)>Ka(HB)。该温度下,用0.100 mol/L盐酸分别滴定浓度均为0. 100 mol/L的NaA溶液和NaB溶液,混合溶液的pH与所加盐酸体积(V)的关系如右图所示。下列说法正确的是

A.滴定前NaA溶液与NaB溶液的体积相同
B.25℃时,Ka(HA)的数量级为l0-11
C.当pH均为6时,两溶液中水的电离程度相同
D.P点对应的两溶液中c(A-)+c(HA)<c(B-)+c(HB)
高三化学单选题中等难度题
已知:25℃时,Ka(HA)>Ka(HB)。该温度下,用0.100 mol/L盐酸分别滴定浓度均为0. 100 mol/L的NaA溶液和NaB溶液,混合溶液的pH与所加盐酸体积(V)的关系如右图所示。下列说法正确的是

A.滴定前NaA溶液与NaB溶液的体积相同
B.25℃时,Ka(HA)的数量级为l0-11
C.当pH均为6时,两溶液中水的电离程度相同
D.P点对应的两溶液中c(A-)+c(HA)<c(B-)+c(HB)
高三化学单选题中等难度题查看答案及解析
已知:25℃时,Ka(HA)>Ka(HB)。该温度下,用0.100 mol/L盐酸分别滴定浓度均为0. 100 mol/L的NaA溶液和NaB溶液,混合溶液的pH与所加盐酸体积(V)的关系如右图所示。下列说法正确的是
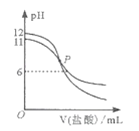
A.滴定前NaA溶液与NaB溶液的体积相同
B.25℃时,Ka(HA)的数量级为l0-11
C.当pH均为6时,两溶液中水的电离程度相同
D.P点对应的两溶液中c(A-)+c(HA)<c(B-)+c(HB)
高三化学单选题中等难度题查看答案及解析
常温下, 用0.100mol·L-1NaOH溶液分别滴定20.00mL0.100mol·L-1的HA溶液和HB溶液的滴定曲线如图。下列说法错误的是(己知lg2≈0.3)
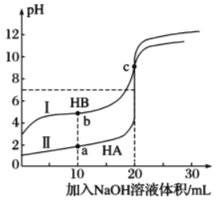
A.HB是弱酸,b点时溶液中c(B-)>c(Na+)>c(HB)
B.a、b、c三点水电离出的c(H+):a>b>c
C.滴定HB溶液时,应用酚酞作指示剂
D.滴定HA溶液时, 当V(NaOH)=19.98mL时溶液pH约为4.3
高三化学单选题中等难度题查看答案及解析
下图为0.100mol/LNaOH溶液分别滴定20.00mL0.100mol/L的HA和HB的滴定曲线。下列说法错误的是(己知1g2≈0.3)

A. HB是弱酸,b点时溶液中c(B-)>c(Na+)>c(HB)
B. a、b、c三点水电离出的c(H+): a<b<c
C. 滴定HB时,不宜用甲基橙作指示剂
D. 滴定HA溶液时,当V(NaOH)=19.98mL时溶液pH约为3.7
高三化学选择题困难题查看答案及解析
常温下,用0.100mol·L-1的NaOH溶液分别滴定同浓度、体积均为20.00mL的盐酸和醋酸溶液(用HA表示酸),得到2条滴定曲线,如图所示。
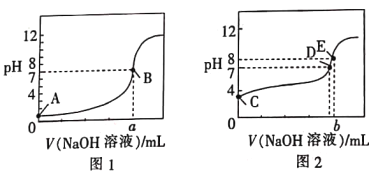
下列说法正确的是
A. 滴定醋酸的曲线是图1
B. 由图分析可得b>a=20
C. D点对应的溶液中:c(Na+)=c(A-)
D. 根据E点可计算得K(HA)=[0.05+(10-6-10-8)]×10-8/(10-6-10-8)
高三化学单选题中等难度题查看答案及解析
常温下,用0.10 mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10 mol·L-1HA溶液和HB溶液所得滴定曲线如图,下列说法不正确的是
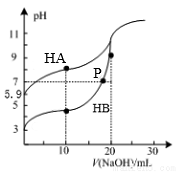
A. Ka(HA)=10-10.8
B. 滴定至P点时,溶液中:c(B-)+c(OH-)<c(HB)+c(H+)
C. 当滴定分别消耗l0mLNaOH 溶液时:c(B-)-c(A-)=c(HA)-c(HB)
D. 当滴定分别消耗20mLNaOH溶液时,将二种溶液混合:c(Na+)>c(B-)>c(A-)>c(H+)
高三化学选择题困难题查看答案及解析
室温下,0.1 mol·L-1 NaOH溶液分别滴定100 mL 0.1 mol·L-1 HA、HB两种酸溶液。pH随NaOH溶液体积如下图所示,下列判断错误的是
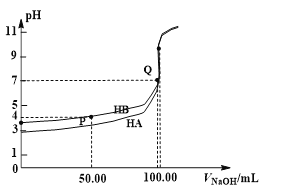
A. 电离常数:Ka(HA) > Ka(HB)
B. Ka(HB)≈10-4
C. pH=7时,c(A—)=c(B—)
D. 中和分数达100%时,HA溶液中存在
高三化学单选题中等难度题查看答案及解析
室温下,0.1 mol·L-1 NaOH溶液分别滴定100 mL 0.1 mol·L-1 HA、HB两种酸溶液。pH随NaOH溶液体积如下图所示,下列判断错误的是
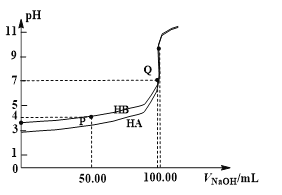
A.电离常数:Ka(HA) > Ka(HB)
B.Ka(HB)≈10-4
C.pH=7时,c(A—)=c(B—)
D.中和分数达100%时,HA溶液中存在
高三化学单选题中等难度题查看答案及解析
25℃时,浓度均为0.100 mol/L的HA溶液和BOH溶液各20.00 mL,分别用0.100 mol/L NaOH溶液、0.100 mol/L 盐酸进行滴定,滴定过程中pH随滴加溶液体积变化关系如图,两图像关于pH=7呈上下对称。下列说法错误的是
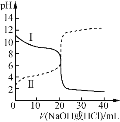
A.曲线Ⅰ表示盐酸滴加到BOH溶液的过程,可用甲基橙作指示剂
B.Ka(HA) =Kb(BOH),交点对应横坐标V< 20.00 mL
C.曲线Ⅰ,滴加溶液到10.00 mL时:c(BOH) > c(Cl-) > c(OH-) >c(H+)
D.曲线Ⅱ,滴加溶液到5.00~10.00 mL时:c(A-) +c(OH-) =c(H+) +c(Na+)
高三化学单选题中等难度题查看答案及解析
25 ℃时,用0.100 0 mol·L-1 NaOH溶液滴定20 mL 0.100 0 mol·L-1一元酸HA(pKa=-lg Ka=4.75)溶液,其滴定曲线如图所示,下列说法正确的是
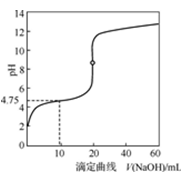
A.当滴定到pH=4.75时,c(Na+)>c(A-)=c(HA)>c(OH-)
B.当溶液中c(H+)+c(OH-)=2×10-7时: c(Na+)=c(A-)>c(OH-)=c(H+)
C.当滴入NaOH溶液20 mL时,c(OH-)=c(H+)+c(HA)
D.当滴入40 mL NaOH溶液时,溶液中:c(Na+)>c(A-)>c(OH-)>c(H+)
高三化学选择题困难题查看答案及解析