-
自20世纪80年代以来建立起的沼气发酵池,其生产的沼气用作燃料,残渣(沼渣)中除含有丰富的氮、磷、钾等常量元素外,还含有对作物生长起重要作用的硼、铜、铁、锌、锰、铬等微量元素,是一种非常好的有机肥。请回答下列问题:
(1)现代化学中,常利用___________上的特征谱线来鉴定元素。
(2)下列微粒基态的电子排布中未成对电子数由多到少的顺序是__________(填字母)。
a.Mn2+ B.Fe2+ C.Cu D.Cr
(3)P4易溶于CS2,难溶于水的原因是___________。
(4)铜离子易与氨水反应形成[Cu(NH3)4]2+配离子。
①[Cu(NH3)4]2+中提供孤电子对的成键原子是__________。
②研究发现NF3与NH3的空间构型相同,而NF3却难以与Cu2+形成配离子,其原因是___________。
(5)某晶胞中各原子的相对位置可用如图所示的坐标系表示:
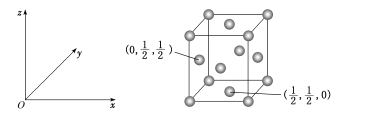
在铁(Fe)的一种立方晶系的晶体结构中,已知2个Fe原子坐标是(0,0,0)及( ,
, ,
, ),且根据均摊法知每个晶胞中有2个Fe原子。
),且根据均摊法知每个晶胞中有2个Fe原子。
①根据以上信息,推断该晶体中原子的堆积方式是__________,
②已知晶体的密度为ρg·cm-3,Fe的摩尔质量是M g·mol-1,阿伏加德罗常数为NA,晶体中距离最近的两个铁原子之间的距离为_________ pm(用代数式表示)。
-
我国有丰富的海水资源,海水中的元素共含有80多种,总储量很大。常量元素包括H、B、C、O、F、Na、Mg、S、Cl、K、Ca、Br、Sr等13种元素,同时还含有Cr、Mn、Fe、Ni、Cu、Zn等微量元素,因此开发利用海水资源具有非常广阔的前景。
(1)上述涉及到的元素中,不属于前四周期的是___,基态原子中的未成对电子数最多是___(写元素符号)。
(2)基态Fe3+的价电子排布式___,基态B原子的电子排布图为___。
(3)B、C、O、F四种元素基态原子第一电离能由大到小的顺序为___(写元素符号)。
(4)CO32-的中心原子价层电子对数为___对,SO32-的空间构型为___,HCHO中C的杂化方式为___。
(5)氨气极易溶于水的主要原因之一为NH3与H2O分子之间可以形成氢键,氨水中存在的氢键有___种。
(6)干冰与水晶熔化需破坏的主要作用分别是___、___。
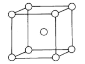
(7)已知钠的密度为ag/cm3,NA为阿伏加德罗常数的值,钠的晶胞结构如图,则晶胞棱长为___ pm。
-
NaI用作制备无机和有机碘化物的原料,也用于医药和照相等,工业利用碘、氢氧化钠和铁屑为原料可生产NaI,其生产流程如下图。
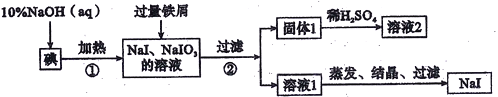
(1)碘元素在周期表中的位置为______________________。
(2)反应①的离子方程式为___________________________________________。
(3)反应②加入过量铁屑的目的是_________________,过滤所得固体1中除剩余铁屑外,还有红褐色固体,则加入铁屑时发生反应的化学方程式为____________________________________。
(4)溶液2中除含有H+外,一定还含有的阳离子是_______________;试设计实验验证溶液2中该金属阳离子的存在:___________________________________________。
(5)溶液2经一系列转化可以得到草酸亚铁晶体(FeC2O4·2H2O,相对分子质量180),称取3.60 g草酸亚铁晶体,用热重法对其进行热分解(隔绝空气加热),得到剩余固体的质量随温度变化的曲线如右图所示:
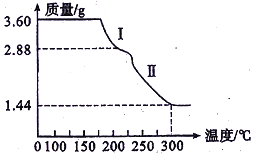
①分析图中数据,根据信息写出过程I发生的化学方程式:_________________________________。
②300℃时剩余固体只含一种成分且是铁的氧化物,写出过程II发生的化学方程式: ________________。
-
重铬酸盐广泛用作氧化剂、皮革制作等。以铬矿石(主要成分是Cr2O3,含FeO、Al2O3、 SiO2等杂质)为原料制取重铬酸钠的流程如下:
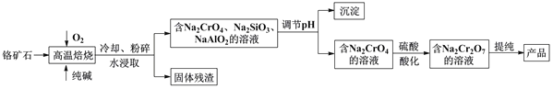
请回答下列问题:
(1) 固体残渣主要是含________元素的氧化物。
(2)写出Cr2O3与纯碱在高温焙烧时反应的化学方程式_______________________。
(3)高温焙烧后粉碎的目的是_____________________________,调节pH时形成的沉淀的成分是_______________________________________________。
(4)写出硫酸酸化使Na2CrO4转化为Na2Cr2O7的离子方程式 ______________________。
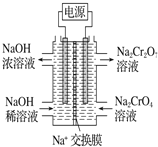
(5)某工厂采用石墨电极电解Na2CrO4溶液,实 现了 Na2CrO4到Na2Cr2O7的转化,其原理如图所示。写出阳极的电极反应式____________________。
(6)Na2Cr2O7可用于测定废水的化学耗氧量(即COD,指每升水样中还原性物质被氧化 所需要O2的质量)。现有某水样100.00 mL,酸化后加入C1 mol/L的Na2Cr2O7溶液 V1 mL,使水中的还原性物质完全被氧化(Cr2O72-还原为Cr3+);再用C2mol/L的FeSO4溶液滴定剩余的Cr2O72-,结果消耗FeSO4溶液V2 mL。
①该水样的COD为________________mg/L;
②假设上述反应后所得溶液中Fe3+和Cr3+的物质的量浓度均为0.1 mol/L,要使Fe3 +沉 淀完全而Cr3+还未开始沉淀.则需调节溶液pH的范围是______________。(可能用到的数据:KSPFe(OH)3=4.0×10-38, KSPCr(OH)3=6.0×10-31, ,
, ,
, ,
, )
)
-
“低碳经济,节能减排”是21世纪世界经济发展的新思路,下列与之相悖的是( )
A. 开发水能、风能、太阳能、地热能、核能等新能源,减少使用煤、石油等化石燃料
B. 大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
C. 大力发展新能源汽车,如混合动力汽车、电动汽车等,以减少碳、氮氧化物的排放
D. 大力开采煤、石油和天然气,以满足经济发展的需要
-
“低碳经济,节能减排”是21世纪世界经济发展的新思路。下列与之相悖的是( )
A.开发水能、风能、太阳能、地热能、核能等新能源,减少使用煤、石油等化石燃料
B.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
C.大力开采煤、石油和天然气,以满足经济发展的需要
D.大力发展新能源汽车,如混合动力汽车、电动汽车等,以减少碳、氮氧化物的排放
-
“低碳经济,节能减排”是21世纪世界经济发展的新思路。下列与之相悖的是( )
A.开发水能、风能、太阳能、地热能、核能等新能源,减少使用煤、石油等化石燃料
B.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
C.大力开采煤、石 油和天然气,以满足经济发展的需要
油和天然气,以满足经济发展的需要
D.大力发展新能源汽车,如混合动力汽车、电动汽车等,以减少碳、氮氧化物的排放
-
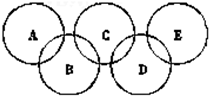
如图为“奥运五环”,如果五元环分别代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素;五种化合物由五种短周期元素形成,每种化合物仅含有两种元素.A是沼气的主要成分;B、E分子中所含电子数都为18,B不稳定,具有较强的氧化性;E是由六个原子构成的分子,可用于火箭燃料;C是由地壳中含量最高的两种元素组成;D中所含的两种元素的原子个数之比为3:4.根据以上信息回答下列问题:
(1)A、B、C、D、E的化学式分别是______.
(2).A燃烧的化学方程式为______ CO2+2H2O
-
A、B、C、D、E、F元素是原子序数依次增大的6种短周期元素。已知A是短周期元素中原子半径最小的元素,A和B形成的18电子的化合物X常用作火箭的燃料,C原子最外层电子数与核外电子总数之比为3∶4,E与C同主族,D和C可以形成原子个数比为1∶1和2∶1的两种离子化合物。
据此回答下列问题:
(1)D和C形成1∶1的化合物中阴阳离个数比为____________。
(2)化合物X的结构式为____________。1 mol气态X在适量C2中燃烧,生成B2和气态A2C, 放出534 kJ的热量,1 mol液态A2C完全汽化需吸收44 kJ热量。请写出气态X在C2中燃烧生成B2和液态A2C时的热化学方程式_____________________________________
(3)某化合物由上述6种元素中的3种元素组成,为常见家用消毒剂的主要成分,其中化学键类型为__________________;该化合物水溶液不呈中性的原因是(用离子方程式表示)__________________________________,该化合物可以通过电解D和F形成化合物的水溶液获得,电解时反应的化学方程式为_________________________________
(4)写出一个可以证明C的非金属性大于E的化学反应方程式:_____________________________________________。
-
X是核外电子数最少的元素,Y是地壳中含量最丰富的元素,Z在地壳中的含量仅次于Y,W可以形成自然界最硬的原子晶体.下列叙述错误的是( )
A.WX4是沼气的主要成分
B.固态X2Y是分子晶体
C.ZW是原子晶体
D.ZY2的水溶液俗称“水玻璃”

,
,
),且根据均摊法知每个晶胞中有2个Fe原子。





