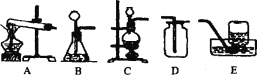-
18世纪70年代,瑞典化学家舍勒首先发现并制得了氯气(Cl2)。氯气是一种黄绿色、密度比空气大且有毒的气体,它能与水发生化学反应生成盐酸和次氯酸(HClO)。氯气也能与碱溶液发生化学反应。在实验室中,通常用二氧化锰固体与浓盐酸在加热的条件下制取氯气。现提供如下图所示实验装置,试回答下列问题:
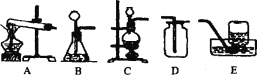

(1)实验室中制取氯气应采用的发生装置是________,收集并吸收氯气应选用的装置为________。(均填序号)
(2)上述装置的烧杯中盛有的氢氧化钠溶液的作用是用于吸收多余的氯气,防止氯气污染空气,试写出氯气和氢氧化钠溶液反应的化学方程式:________。
(3)自来水厂经常用氯气做消毒剂。目前市场上出售的某些假冒“纯净水”是用自来水灌装的,请你利用所学的化学知识加以鉴别,并写出有关的化学方程式________,_______ 。
(4)次氯酸具有漂白性,它可以将某些有色物质氧化成无色物质。某同学用滴管将饱和氯水(氯气的水溶液)逐滴滴入含有酚酞试液的NaOH溶液中,当滴到最后一滴时,红色突然褪去。红色褪去的原因可能有两种情况(用简要的文字说明):①_____;②_____。
(5)请设计一个简单的实验,确定(4)中红色褪去的原因是①还是②?________。
-
瑞典化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合加热,在世界上首先得到了氯气.已知Cl2和碱溶液在不同条件下,得到的产物不同,某兴趣小组用如图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质.
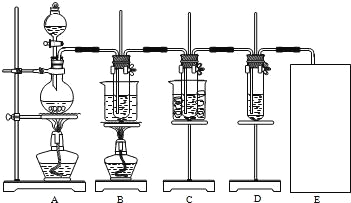
图中:A为氯气发生装置;B的试管里盛有15mL 30% KOH溶液,并置于水浴中;C的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;D的试管里盛有紫色石蕊试液.
请填写下列空白:
(1)制取氯气时,在圆底烧瓶里加入一定质量的二氧化锰,通过_____(填仪器名称)向圆底烧瓶中加入适量的浓盐酸.装置A中反应的离子方程式是_____.
(2)制取氯酸钾是在装置B中进行的,装置B中制取氯酸钾的化学反应方程式是____________.该小组同学发现制得的氯酸钾产量偏低,原因是氯气中含有杂质,改进方法是______.
(3)实验中装置D的试管中产生的现象是________.
(4)请在装置图方框中画出上述实验还缺少的装置,并注明试剂.________
(5)该小组同学认为:SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强.但是如果将SO2和Cl2同时通入到品红溶液中,则会发现褪色效果并不像该小组同学想象的那样.请你分析原因(用离子方程式表示)_______.
-
下列“科学史话”中得出的结论不正确的是( )
A.从舍勒发现一种黄绿色气体,到戴维确认该气体为氯气,花了三十多年时间,说明科学研究要付出艰辛的劳动
B.由于化学工业的发展,历史上出现了“伦敦光化学烟雾”事件,预示着化学最终只会给人类带来灾难
C.门捷列夫发现的元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑
D.凯库勒梦其所想,从梦中得到启发,成功地提出了苯环结构,表明灵感来自于实践和思考
-
下列有关于Cl2的说法中,不正确的是
A. Cl2是一种黄绿色、密度比空气大的有毒气体
B. Cl2能与水反应生成盐酸和次氯酸
C. 工业上用Cl2和石灰水为原料制造漂白粉
D. 红热的铁丝在Cl2中剧烈燃烧,产生棕色烟
-
下列有关氯气的说法正确的是 ( )。
A.氯气是黄绿色气体,有毒,有刺激性气味,氯水还可消毒杀菌
B.液氯就是氯气的水溶液,它能使干燥的有色布条退色
C.红热的铁丝在Cl2中燃烧产生棕色的雾;H2在Cl2中燃烧火焰呈淡蓝色
D.氯水长时间放置会变质,是因为氯气几乎完全挥发,剩下的就是水
-
通过实验测定出空气组成的科学家是( )
A. 法国的拉瓦锡 B. 英国的汤姆生 C. 瑞典的舍勒 D. 意大利的阿伏加德罗
-
PCl3有毒,在潮湿的空气中可发生水解反应产生大量的白雾。它在实验室和工业上都有重要的应用。在实验室中制取PCl3,在D中放入足量白磷,将Cl2迅速而且不间断地通入D中,氯气与白磷会发生反应,产生火焰。

三氯化磷和五氯化磷的物理常数如下:
| 熔点 | 沸点 |
| 三氯化磷 | -112℃ | 76℃ |
| 五氯化磷 | 146℃ | 200℃分解 |
注:常温下五氯化磷不溶于三氯化磷
(1)写出A中发生反应的化学方程式:____________________________。
(2)反应开始前需要检查装置气密性,检查方法为____________________________。
(3)氯气和白磷反应放出大量的热,为使仪器D不致因局部过热而炸裂,实验开始前应在D的底部放少量____________________________。
(4)在烧杯E中加入冰盐水,其作用是____________________________。
(5)白磷与氯气反应产物中可能含有一定量的PCl5,从中分离出三氯化磷的方法是______________。经过一段时间反应发现B中竖直导管液面上开,可能的原因是____________________________。
(6)装置F的作用是____________________________。
-
20世纪90年代,国际上提出了“预防污染”的新概念。“绿色化学”是“预防污染”的基本手段,下列各项中属于“绿色化学”的是( )
A.处理废弃物 B.杜绝污染源
C.减少有毒物 D.治理污染点
-
能够用键能大小解释的是( )
A.氮气的化学性质比氧气稳定
B.常温常压下,溴呈液态,碘呈固态
C.稀有气体一般很难发生化学反应
D.相同状态下,氯气的密度比空气的大
-
70年代开始发现氯气应用水消毒会产生具有致癌作用的卤代甲烷类化合物。氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的广泛消毒剂,是一种黄绿色的气体,易溶于水。我国从2000年起已逐步用消毒剂ClO2代替氯气对饮用水进行消毒。
(1)ClO2消毒水时,可将Fe2+、Mn2+转化成Fe(OH)3、MnO2难溶物除去,用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子ClO2-。2001年我国卫生部规定,饮用水的ClO-2含量应不超过0.2mg/L。若饮用水中ClO2-的含量超标,可向其中加入适量的某还原剂,该反应的氧化产物是_____________(填化学式)。
ClO2在杀菌消毒的同时,可将剧毒氰化物中碳、氮元素氧化成无毒气体而除去,写出用ClO2氧化除去NaCN的化学方程式___________________________________。
(2)①工业上制备ClO2,可以通过NaClO3在H2SO4存在的条件下与Na2SO3反应制得。
请写出该反应的离子方程式:_________________________________________。
②实验室制备ClO2,可以用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料在一定条件下制得,只是制得的ClO2中混有NH3除去ClO2中的NH3可选用的试剂是____;(填序号)
A.浓硫酸 B.饱和食盐水
C.碱石灰 D.水
(3)测定ClO2(如图)的过程如下:在锥形瓶中加入足量的碘化钾,用100mL水溶解后,再加3mL硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收;将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用cmol/L硫代硫酸钠标准溶液滴定(I2+2S2O32-===2I—+S4O62—),共用去V ml硫代硫酸钠溶液。
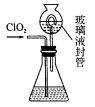
①装置中玻璃液封管的作用是__________________;
②滴定终点的现象是:_________________________。