-
孔雀石主要含Cu2 (OH)2CO3,还含少量Fe、Si的化合物。某工厂以孔雀石为主要原料制备CuSO4·5 H2O及纳米材料G,主要步骤如下:
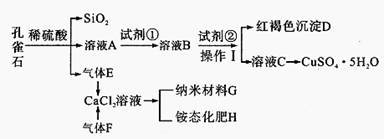
已知该条件下,通过调节溶液的酸碱性而使Fe3+、Fe2+、Cu2+生成沉淀的pH分别如下:
| 物质 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe(OH)3 | 2.2 | 3.2 |
| Fe(OH)2 | 7.6 | 9.6 |
| Cu(OH)2 | 4.7 | 6.4 |
请回答下列问题:
(1)写出孔雀石主要成分Cu2(OH)2CO3与稀硫酸反应的化学方程式 ________ 。
(2)溶液A的金属离子有Cu2+、Fe2+、Fe3+。要检验其中的Fe2+应选择下列试剂中的________。
a.KMnO4 b.NaOH c.H2O2 d.KSCN
(3)溶液A中的金属离子有Cu2+、Fe2+、Fe3+。试剂①是一种氧化剂,把Fe2+氧化成Fe3+的目的是________。该工厂选用试剂①最好为下列中的________(填代号)。
a.H2O2 b.空气 c.Cl2 d.KSCN
(4)根据下图有关数据,你认为工业上氧化操作时应采取的措施是________。
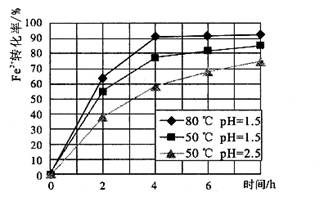
(5)向溶液B中加入试剂②的化学式为________,操作I的名称是________。
(6)气体E和气体F应该先通人CaCl2溶液中的是________(填化学式)。写出制备G和H的化学反应方程式________。
(7)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定,反应中MnO4-还原为Mn2+,则该反应的离子方程式为________ ________。取A溶液20.00 mL,用去0.0240mol/LKMnO4溶液16.00 mL时,恰好达到滴定终点,则A溶液中Fe2+浓度为________。
-
某工厂以孔雀石[主要成分为Cu2(OH)2CO3,含有少量Fe、Si的氧化物]为主要原料制备蓝矾晶体(CuSO4·5H2O),其生产流程如图所示:
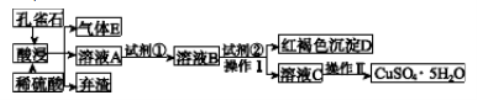
已知该条件下,通过调节溶液的酸碱性而使Fe3+、Fe2+、Cu2+生成沉淀的pH分别如下表所示:
| 物质 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe(OH)3 | 2.2 | 3.2 |
| Fe(OH)2 | 7.6 | 9.6 |
| Cu(OH)2 | 4.7 | 6.4 |
回答下列问题:
(1)弃渣的主要成分是____________,Ⅱ中有“洗涤”的操作,其目的是_____________________。
(2)溶液A中的金属离子有Cu2+、Fe2+、Fe3+。试剂①是一种氧化剂,则试剂①最好为下列中的____________,反应的离子方程式为______________________。
a.Na2O2 b.H2O2 c.Cl2 d.KSCN
(3)根据下图有关数据,你认为工业上氧化操作时应采取措施将反应温度及溶液pH分别控制在_________________,氧化时间为________h左右。
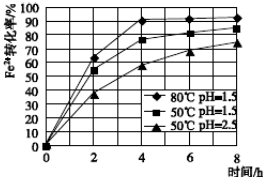
(4)操作Ⅰ中溶液的pH应控制在________范围内。
(5)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液进行滴定,则KMnO4溶液应置于________(填“酸”或“碱”)式滴定管中。若滴定20.00mLA的溶液,用去0.0240mol·L-1KMnO4溶液16.00mL时恰好达到滴定终点,则A溶液中Fe2+的浓度为________________。
-
(16分)孔雀石主要含Cu2(OH)2CO3,还含少量Fe、SiO2的化合物,实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下:
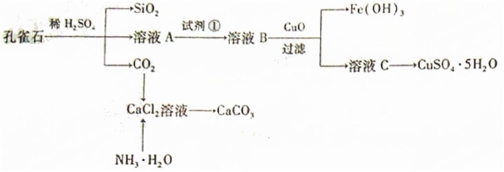
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中试剂①为 (填代号),检验溶液A中Fe3+的最佳试剂为 (填代号)。
a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN
(2)由溶液C获得CuSO4·5H2O,需要经过加热蒸发、 、过滤等操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是 。
(3)制备CaCO3时,应向CaCl2溶液中先通入 ,然后再通入 (填化学式)。
(4)欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时视线应 。用KMnO4标准溶液滴定时应选用 滴定管(填“酸式”或“碱式”)。
-
(12分)孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下:
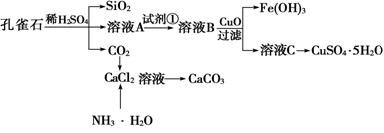
请回答下列问题:
(1)溶液A中的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中试剂①为________(填代号),检验溶液A中Fe3+的最佳试剂_____(填代号)。
a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN
(2)由溶液C获得CuSO4·5H2O,需要经过加热蒸发、________、过滤等操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是 ________________。
(3)制备CaCO3时,应向CaCl2溶液中先通入(或先加入)________(填化学式)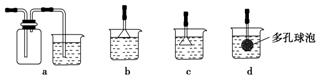 。
。
(4)欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时视线应________,直到________。用KMnO4标准溶液滴定时应选用________滴定管(填“酸式”或“碱式”)。
-
(12分)孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。以孔雀石为原料可制备CuSO4·5H2O及纳米材料G,步骤如下:
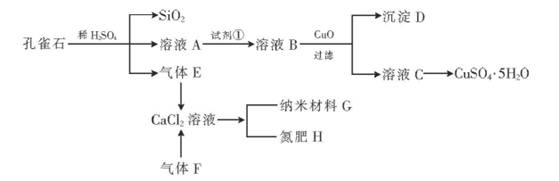
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中,试剂①最佳为(填代号),检验溶液A中Fe3+的最佳试剂为________(填代号)。
a. KMnO4 b.(NH4)2S c.H2O2 d.KSCN
沉淀D中除了过量的CuO外,还存在另一种固体,其化学式为________。加入CuO作用是________。
(2)由溶液C获得CuSO4·5H2O,需要经过一系列操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是________。
(3)制备纳米材料G时,应向CaCl2溶液中先通入(或先加入)________(填化学式)。写出该反应的化学方程式________。
(4)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定,取用KMnO4标准溶液应用________(填写仪器名称);取A溶液稀释一定倍数后,用KMnO4标准溶液滴定,终点现象为________。
-
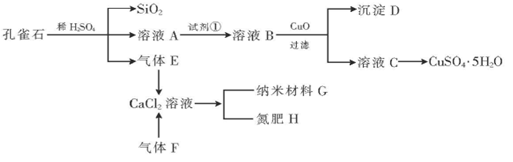
(11分)孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。以孔雀石为原料可制备CuSO4·5H2O及纳米材料G,步骤如下:
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中,试剂①最佳为________(填代号),检验溶液A中Fe3+的最佳试剂为________(填代号)。
a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN[
沉淀D中除了过量的CuO外,还存在另一种固体,其化学式为________。加入CuO作用是____________________________________ 。
(2)由溶液C获得CuSO4·5H2O,需要经过一系列操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是________。
(3)制备纳米材料G时,应向CaCl2溶液中先通入(或先加入)________(填化学式)。
写出该反应的化学方程式__________________________ 。
(4)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定,取用KMnO4标准溶液
应用______________(填写仪器名称);取A溶液稀释一定倍数后,用KMnO4标
准溶液滴定,终点现象为________。
-
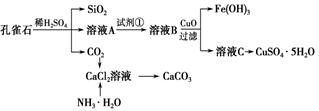
(12分)孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下:
请回答下列问题:
(1)溶液A中的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中试剂①为________(填代号),检验溶液A中Fe3+的最佳试剂为________(填代号)。
a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN
(2)由溶液C获得CuSO4·5H2O,需要经过加热蒸发、________、过滤等操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是___________。
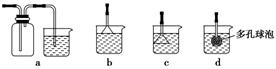
(3)制备CaCO3时,应向CaCl2溶液中先通入(或先加入)________(填化学式)。若实验过程中有氨气逸出,应选用下列________(填代号)装置回收。
-
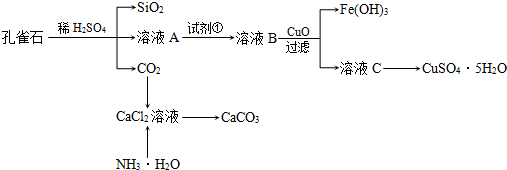
孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物,实验室以孔雀石为原料制备CuSO4•5H2O及CaCO3,步骤如下:
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+:从下列所给试剂中选择:实验步骤中试剂①为0______(填代号),检验溶液A中Fe3+的最试剂为______(填代号).
a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN
(2)由溶液C获得CuSO4•5H2O,需要经过加热蒸发,______,过滤等操作.除烧杯、漏斗外,过滤操作还用到另一玻璃仪器______,该仪器在此操作中的主要作用是______.
(3)制备CaCO3时,应向CaCl2溶液中先通入(或先加入)______(填化学式).若实验过程中有氨气逸出、应选用下列______装置回收(填代号).
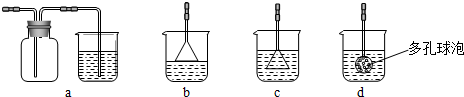
(4)欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时视线应______,直到______.用KMnO4标准溶液滴定时应选用______滴定管(填“酸式”或“碱式”).
-
孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物,实验室以孔雀石为原料制备CuSO4•5H2O及CaCO3,步骤如下:
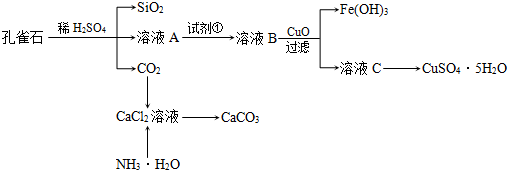
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+:从下列所给试剂中选择:实验步骤中试剂①为0______(填代号),检验溶液A中Fe3+的最试剂为______(填代号).
a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN
(2)由溶液C获得CuSO4•5H2O,需要经过加热蒸发,______,过滤等操作.除烧杯、漏斗外,过滤操作还用到另一玻璃仪器______,该仪器在此操作中的主要作用是______.
(3)制备CaCO3时,应向CaCl2溶液中先通入(或先加入)______(填化学式).若实验过程中有氨气逸出、应选用下列______装置回收(填代号).
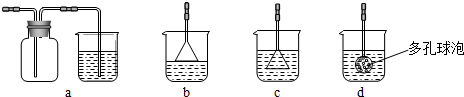
(4)欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时视线应______,直到______.用KMnO4标准溶液滴定时应选用______滴定管(填“酸式”或“碱式”).
-
孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。以孔雀石为原料可制备CuSO4·5H2O及纳米材料G,步骤如下:
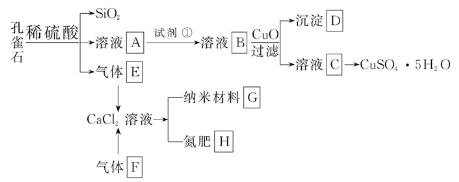
请回答下列问题:
(1)溶液A中的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中,试剂①最佳为_______(填代号)。
a.KMnO4 b.(NH4)2S c.H2O2 d.HNO3
沉淀D中除了过量的CuO外,还存在另一种固体,其化学式为______________。加入CuO的作用是_____________________。
(2)由溶液C获得CuSO4·5H2O,需要经过一系列操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是______________。
(3)制备纳米材料G时,应向CaCl2溶液中先通入(或先加入) _______ (填化学式)。写出该反应的化学方程式_______________________________________。
(4)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定,取用KMnO4标准溶液应用_______ (填写仪器名称);取A溶液稀释一定倍数后,用KMnO4标准溶液滴定,终点现象为_______。






 。
。







