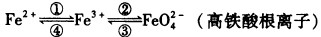-
铁及其化合物之间的相互转化可用下式表示:Fe2+ Fe3+
Fe3+ FeO42-(高铁酸根离子)。回答下列有关问题:
FeO42-(高铁酸根离子)。回答下列有关问题:
(1)Fe与过量盐酸反应可以制取FeCl2。若用反应所得的酸性溶液,实现上述①、④的转化,要求产物纯净,可选用__________(填字母)。
a.Cl2 b.Fe c.Cu d.KMnO4
(2)如下化学方程式中:Fe2O3+3NaClO+4KOH=2K2FeO4(高铁酸钾)+3NaCl+2H2O,还原剂是______________,具有__________性。
(3)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体。高铁酸钾作为水处理剂发挥的作用是___________、__________。
(4)某同学为了检验家中的一瓶补铁药(成分为FeSO4)是否变质,查阅了有关资料,得知Fe2+能被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色,并结合已学的知识设计了如下实验:将药片除去糖衣研细后,溶解过滤,取滤液分别加入两支试管中,在试管Ⅰ中滴入酸性高锰酸钾溶液,在试管Ⅱ中滴入KSCN溶液。
①请你填出该同学实验中出现以下现象时应得出的结论:
| 实验现象 | 试管Ⅰ | 试管Ⅱ | 结论 |
| a | 褪色 | 不变红 | ___ |
| b | 不褪色 | 变红 | ___ |
| c | 褪色 | 变红 | ___ |
②能不能将KMnO4和KSCN滴入到同一试管中进行验证,为什么?试进行解释:________。
-
铁是人类较早使用的金属之一,铁及其化合物之间的相互转化作用可用下式表示:
Fe2+  Fe3+
Fe3+  FeO42-(高铁酸根离子)
FeO42-(高铁酸根离子)
回答下列有关问题:
(1)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒大小范围是______nm。
(2)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,生成FeCl2和CuCl2,制造印刷电路板。写出FeCl3溶液腐蚀铜的化学反应方程式:_____________。检验反应后溶液中还存在Fe3+的试剂是__________。
(3)在下列化学方程式中:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O还原剂是_______________,生成1molNa2FeO4转移电子数目为__________ 。
。
-
高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为: 3ClO-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O,下列有关说法正确的是( )
A.ClO-是氧化剂、OH-是还原剂 B.Fe3+是还原剂、FeO42-是还原产物
C.生成2molFeO42-转移6NA个电子 D.ClO-的还原性大于FeO42-
-
铁的氧化物有很多,在中学化学中经常提到的有FeO、Fe2O3和Fe3O4,而且在一定条件下它们之间是可以相互转化的,例如:在1400℃以上的温度下加热Fe2O3时,Fe2O3会部分失去氧,生成Fe3O4.下列有关说法正确的是
A. FeO、Fe2O3和Fe3O4均为黑色固体
B. Fe3O4常写成FeO•Fe2O3,其中既有+2价的Fe,又有+3价的Fe,所以Fe3O4是一种混合物
C. 热稳定性Fe2O3>Fe3O4
D. FeO、Fe2O3和Fe3O4均可与盐酸反应,且反应类型均为复分解反应
-
根据不同价态铁元素之间的相互转化关系,回答下列问题:
(1)配制含Fe2+的溶液时,常常向溶液中加入少量____________,使被氧气氧化形成的Fe3+还原为Fe2+。
(2)为除去废水中的Fe2+,常先将废水中的Fe2+氧化为________,再根据Fe3+的性质使Fe3+转化为红褐色的________沉淀析出。
(3)在制作印刷电路板的过程中常利用铜与氯化铁溶液的反应。反应的离子方程式为________________。
(4)为消除废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,这一处理过程可用两个离子方程式表示为____________________________,______________________________;处理过程中需定期添加的原料是__________________。
-
高铁酸钾(K2FeO4)是一种常用的水处理剂。工业制备高铁酸钾的离子方程式为ClO+Fe3++OH— FeO42-+Cl+H2O(未配平)。下列叙述不正确的是
A.生成2mol K2FeO4时,转移的电子数为6NA B.K2FeO4中铁元素的化合价是+6
C.还原产物与氧化产物的物质的量之比为2∶3 D.ClO-的氧化性强于FeO42-
-
已知氧化性:Fe3+>I2>SO42-,下列说法或离子方程式正确的是
A.2Fe3++ SO2+ 2H2O = 2Fe2++ SO42-+ 4H+
B.Fe3O4可写成FeO·Fe2O3,Fe3I8可写成FeI2·2FeI3
C.还原性:Fe2+>SO2>I-
D.反应H2SO4(浓)+ 2HI = I2+ SO2↑+ 2H2O不能进行
-
已知氧化性:Fe3+>I2>SO42-,下列说法或离子方程式正确的是( )
A. 还原性:Fe2+>SO2>I-
B. Fe3O4可写成FeO•Fe2O3,Fe3I8可写成FeI2•2FeI3
C. 2 Fe3+ + SO2 + 2H2O = 2 Fe2+ + SO42- + 4H+
D. 反应H2SO4(浓)+ 2HI = I 2 + SO2↑+ 2H2O不能进行
-
铁是人类较早使用的金属之一,铁及其化合物之间的相互转化作用可用下式表示:
I.回答下列有关问题:
(1)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒大小范围是______nm。
(2)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,生成FeCl2和CuCl2,制造印刷电路板。写出FeCl3溶液腐蚀铜的化学反应方程式:___________。检验反应后溶液中还存在Fe3+的试剂是__________。
(3)在下列化学方程式中:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O还原剂是______.
II.现有五种溶液,分别含下列离子:①Ag+,②Mg2+,③Fe2+,④Al3+,⑤Fe3+。
(1)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是______,加铁粉后溶液增重的是 _____________(填写离子符号)
(2)向Fe2+的溶液中滴加NaOH溶液,现象是___________________ 。
(3)欲除去FeCl2中FeCl3选用的试剂是________ , 并写出相应离子方程式:__________。
-
铁是人类较早使用的金属之一,铁及其化合物之间的相互转化作用可用下式表示:
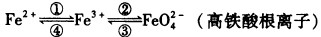
I.回答下列有关问题:
(1)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒大小范围是______nm。
(2)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,生成FeCl2和CuCl2,制造印刷电路板。写出FeCl3溶液腐蚀铜的化学反应方程式:___________。检验反应后溶液中还存在Fe3+的试剂是__________。
(3)在下列化学方程式中:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O还原剂是______,生成1molNa2FeO4转移电子数目为__________。
II.现有五种溶液,分别含下列离子:①Ag+,②Mg2+,③Fe2+,④Al3+,⑤Fe3+。
(1)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是______,加铁粉后溶液增重的是______;
(2)向Fe2+的溶液中滴加NaOH溶液,现象是___________________ 。
(3)欲除去FeCl2中FeCl3选用合适的试剂和分离方法,并写出相应离子方程式:__________。
Fe3+
FeO42-(高铁酸根离子)。回答下列有关问题: