-
NOx、CO、SO2等大气污染气体的处理和利用是世界各国研究的热点问题。
(1)已知:
I. 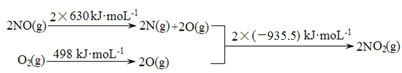
II. 2NO(g)+O2(g)  2NO2(g) ΔH1
2NO2(g) ΔH1
2SO2(g)+O2(g)  2SO3(g) ΔH2 =-196.6 kJ·mol-1
2SO3(g) ΔH2 =-196.6 kJ·mol-1
① ΔH1 =________________kJ·mol-1。
② 写出NO2气体与SO2气体反应生成SO3气体和NO气体的热化学方程式________。
(2)煤炭燃烧过程中释放出大量的SO2,严重破坏生态环境。燃烧过程中加入石灰石可以把硫元素以CaSO4的形式固定,从而降低SO2的排放,该反应的化学方程式是______。
(3)煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低了脱硫效率。发生的两个相关反应的热化学方程式如下:
反应Ⅰ:CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4 kJ·mol-1
CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4 kJ·mol-1
反应Ⅱ:CaSO4(s)+4CO(g) CaS(s)+4CO2(g) ΔH2=-175.6 kJ·mol-1
CaS(s)+4CO2(g) ΔH2=-175.6 kJ·mol-1
资料:①反应Ⅰ和反应Ⅱ同时发生 ②反应Ⅰ的速率大于反应Ⅱ的速率
请回答下列问题:
① 下列反应过程能量变化示意图正确的是_______________。

② 图1为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物中CaS质量百分数的关系曲线。则降低该反应体系中SO2生成量的措施有_________(填字母)。
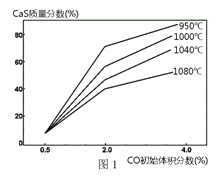
A. 向该反应体系中投入石灰石
B. 在合适的温度区间内控制较低的反应温度
C. 提高CO的初始体积百分数
D. 提高反应体系的温度
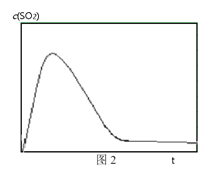
③ 图2表示恒温恒容条件下反应体系中c(SO2)随时间t变化的总趋势图。请从化学反应原理的角度解释c(SO2)先增加后降低的原因_______。
-
(1)SO2、NOx、CO等气体和可吸入颗粒物对环境的污染尤其严重,为了减少它们对环境的污染,通常采用下列措施进行处理:
已知:①N2(g)+O2(g) 2NO(g) ΔH1=+180 kJ·mol-1
2NO(g) ΔH1=+180 kJ·mol-1
②2CO(g)+O2(g) 2CO2(g) ΔH2=-566 kJ·mol-1
2CO2(g) ΔH2=-566 kJ·mol-1
可以在汽车的排气管上安装一个催化装置,使汽车尾气中的CO、NO转化成无污染的物质,则该反应热化学方程式为____________________________,该反应自发进行的条件是_________。
(2)通常将SO2经过净化后,与空气进行催化氧化可制硫酸。不同温度下向一恒容密闭容器中通入n(SO2) : n(O2)=2 : 1[2SO2(g)+O2(g) 2SO3(g)],测得容器内总压强与反应时间如图1所示。
2SO3(g)],测得容器内总压强与反应时间如图1所示。

①下列说法不正确的是________;
A.T2>T1 B.该反应正向是吸热反应 C.增大压强一定以使平衡正向移动
D.其他条件不变,向平衡体系中再按物质的量之比为2 : 1充入SO2和O2,达到新的平衡后SO2平衡转化率增大
②图中B点的平衡常数Kp=__________________________(提示:用平衡分压代替平衡浓度计算,平衡分压=总压×物质的量分数)
③ 在压强为p1 MPa下,将2.0 mol SO2(g)和1.0 mol O2(g)充入容积为2 L的密闭容器中,反应达到平衡时,测得SO3气体的体积分数随温度的变化曲线如图所示,请在图中画出p2 MPa(p1<p2 )时平衡体系中SO3气体的体积分数随温度变化的曲线(表明p2 )。 ______________

(3)NH4Cl溶液呈酸性的原因(用相应离子方程式表示)______________________________;常温下,若用pH=3的盐酸滴定pH=11的氨水生成NH4Cl溶液,则用去两溶液的体积关系:V(盐酸)________V(氨水)(填“>”、“=”或“<”),滴定终点的判断:__________________。
-
研究NO2、SO2、CO等大气污染气体的处理及利用的方法具有重要意义。
(1)①已知:2SO2(g)+O2(g) 2SO3(g) ΔH=−196.6 kJ·mol–1
2SO3(g) ΔH=−196.6 kJ·mol–1
2NO(g)+O2(g) 2NO2(g) ΔH=−113.0 kJ·mol–1
2NO2(g) ΔH=−113.0 kJ·mol–1
请写出NO2与SO2反应生成SO3(g)和NO的热化学方程式 。
②一定条件下,将NO2与SO2以体积比1:2置于2L密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO2的同时生成1 molNO2
(2)工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO ( g ) + 2H2 ( g )  CH3OH ( g ) △H=-116kJ/mol
CH3OH ( g ) △H=-116kJ/mol
一定条件下在2L密闭容器中,将1 mol CO与3 mol H2的混合气体在催化剂作用下发生反应生成甲醇。
① 2min时测得生成CH3OH 0.2mol,则0~2min的平均反应速率v(H2)= 。
②反应5min后达到平衡,若平衡后将容器的容积压缩到原来的l/2,其他条件不变,对平衡体系产生的影响是 (填字母序号)。
a.c(H2)减少
b.正反应速率加快,逆反应速率减慢
c.CH3OH 的物质的量增加
d.重新平衡c(H2)/c(CH3OH)减小
(3)在密闭容器中充有1mol CO与2 mol H2,在催化剂作用下反应生成甲醇,CO的转化率(α)与温度(T)、压强(P) 的关系如图所示。
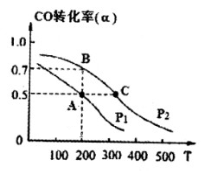
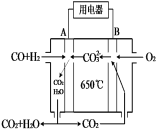
A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA tC(填“>”、“<”或“=”)。
② 若A点时容器的体积为1 L,则该温度下B的平衡常数 KB= ,C点的平衡常数KC KB(填“<”、“>”或“=”)。
(4)下图是MCFC燃料电池,它是以水煤气(CO、H2)为燃料,一定比例Li2CO3和Na2CO3共熔混合物为电解质。A为电池的 极(选填“正”或“负”),写出B极电极反应式 。
-
研究NO2、SO2、CO等大气污染气体的处理及利用的方法具有重要意义。
(1)①已知:2SO2(g)+O2(g) 2SO3(g) ΔH=−196.6 kJ·mol–1
2SO3(g) ΔH=−196.6 kJ·mol–1
2NO(g)+O2(g) 2NO2(g) ΔH=−113.0 kJ·mol–1
2NO2(g) ΔH=−113.0 kJ·mol–1
请写出NO2与SO2反应生成SO3(g)和NO的热化学方程式 。
②一定条件下,将NO2与SO2以体积比1:2置于2L密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO2的同时生成1 molNO2
(2)工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO ( g ) + 2H2 ( g )  CH3OH ( g ) △H=-116kJ/mol
CH3OH ( g ) △H=-116kJ/mol
一定条件下在2L密闭容器中,将1 mol CO与3 mol H2的混合气体在催化剂作用下发生反应生成甲醇。
① 2min时测得生成CH3OH 0.2mol,则0~2min的平均反应速率v(H2)= 。
②反应5min后达到平衡,若平衡后将容器的容积压缩到原来的l/2,其他条件不变,对平衡体系产生的影响是 (填字母序号)。
a.c(H2)减少
b.正反应速率加快,逆反应速率减慢
c.CH3OH 的物质的量增加
d.重新平衡c(H2)/c(CH3OH)减小
(3)在密闭容器中充有1mol CO与2 mol H2,在催化剂作用下反应生成甲醇,CO的转化率(α)与温度(T)、压强(P) 的关系如图所示。
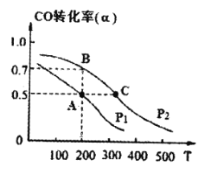

A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA tC(填“>”、“<”或“=”)。
② 若A点时容器的体积为1 L,则该温度下B的平衡常数 KB= ,C点的平衡常数KC KB(填“<”、“>”或“=”)。
(4)下图是MCFC燃料电池,它是以水煤气(CO、H2)为燃料,一定比例Li2CO3和Na2CO3共熔混合物为电解质。A为电池的 极(选填“正”或“负”),写出B极电极反应式 。
-
目前,对CO、NOx的综合利用是科学家研究的热点。回答下列问题:
(1)已知:N2(g)+O2(g)=2NO(g) ∆H1=+180.5kJ·mol-1
2CO(g)+O2(g)=2CO2(g) ∆H2=-566kJ·mol-1
2NO(g)+O2(g)=2NO2(g) ∆H3=-116.2kJ·mol-1
写出CO和NO2反应生成N2的热化学方程式:____。
(2)制备AlCl3的实际生产过程中,常加入足量的碳粉,反应后生成CO(g)。T℃时,向恒容密闭容器中加入3mol Al2O3(s)、8mol C(s)和3.3mol Cl2(g),发生反应。Cl2的浓度变化如图1所示;图2为20min后改变容器中条件,平衡体系的反应速率(v)随时间(t)的变化关系,且四个阶段都各改变一种不同的条件。

①容器中发生反应的化学方程式为___。
②0~15min内,该反应的平均速率v(CO)=___mol·L-1·min-1。
③T℃时,该反应的平衡常数K=___。
④15min时的平衡常数K(15)、44 min时的平衡常数K(44)与55min时的平衡常数K(55)的大小关系为____。
(3)N2O5在一定条件下可发生分【解析】
2N2O5(g) 4NO2(g)+O2(g)。一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是___(填标号)。
4NO2(g)+O2(g)。一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是___(填标号)。
A.容器中气体的密度不发生变化
B.NO2和O2的体积比保持不变
C.v正(NO2)=2v逆(N2O5)
D.气体的平均相对分子质量为43.2,且保持不变
-
氮和硫的氧化物的综合利用是目前研究的热点之一。已知:
i.N2(g)+O2(g)=2NO(g) △H=+180.0 kJ·mol-1
ii.2SO2(g)+O2(g)=2SO3(g) △H=-196.6 kJ·mol-1
iii.2NO(g)+O2(g)=2NO2(g) △H=-113.0 kJ·mol-1
(1)反应iV:2NO2(g)+2SO2(g)=2SO3(g)+N2(g)+O2(g)的 △H=________;该反应在密闭容器中达到平衡后,只改变下列条件,一定能使N2的平衡体积分数增大的是______(填选项字母)。
A 缩小容器容积 B 再充入SO2 C 降低温度 D 分离出SO3
(2)T1°C时,容积相等的密闭容器中分别充入NO2和SO2的混合气体4 mol,发生反应iV。NO2或SO2的平衡转化率(a)与起始充入的 关系如图1所示。
关系如图1所示。
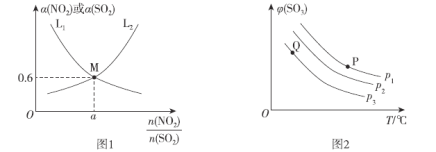
①图中能表示平衡时a(SO2)与起始充入的 关系的曲线为_____(填“L1”或“L2”)。
关系的曲线为_____(填“L1”或“L2”)。
②反应的平衡常数K=________。
(3)向密闭容器中充入一定量SO2和O2,发生反应ii。SO3的平衡体积分数(φ)与温度(T)和压强(p)的关系如图2所示。
①P1、P2 、P3由大到小的顺序为__________。
②P、Q两点对应状态下,单位体积内反应物活化分子数目:P__________Q(填“>”、“<”或“=”)。
-
研究NOx、SO2、CO等大气污染气体的处理方法具有重要意义,请回答下列问题:
(1)一定条件下,向一带活塞的密闭容器中充入2mol SO2和1mol O2发生反应,则下列说法正确的是 。
A.若反应速率v(SO2)﹦v(SO3),则可以说明该可逆反应已达到平衡状态
B.保持温度和容器体积不变,充入2mol N2,化学反应速率加快
C.平衡后仅增大反应物浓度,则平衡一定右移,各反应物的转化率一定都增大
D.平衡后移动活塞压缩气体,平衡时SO2、O2的百分含量减小,SO3的百分含量增大
E.保持温度和容器体积不变,平衡后再充入2mol SO3,再次平衡时各组分浓度均比原平衡时的浓度大
F.平衡后升高温度,平衡常数K增大
(2)若某温度下,SO2(g)+  O2(g)
O2(g) SO3(g) △H=-98 kJ/mol。开始时在100 L的密闭容器中加入4.0 mol SO2(g)和10.0 mol O2(g),当反应达到平衡时共放出196kJ的热量,该温度下的平衡常数K= (用分数表示)。在该温度下,分别将0.2mol/L 的SO2 和0.1mol/L O2放入固定体积的密闭容器中,当SO2转化率为60%时,该反应向 方向进行。
SO3(g) △H=-98 kJ/mol。开始时在100 L的密闭容器中加入4.0 mol SO2(g)和10.0 mol O2(g),当反应达到平衡时共放出196kJ的热量,该温度下的平衡常数K= (用分数表示)。在该温度下,分别将0.2mol/L 的SO2 和0.1mol/L O2放入固定体积的密闭容器中,当SO2转化率为60%时,该反应向 方向进行。
(3)在一个2L的密闭容器中充入一定量的SO3发生反应:其中SO3的变化如下图所示:从10 min起,压缩容器为1L,则SO3的变化曲 线为 (填图像中的字母序号)。
线为 (填图像中的字母序号)。
(4)反应N2O4(g) 2NO2(g);△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
2NO2(g);△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
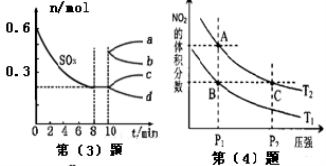
A.A、C两点的反应速率:A>C
B .A、C两点气体的颜色:A深,C浅
.A、C两点气体的颜色:A深,C浅
C.由状态B到状态A,可以用加热的方法
D.若P2>P1,则化学平衡常数KA>KC
(5)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574KJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160KJ/mol
请写出1molCH4还原NO2生成N2、CO2、H2O气态物质的热化学方程式 。
-
研究 NOx、SO2、CO 等大气污染气体的处理方法具有重要意义。
(1)处理含 CO、SO2 烟道气污染的一种方法是将其在催化剂作用下转化为单质 S。
已知:①CO(g)+ 1/2O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
②S(s)+ O2(g)=SO2(g) ΔH=-296.0kJ·mol-1
此反应的热化学方程式是___________________。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
① CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-akJ·mol-1 (a>0)
② 2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-bkJ·mol-1 (b>0)
若用标准状况下 3.36LCO 还原 NO2 至 N2(CO 完全反应)的整个过程中转移电子的物质的量为_______mol,放出的热量为_______ kJ(用含有 a 和 b 的代数式表示)。
(3)用 CH4 催化还原 NOx 也可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574kJ·mol-1 ①
CH4(g)+4NO (g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=?②
若 1molCH4 还原 NO2 至 N2 整个过程中放出的热量为 867kJ,则 ΔH2=_______ 。
(4)工业上一般用碱溶液来吸收 NO2,SO2。写出用氨水吸收过量 SO2 的离子方程式__________________ 。
-
研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:1molCO(g)与适量的SO2(g)反应生成S(s)和CO2(g)时,放出135kJ的热量,则此反应的热化学方程式为______________。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体,用CO(g)处理NO2(g)的能量转化关系如图所示。

标准状况下,22.4LCO和NO2发生上述反应。整个过程中,转移电子的物质的量为___________mol,放出的热量为___________kJ(用含有a的代数式表示)。
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ/mol
② CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2
若1molCH4(g)直接将NO2(g)还原至N2(g),整个过程中放出的热量为867kJ,则△H2=_____________。
-
研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:
①CO(g)+1/2O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
②S(s)+O2(g)=SO2(g) ΔH=-296.0kJ·mol-1
此反应的热化学方程式是___________________________。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
CO(g)+NO2(g) =NO(g)+CO2(g) ΔH=-akJ·mol-1(a>0)
2CO(g)+2NO(g) =N2(g)+2CO2(g) ΔH=-bkJ·mol-1(b>0)
若用标准状况下3.36LCO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为________mol,放出的热量为________kJ(用含有a和b的代数式表示)
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574kJ·mol-1①
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=?②
若1molCH4还原NO2至N2,整个过程中放出的热量为867kJ,则ΔH2=________

2NO2(g) ΔH1
2SO3(g) ΔH2 =-196.6 kJ·mol-1
CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4 kJ·mol-1
CaS(s)+4CO2(g) ΔH2=-175.6 kJ·mol-1












