-
利用氨水吸收烟气中的二氧化硫,其相关反应的主要热化学方程式如下:
SO2(g)+NH3·H2O(aq)===NH4HSO3(aq);ΔH1=a kJ·mol-1
NH3·H2O(aq)+NH4HSO3(aq)===(NH4)2SO3(aq)+H2O(l);ΔH2=b kJ·mol-1
2(NH4)2SO3(aq)+O2(g)===2(NH4)2SO4(aq);ΔH3=c kJ·mol-1
(1) 反应2SO2(g)+4NH3·H2O (aq)+O2(g)===2(NH4)2SO4(aq)+2H2O(l)的ΔH=_______kJ·mol-1。
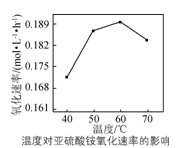
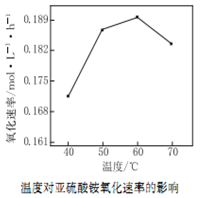
(2) 用空气氧化(NH4)2SO3的速率随温度的变化如右图所示,当温度超过60℃时,(NH4)2SO3氧化速率下降的原因可能是________。
(3)以磷石膏废渣和碳酸铵为原料制备硫酸铵,不仅解决了环境问题,还使硫资源获得二次利用。反应的离子方程式为CaSO4(s)+CO(aq)SO(aq)+CaCO3(s),该反应的平衡常数K=________。
[已知Ksp( CaCO3) =2.9×10-9,Ksp( CaSO4) =9.1×10-6]
(4) (NH4)2SO4在工农业生产中有多种用途。
① 将黄铜精矿(主要成分Cu2S)与硫酸铵混合后在空气中进行焙烧,可转化为硫酸铜同时产生氨气。该反应的化学方程式为________。
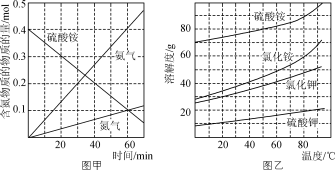
② 研究硫酸铵的分解机理有利于对磷石膏的开发。在500 ℃下硫酸铵分解过程中得到4种产物,其含氮物质随时间变化关系如图甲所示。写出该条件下硫酸铵分解的化学方程式,并用单线桥标出电子转移的方向及数目:________。
③ (NH4)2SO4是工业制备K2SO4的重要原料。根据图乙中相关物质的溶解度曲线,简述工业上制备K2SO4晶体的设计思路:________。
-
利用氨水吸收烟气中的二氧化硫,其相关反应的主要热化学方程式如下:
SO2(g)+NH3·H2O(aq)=NH4HSO3(aq) △H1=a kJ·mol-1
NH3·H2O(aq)+NH4HSO3(aq)=(NH4)2SO3(aq)+H2O(l) △H2=b kJ·mol-1
2(NH4)2SO3(aq)+O2(g)=2(NH4)2SO4(aq) △H3=c kJ·mol-1
(1)反应2SO2(g)+4NH3·H2O(aq)+O2(g)=2(NH4)2SO4(aq)+2H2O(l)的△H= kJ·mol-1。
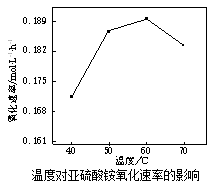
(2)空气氧化(NH4)2SO3的速率随温度的变化如图所示,当温度超过60 ℃时,(NH4)2SO3氧化速率下降的原因可能是 。
(3)以磷石膏废渣和碳酸铵为原料制备硫酸铵,不仅解决了环境问题,还使硫资源获得二次利用。反应的离子方程式为CaSO4(s)+CO32—(aq) SO42—(aq)+CaCO3(s),该反应的平衡常数K= 。
SO42—(aq)+CaCO3(s),该反应的平衡常数K= 。
[ 已知Ksp(CaCO3)=2.9×10-9,Ksp(CaSO4)=9.1×10-6 ]
(4)(NH4)2SO4在工农业生产中有多种用途。
①将黄铜精矿(主要成分Cu2S)与硫酸铵混合后在空气中进行焙烧,可转化为硫酸铜同时产生氨气。该反应的化学方程式为 。
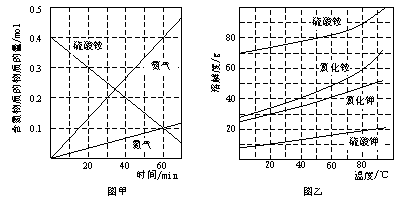
②研究硫酸铵的分解机理有利于对磷石膏的开发。在500 ℃下硫酸铵分解过程中得到4种产物,其含氮物质随时间变化关系如图甲所示。写出该条件下硫酸铵分解的化学方程式,并用单线桥标出电子转移的方向及数目: 。
③(NH4)2SO4是工业制备K2SO4的重要原料。根据图乙中相关物质的溶解度曲线,简述工业上制备K2SO4晶体的设计思路: 。
-
利用氨水吸收烟气中的二氧化硫,其相关反应的主要热化学方程式如下:
SO2(g)+NH3·H2O(aq)=NH4HSO3(aq) △H1=a kJ·mol-1
NH3·H2O(aq)+NH4HSO3(aq)=(NH4)2SO3(aq)+H2O(l) △H2=b kJ·mol-1
2(NH4)2SO3(aq)+O2(g)=2(NH4)2SO4(aq) △H3=c kJ·mol-1
⑴反应2SO2(g)+4NH3·H2O(aq)+O2(g)=2(NH4)2SO4(aq)+2H2O(l)的 △H=_____kJ·mol-1。
⑵空气氧化(NH4)2SO3的速率随温度的变化如图所示,当温度超过60℃时,(NH4)2SO3氧化速率下降的原因可能是_______。
⑶以磷石膏废渣和碳酸铵为原料制备硫酸铵,不仅解决了环境问题,还使硫资源获得二次利用。反应的离子方程式为CaSO4(s)+CO32—(aq)SO42—(aq)+CaCO3(s),该反应的平衡常数 K=____。 [已知Ksp(CaCO3)=2.9×10-9,Ksp(CaSO4)=9.1×10-6 ]
⑷(NH4)2SO4在工农业生产中有多种用途。
①将黄铜精矿(主要成分Cu2S)与硫酸铵混合后在空气中进行焙烧,可转化为硫酸铜同时产生氨气。该反应的化学方程式为________。
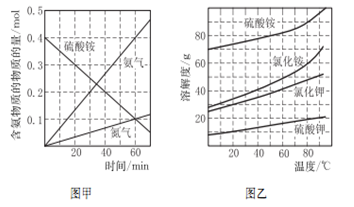
②研究硫酸铵的分解机理有利于对磷石膏的开发。在500℃下硫酸铵分解过程中得到4种产物,其含氮物质随时间变化关系如图甲所示。写出该条件下硫酸铵分解的化学方程式,并用单线桥标出电子转移的方向及数目:_____________。
③(NH4)2SO4是工业制备K2SO4的重要原料。根据图乙中相关物质的溶解度曲线,简述工业上制备K2SO4晶体的设计思路:___________。
-
有效脱除烟气中的SO2是环境保护的重要课题。
(1)氨水可以脱除烟气中的SO2。氨水脱硫的相关热化学方程式如下:
2NH3(g) +H2O(l) +SO2(g) =(NH4)2SO3(aq) ΔH= akJ·mol−1
(NH4)2SO3(aq)+H2O(l) +SO2(g) =2NH4HSO3(aq) ΔH = bkJ·mol−1
2(NH4)2SO3(aq) +O2(g) =2(NH4)2SO4(aq) ΔH =ckJ·mol−1
反应NH3(g) +NH4HSO3(aq) + O2(g) = (NH4)2SO4(aq)的ΔH=____kJ·mol−1。
O2(g) = (NH4)2SO4(aq)的ΔH=____kJ·mol−1。
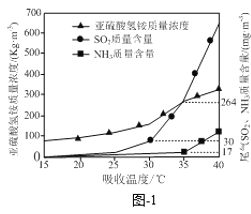
已知:SO2的国家排放标准为80mg·m−3。氨水脱除烟气中的SO2是在吸收塔中进行的,控制其他实验条件相同,仅改变吸收塔的温度,实验结果如题图-1所示,为了尽可能获得NH4HSO3,则吸收塔合适的温度约为________。
A.25℃ B.31℃ C.35℃
(2)电解法可以脱除烟气中的SO2。用Na2SO4溶液吸收烟气中的SO2,使用惰性电极电解吸收后的溶液,H2SO3在阴极被还原为硫单质,阴极的电极反应式为_______。
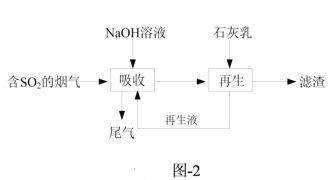
(3)钠钙双碱法可高效脱除烟气中的SO2,脱硫的流程如题图-2所示。
①“吸收”时气液逆流在吸收塔中接触,吸收时不宜直接使用石灰乳的原因是_______。
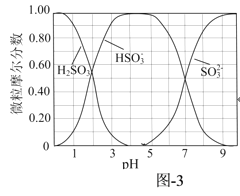
②水溶液中H2SO3、HSO 、SO
、SO 随pH的分布如题图−3所示,“再生液”用NaOH溶液调pH至7~9得到溶液X,溶液X吸收SO2时主要反应的离子方程式为______。
随pH的分布如题图−3所示,“再生液”用NaOH溶液调pH至7~9得到溶液X,溶液X吸收SO2时主要反应的离子方程式为______。
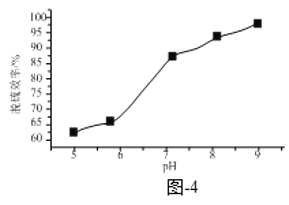
③已知Na2SO3的溶解度随着pH增大而减小。溶液X的pH对脱硫效率的影响如题图-4所示。当pH由6升高到7时,脱硫效率迅速增大的原因为______;当pH大于7时,随pH增大脱硫效率增速放缓的原因为______。
-
通过以下反应可以除去烟气中的二氧化硫,并获得氮肥。下列说法不正确的是
①SO2(g)+NH3·H2O(aq) = NH4HSO3(aq) △H1=akJ·mol-1
②NH3·H2O(aq)+NH4HSO3(aq) = (NH4)2SO3(aq)+H2O(l) △H2=bkJ·mol-1
③2(NH4)2SO3(ap)+O2(g) = 2(NH4)2SO4(aq) △H3=ckJ·mol-1
A. 反应①是吸收烟气中二氧化硫的方法之一
B. 反应③是将还原性较强的(NH4)2SO3转化为较稳定的铵盐作氮肥
C. 2NH3·H2O(aq)+2NH4HSO3(aq)=2 (NH4)2SO3(aq)+2H2O(g) △H2=2bkJ·mol-1
D. 反应2SO2(g)+4NH3·H2O(aq)+O2(g) = 2(NH4)2SO4(aq)+2H2O(l)的△H=(2a+2b+c)kJ·mol-1
-
汽车尾气的主要成分有CO、SO2、NO、NO2等。
(1)利用氨水可以将SO2、氮氧化物吸收,原理如下图所示。
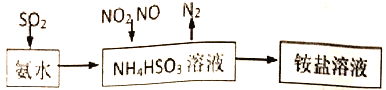
①25℃时,在pH=5的 NH4HSO3溶液中,c(SO32-)+c(NH3·H2O)-c(H2SO3)=__________mol/L(填确值)
②请写出NO2和NO按体积比1:1被吸收时反应的离子方程式_____________________。
(2)科研工作者目前正在尝试以二氧化钛(TiO2)催化分解汽车尾气的研究。
①已知:2NO(g)+O2(g)=2NO2(g) △H1=-113.0kJ·mol-1
3NO2(g)+H2O(g)=2HNO3(g)+NO(g) △H2=-138.0 kJ·mol-1
TiO2催化尾气降解原理可表示为:2COg)+O2(g) 2CO2(g) △H3
2CO2(g) △H3
则2H2O(g)+4NO(g)+3O2(g) 4HNO3(g) △H4=______________________。
4HNO3(g) △H4=______________________。
②在O2、H2O(g)浓度一定条件下,模拟CO、NO的降解,得到其降解率(即转化率)如图1所示。请解释T1后NO降解率下降的可能原因______________________。
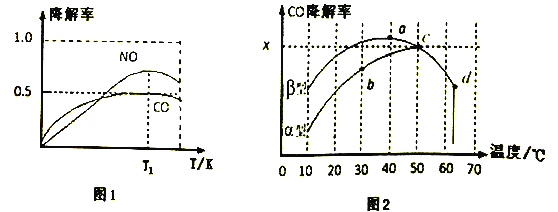
(3)沥青混凝土也可降解CO。如图2为在不同颗粒间隙的沥青混凝土(α、β型)在不同温度下,反应相同时间,测得CO降解率变化。结合如图回答下列问题:
①已知在50℃时在α型沥青混凝土容器中,平衡时O2浓度为0.01mol·L-1,求此温度下CO降解反应的平衡常数____________________________________________。(用含x的代数式表示)
②科研团队以β型沥青混凝土颗粒为载体,将TiO2改为催化效果更好的TiO2纳米管,在10℃~60℃范围内进行实验,请在如图中用线段与“ ”阴影描绘出CO降解率随温度变化的曲线可能出现的最大区域范围(在图中画出)。____________
”阴影描绘出CO降解率随温度变化的曲线可能出现的最大区域范围(在图中画出)。____________
(4)TiO2纳米管的制备是在弱酸性水溶液中以金属钛为阳极进行电解,写出阳极的电极反应式____________________________________________。
-
燃煤烟气中的SO2、NOx是形成酸雨的有害物质。应设法吸收利用。
I.吸收SO2:通入氨水将其转化为NH4HSO3,NH4HSO3溶液呈_____性(填“酸”、“碱”、“中”);再通空气将NH4HSO3氧化,溶液pH将__________(填“增大”、“减小”、“不变”)
Ⅱ.处理NO:先用O3处理,再用Na2SO3溶液吸收。O3处理的热化学方程式为:
NO(g)+O3(g)=NO2(g)+O2(g) △H=akJ·mol-1
NO2(g)=NO(g)+1/2O2(g) △H=bkJ·mol-1
(1)反应NO(g)+O3(g)=3NO2(g)的△H=_______kJ·mol-1。
(2)用Na2SO3溶液吸收时,溶液中SO32-将NO2转化为NO2-,反应的氧化产物是_________。
Ⅲ.利用SO2:分离出SO2可用于生产硫酸,反应之一:2SO2(g)+O2(g) 2SO3(g) △H<0。
2SO3(g) △H<0。
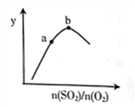
(3)恒温恒容下,改变SO2、O2的物质的量之比[n(SO2)/n(O2)],平衡时测定Y的值,Y与[n(SO2)/n(O2)]的关系如图所示,则Y可能是______________。
A.正反应速率 B.SO3的体积分数 C.SO2的转化率 D.SO2的体积分数
a→b段y变化的原因是___________。
(4)Kp是以各气体平衡分压(各气体的分压=总压×各气体的体积分数)代替平衡浓度表示的平衡常数。
①Kp与温度(T/K)的关系是㏒Kp= -4.86(R为常数),请判断R___0(填“>”或“<”),原因是________。
-4.86(R为常数),请判断R___0(填“>”或“<”),原因是________。
②在10.0%SO2、13.5%O2、76.5%N2(体积分数)时,SO2平衡转化率与温度、压强的关系如图。
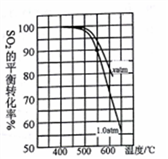
则x_____1.0(填“>”或“<”);计算550℃、1.0atm下,2SO2(g)+O2(g) 2SO3(g)的Kp=____。(精确到1位小数)
2SO3(g)的Kp=____。(精确到1位小数)
-
造成酸雨的主要物质是NO2和SO2,某科研小组进行如下研究。
(1)处理二氧化硫通常是先在水中把它氧化成硫酸,再用NH3·H2O吸收。
已知2NH3·H2O (aq) + H2SO4(aq)==(NH4)2SO4(aq)+ 2H2O(l) △H=-24.2kJ/mol,中和热△H=-57.3 kJ/mol则1mol NH3·H2O理论上完全电离时需要吸收的热量为________。
(2)常温下也可以用NaOH溶液直接吸收SO2,在吸收过程中,溶液pH随n(SO32-):n(HSO3-)变化关系如下表:
| n(SO32-):n(HSO3-) | 88:12 | 1:1 | 12:88 |
| pH | 8.2 | 7.4 | 6.0 |
①当吸收液呈中性时,溶液中离子浓度由大到小排列顺序为___________。
②当向NaOH溶液中通入足量的SO2时,得到NaHSO3溶液,在pH为4~7之间电解,硫元素在阴极上被还原为Na2S2O4,这是电化学脱硫技术之一。写出该阴极的电极反应式_______。
(3)向容积为2L,密闭容器中分别充入0.20molNO2和0.4mol SO2,发生SO2(g)+NO2(g)  SO3(g)+NO(g) △H=-41.8 kJ/mol 在不同温度下测定同一时刻NO2的转化率,结果如下图所示。
SO3(g)+NO(g) △H=-41.8 kJ/mol 在不同温度下测定同一时刻NO2的转化率,结果如下图所示。
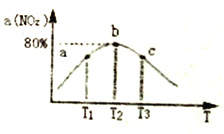
①a、c两点反应速率大小关系: v(a) ___v(c)。(填“>”、“<” 或“=”)
②温度为T2时从反应开始经过2min 达到b点,用SO3表示这段时间的反应速率为______,此温度下该反应的平衡常数为_______。若在此温度下,保持容器的容积不变,再向容器中充入0.10molNO2和0.2molSO2,NO2的转化率_______(填“增大”、“减小”或“不变”).
③NO2的转化率随温度升高先增大后减小的原因是____________。
-
造成酸雨的主要物质是NO2和SO2,某科研小组进行如下研究。
(1)处理二氧化硫通常是先在水中把它氧化成硫酸,再用NH3•H2O吸收。已知2NH3•H2O(aq)+H2SO4(aq)=(NH4)2SO4(aq)+2H2O(l) ΔH=-24.2kJ/mol,中和热ΔH=-57.3kJ/mol则1molNH3•H2O理论上完全电离时需要吸收的热量为___。
(2)常温下也可以用NaOH溶液直接吸收SO2,在吸收过程中,溶液pH随n(SO32-):n(HSO3-)变化关系如下表:
| n(SO32-):n(HSO3-) | 88:12 | 1:1 | 12:88 |
| pH | 8.2 | 7.4 | 6.0 |
①当吸收液呈中性时,溶液中离子浓度由大到小排列顺序为___。
②当向NaOH溶液中通入足量的SO2时,得到NaHSO3溶液,在pH为4∼7之间电解,硫元素在阴极上被还原为Na2S2O4,这是电化学脱硫技术之一。写出该阴极的电极反应式___。
(3)向容积为2L,密闭容器中分别充入0.20molNO2和0.4molSO2,发生SO2(g)+NO2(g)⇌SO3(g)+NO(g) ΔH=-41.8kJ/mol在不同温度下测定同一时刻NO2的转化率,结果如图所示。
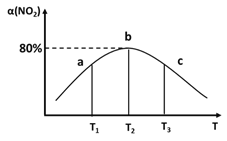
①a、c两点反应速率大小关系:v正(a)___v逆(c)。(填“>”“<”或“=”)
②温度为T2时,该反应的平衡常数为___。若在此温度下,保持容器的容积不变,再向容器中充入0.10molNO2和0.2molSO2,NO2的转化率___(填“增大”“减小”或“不变”)。
-
下列反应的离子方程式书写不正确的是( )
A. 向氯化铝溶液中加入过量的氨水:Al3++3NH3·H2O= Al(OH)3↓+3NH4+
B. 用氨水吸收过量的二氧化硫:NH3·H2O+SO2 = NH4+ +HSO3-
C. 向偏铝酸钠溶液中加入过量的稀盐酸:AlO2-+H++H2O= Al(OH)3↓
D. 向次氯酸钠溶液中通入少量二氧化碳:2ClO-+CO2+H2O=2HClO +CO32-















