-
已知25℃时:①HF(aq)+OH-(aq)===F-(aq)+H2O(l) ΔH1=-67.7 kJ·mol-1
②H+(aq)+OH-(aq)===H2O(l) ΔH2=-57.3 kJ·mol-1
③Ba2+(aq)+SO42-(aq)===BaSO4(s) ΔH3<0
下列说法正确的是
A.HF的电离方程式及热效应:HF(aq)===H+(aq)+F-(aq) ΔH>0
B.在氢氧化钠溶液与盐酸的反应中,盐酸量一定,氢氧化钠溶液量越多,中和热越大
C.ΔH2=-57.3 kJ·mol-1是强酸和强碱在稀溶液中反应生成可溶盐的中和热
D.稀硫酸与稀氢氧化钡溶液反应的热化学方程式为:H2SO4(aq)+Ba(OH)2(aq)===BaSO4(s)+ 2H2O(l)ΔH=-114.6 kJ·mol-1
-
已知25℃时:①H+(aq)+OH-(aq)=H2O(l) △H1=-57.3kJ/mol
②HF(aq)+OH-(aq)=F-(aq)+H2O(l) △H2=-67.7kJ/mol
③Ba2+(aq)+SO42-(aq)=BaSO4(s) △H3<0
下列说法正确的是( )
A.△H1=-57.3kJ/mol是强酸和强碱在稀溶液中反应生成可溶性盐的中和热
B.在氢氧化钠溶液与盐酸的反应中,盐酸量一定,氢氧化钠溶液量越多,中和热越大
C.HF的电离方程式及热效应:HF(aq) H+(aq)+F-(aq) △H>0
H+(aq)+F-(aq) △H>0
D.稀硫酸与稀氢氧化钡溶液反应的热化学方程式为
H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) △H=-114.6kJ/mol
-
已知25℃时: ①HF(aq)+OH-(aq)=F-(aq)+H2O(l)△H1=-67.7kJ•mol-1
②H+(aq)+OH-(aq)=H2O(l)△H2=-57.3kJ•mol-1
③Ba2+(aq)+SO42-(aq)=BaSO4(s)△H3<0
下列说法正确的是( )
A. HF的电离方程式及热效应:HF(aq)⇌H+(aq)+F-(aq)△H>0
B. 在氢氧化钠溶液与盐酸的反应中,氢氧化钠溶液量越多,中和热越大
C. △H2=-57.3kJ•mol-1是强酸和强碱在稀溶液中反应生成可溶盐的中和热
D. 稀硫酸与稀氢氧化钡溶液反应的热化学方程式为 H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)△H=-114.6kJ•mol-1
-
已知25℃时:
①HF(aq)+OH-(aq)=F-(aq)+H2O(l)ΔH1=-67.7kJ·mol-1
②H+(aq)+OH-(aq)=H2O(l)ΔH2=-57.3kJ·mol-1
③Ba2+(aq)+SO42—(aq)=BaSO4(s)ΔH3<0
下列说法正确的是( )
A.HF的电离方程式及热效应:HF(aq) H+(aq)+F-(aq) ΔH>0
H+(aq)+F-(aq) ΔH>0
B.在氢氧化钠溶液与盐酸的反应中,氢氧化钠溶液量越多,中和热越大
C.ΔH2=-57.3 kJ·mol-1是强酸和强碱在稀溶液中反应生成可溶盐的中和热
D.稀硫酸与稀氢氧化钡溶液反应的热化学方程式为H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)ΔH=-114.6 kJ·mol-1
-
氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25℃时:
①HF(aq)+OH﹣(aq)⇌H2O(l)+F﹣(aq)△H=﹣67.7kJ/mol;
②H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJ/mol。
在20mL0.1mol/L的氢氟酸中滴加0.1mol/L的NaOH V mL,下列说法正确的是( )
A.氢氟酸的电离方程式及热效应可表示为:HF(aq)⇌H+(aq)+F﹣(aq)△H=+10.4kJ/mol
B.当V=20 mL时,溶液中:c(OH﹣)=c(HF)+c(H+)
C.当V=20 mL时,溶液中:c(F﹣)=c(Na+)=0.1mol/L
D.当V>0时,溶液中一定存在c(Na+)>c(F﹣)>c(OH﹣)>c(H+)
-
氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25℃时
①HF(aq)+OH—(aq)=F—(aq)+H2O(l) △H=−67.7KJ·mol—1
②H+(aq)+OH—(aq)=H2O(l) △H=−57.3KJ·mol—1
在20mL0.1·molL—1氢氟酸中加入VmL0.1mol·L—1NaOH溶液,下列有关说法正确的是
A.氢氟酸的电离方程式及热效应可表示为:HF(aq)=H+(aq) +F−(aq) △H=+10.4KJ·mol—1
B.当V=20时,溶液中:c(OH—)=c(HF) +c(H+)
C.当V=20时,溶液中:c(F—)<c(Na+)=0.1mol·L—1
D.当V>20时, 溶液中一定存在:c(Na+)>c(F—)>c(OH—)>c(H+)
-
已知:①H+(aq)+OH-(aq)===H2O(l) ΔH1=-57.3 kJ·mol-1,
②H2(g)+ O2(g)===H2O(g) ΔH2=-241.8 kJ·mol-1,下列有关说法正确的是
O2(g)===H2O(g) ΔH2=-241.8 kJ·mol-1,下列有关说法正确的是
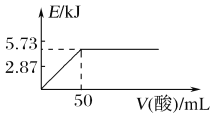
A. 向含0.1 mol NaOH的溶液中加入一定体积的0.1 mol·L-1乙二酸,反应中的能量变化如上图所示
B. H2SO4(aq)+Ba(OH)2(aq)===BaSO4(s)+2H2O(l) ΔH=-114.6 kJ·mol-1
C. 氢气的标准燃烧热为241.8 kJ·mol-1
D. 若反应②中水为液态,则同样条件下的反应热:ΔH>ΔH2
-
已知反应:①101kPa时,C(s) + 1/2O2(g)=CO(g);△H1=-110.5kJ/mol
②稀溶液中,H+(aq) + OH-(aq)=H2O(1);△H2=-57.3kJ/mol
下列结论正确的是
A.若碳的燃烧热用△H3来表示,则△H3<△H1
B.若碳的燃烧热用△H3来表示,则△H3>△H1
C.浓硫酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
-
已知反应:①101kPa时,C(s) + 1/2O2(g)=CO(g) △H1=-110.5kJ/mol
②稀溶液中,H+(aq) + OH-(aq)=H2O(1) △H2=-57.3kJ/mol
下列结论正确的是( )
A.若碳的燃烧热用△H3来表示,则△H3<△H1
B.若碳的燃烧热用△H3来表示,则△H3>△H1
C.浓硫酸与稀NaOH溶液反应的中和热为57.3kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
-
已知反应:①101kPa时,C(s) + 1/2O2(g)=CO(g);△H1=-110.5kJ/mol
②稀溶液中,H+(aq) + OH-(aq)=H2O(1);△H2=-57.3kJ/mol
下列结论正确的是 ( )
A.若碳的燃烧热用△H3来表示,则△H3<△H1
B.若碳的燃烧热用△H3来表示,则△H3=△H1
C.浓硫酸与稀NaOH溶液反应的中和热为-57.3kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
H+(aq)+F-(aq) △H>0
