在密闭容器中发生可逆反应4NH3+5O24NO+6H2O(g),以下是不同情况下的反应速率,其中最快的是
A.v(O2)=0.001mol/(L·S)
B.v(NH3)=0.002 mol/(L·S)
C.v(H2O)=0.003 mol/(L·h)
D.v(NO)=0.008 mol/(L·S)
高三化学选择题极难题
在密闭容器中发生可逆反应4NH3+5O24NO+6H2O(g),以下是不同情况下的反应速率,其中最快的是
A.v(O2)=0.001mol/(L·S)
B.v(NH3)=0.002 mol/(L·S)
C.v(H2O)=0.003 mol/(L·h)
D.v(NO)=0.008 mol/(L·S)
高三化学选择题极难题
在密闭容器中发生可逆反应4NH3+5O24NO+6H2O(g),以下是不同情况下的反应速率,其中最快的是
A.v(O2)=0.001mol/(L·S)
B.v(NH3)=0.002 mol/(L·S)
C.v(H2O)=0.003 mol/(L·h)
D.v(NO)=0.008 mol/(L·S)
高三化学选择题极难题查看答案及解析
对于反应:4NH3(g) + 5O2(g) 4NO(g) + 6H2O(g), 下列为四种不同情况下测得的反应速率,其中能表明该反应进行最快的是
A.v(NH3)= 0.2mol·L-1·s-1
B.v(O2 )= 0.24 mol·L-1·s-1
C.v(H2O )= 0.25 mol·L-1·s-1
D.v(NO) = 0.15 mol·L-1·s-1
高三化学选择题简单题查看答案及解析
反应 4NH3+5O24NO+6H2O 在5L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率
x(
x表示反应物的消耗速率或生成物的生成速率)为 ( )
A.(NH3)= 0.002mol/(L·s) B.
(O2)= 0.01mol/(L·s)
C.(NO)= 0.008mol/(L·s) D.
(H2O)= 0.003mol/(L·s)
高三化学选择题中等难度题查看答案及解析
对在密闭容器中进行的可逆反应:4NH3(g)+5O24NO(g)+6H2O(g),下列叙述正确的是
A.反应达到平衡时,若两种反应物的转化率相等,则起始投入的n(NH3)∶n(O2)=1∶1
B.反应达到平衡后,再向体系中充入O2,将提高NH3的转化率
C.反应达到平衡时,若向体系中充入稀有气体,速率增大
D.当v正(NH3):v正(NO)=1∶1时,说明该化学反应已经达到平衡
高三化学单选题中等难度题查看答案及解析
高三化学选择题中等难度题查看答案及解析
已知反应4NH3(g)+5O2(g)==4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了4.5mol,试计算分别用NH3、O2、NO、H2O四种不同物质表示的该反应的反应速率。
高三化学填空题中等难度题查看答案及解析
固定体积的密闭容器中,发生:4NH3(g)+5O2(g)4NO(g)+6H2O(g),能判断该反应达到平衡状态的依据是
A.5υ正(O2)=4υ逆(NO) B.容器内气体密度不再变化
C.c(NH3)不再变化 D.c(NH3)=1.5c(H2O)
高三化学单选题中等难度题查看答案及解析
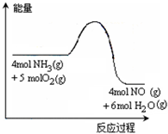
在一定条件下密闭容器中发生: 4NH3(g) + 5O2(g) 4NO (g)+ 6H2O(g)
反应过程中能量变化如图所示;下列说法正确的是
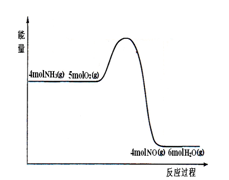
A.由图可知,该反应的正反应是吸热反应
B.升高温度可以提高NH3的转化率
C.反应体系中加入催化剂可增加反应热
D.将平衡混合物通入水中一定有硝酸铵生成
高三化学选择题中等难度题查看答案及解析
反应4NH3+5O2 4NO+6H2O在5 L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3 mol,则此反应的平均速率
(表示反应物的消耗速率或生成物的生成速率)为( )
A. = 0.01 mol / (L·s) B.
= 0.008 mol / (L·s)
C. = 0.003 mol / (L·s) D.
= 0.004 mol / (L·s)
高三化学选择题中等难度题查看答案及解析
反应4NH3(气)+5O2(气) 4NO(气)+6H2O(气)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率
(X)(反应物的消耗速率或产物的生成速率)可表示为
A.(NH3) = 0.010 mol/(L·s)
B. (O2) = 0.0010 mol/(L·s)
C. (NO) = 0.0010 mol/(L·s)
D. (H2O) = 0.045 mol/(L·s)
高三化学选择题中等难度题查看答案及解析