-
碳酸钠是一种重要的化工原料,主要采用氨碱法生产。回答下列问题:
(1)碳酸钠俗称________,可作为碱使用的原因是___________(用离子方程式表示)。
(2)已知:①2NaOH(s)+CO2(g)=Na2CO3(s)+H2O(g) ΔH1=−127.4 kJ·mol−1
②NaOH(s)+CO2(g)= NaHCO3(s) ΔH1=−131.5 kJ·mol−1
反应2NaHCO3 (s)= Na2CO3(s)+ H2O(g) +CO2(g)的ΔH=_______ kJ·mol−1,该反应的平衡常数表达式K=________。
(3)向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中 =_____________(保留三位有效数字)。已知Ksp(BaCO3)=2.6×10−9,Ksp(BaSO4)=1.1×10−10。
=_____________(保留三位有效数字)。已知Ksp(BaCO3)=2.6×10−9,Ksp(BaSO4)=1.1×10−10。
(4)已知室温时,Ksp[Mg(OH)2]=4.0×10−11。在0.1 mol/L的MgCl2溶液中,逐滴加入NaOH溶液,当Mg2+完全沉淀时,溶液的pH是_____________(已知lg2=0.3) 。
-
CO2是一种重要的化工原料,依据题给信息,回答下列问题:
Ⅰ.碳酸钠可利用CO2采用氨碱法生产
(1)碳酸钠可作为碱使用的原因是_____________(用离子方程式表示)。
(2)已知:①2NaOH(s)+CO2(g)=Na2CO3(s)+H2O(g) ΔH1=−127.4 kJ/mol
②NaOH(s)+CO2(g)=NaHCO3(s) ΔH2=−131.5kJ/mol
反应2NaHCO3(s)=Na2CO3(s)+ H2O(g) +CO2(g)的ΔH=___________ kJ/mol。
Ⅱ.在体积为2 L的密闭容器中,充入1mol/LCO2 和1mol/L H2,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | | | 800 | | 830 | 1000 | 1200 |
| K | 0.6 | | | 0.9 | | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应为____________反应(选填吸热、放热)。
(2)能判断该反应是否达到化学平衡状态的依据是_______________。
a.容器中压强不变 b.混合气体中 c(CO)不变
c. υ正(H2)=υ逆(H2O) d. c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为____________℃。
(4)某温度下经2min反应达到平衡后c(CO)=0.8mol/L,此温度下的平衡常数为________。
-
I.碳酸钠是一种重要的化工原料,主要采用氨碱法生产。回答下列问题:
(1)已知:①2NaOH(s)+CO2(g)=Na2CO3(s)+H2O(g) ΔH1=−127.4kJ/mol
②NaOH(s)+CO2(g) = NaHCO3(s) ΔH2=−131.5kJ/mol
反应2NaHCO3(s)=Na2CO3(s) +H2O(g) +CO2(g)的ΔH=____kJ/mol,不同温度下NaHCO3分解反应的平衡常数K313K____K298K(填“大于"“小于”或“等于”),该反应的平衡常数表达式K=______。
(2)向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时溶液中 =____。(保留一位小数,已知Ksp(BaCO3)=2.6×10−9 ,Ksp(BaSO4)=1.1×10−10)
=____。(保留一位小数,已知Ksp(BaCO3)=2.6×10−9 ,Ksp(BaSO4)=1.1×10−10)
II.Mg﹣H2O2电池可用于驱动无人驾驶的潜航器,该电池以海水为电解质溶液,其工作原理如图所示,电池总反应是:Mg+H2O2+2H+═ Mg2++2H2O

(1)负极材料为_____,发生___反应(填“氧化”或“还原”)
(2)两极电极反应式为:
负极:_________________;正极:_________________;
(3)有4.8gMg反应时时,外电路中转移电子数为______。
-
纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。请按要求回答问题:
(1)“氨碱法”产生大量CaCl2废弃物,请写出该工艺中产生CaCl2的化学方程式:___________________________。
(2)写出“联合制碱法”有关反应的化学方程式:_______________________
(3)CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?_______________________。
(4)绿色化学的重要原则之一是提高反应的原子利用率。根据“联合制碱法”总反应列出计算原子利用率的表达式:原子利用率(%)=_________________。
-
工业上用粗盐(含Ca2+、Mg2+、 等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,工艺流程如下图所示,下列有关说法正确的是( )
等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,工艺流程如下图所示,下列有关说法正确的是( )
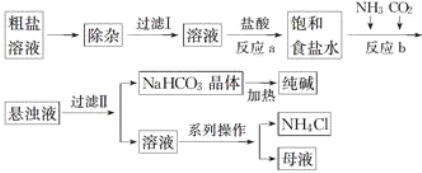
A. 在“侯氏制碱法”中涉及到了氧化还原反应
B. 饱和食盐水中先通入的气体为CO2
C. 流程图中的系列操作中一定需要玻璃棒
D. 工艺中只有碳酸氢钠加热分解产生的CO2可回收循环利用
-
下列说法正确的是
A.联合制碱法的优点是减少了对设备的腐蚀
B.工业生产硫酸时,用98%硫酸的来吸收三氧化硫,可以避免形成酸雾并提高吸收率
C.合成氨是天然固氮的方法之一
D.碳酸钠俗称小苏打,甲烷是一种清洁能源
-
(10分)某化学小组欲以CO2主要为原料,采用下图所示装置模拟“侯氏制碱法”制取NaHCO3,并对CO2与NaOH的反应进行探究。请你参与并完成对有关问题的解答。
【资料获悉】
1、“侯氏制碱法”原理:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl,然后再将NaHCO3制成Na2CO3。
2、Na2CO3与盐酸反应是分步进行:Na2CO3先与盐酸反应生成NaHCO3;然后再发生NaHCO3+HCl= NaCl+H2O +CO2↑
【实验设计】

【实验探究】
(1)装置乙的作用是 。
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有 、洗涤、灼烧。NaHCO3转化为Na2CO3的化学方程式为 。
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,取加热了t1 min的NaHCO3样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中有关离子的物质的量的变化如下图所示。
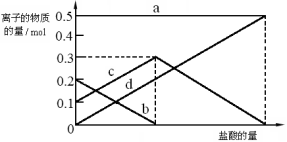
则曲线c对应的溶液中的离子是 (填离子符号);该样品中NaHCO3和Na2CO3的物质的量之比是 。
(4)若将装置甲产生的纯净的CO22.24L(标准状况下)通入100mLNaOH溶液中,充分反应后,将溶液小心蒸干,得到不含结晶水的固体W,其质量为10.16g,则W的成分为 (填化学式),原NaOH溶液的物质的量浓度为 。
-
(1)碳酸钠俗称纯碱,可作为碱使用的原因是__________________(用离子方程式表示)。
(2)25℃时,pH均为11的 NaOH 溶液和Na2CO3溶液中,水电离的OH-浓度之比是_____
(3)在0.1 mol·L-1的Na2CO3溶液中,下列粒子浓度关系式正确的是________。
A.[CO32-]+[HCO3-]=0.1 mol·L-1
B.[CO32-]+[HCO3-]+[H2CO3]=0.1 mol·L-1
C.[OH-]=[H+]+[HCO3-]
D.[Na+]+[OH-]=[H+]+[HCO3-]
(4)常温下0.1 mol·L-1的Na2CO3溶液中,离子浓度由大到小的顺序是__________________________________。
(5)向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时溶液中 =__________。(已知Ksp(BaCO3)=2.6×10−9,Ksp(BaSO4)=1.1×10−10,结果保留一位小数)
=__________。(已知Ksp(BaCO3)=2.6×10−9,Ksp(BaSO4)=1.1×10−10,结果保留一位小数)
-
化学与生活密切相关。下列说法错误的是
A. 硅酸钠的水溶液俗称水玻璃,是制备硅胶和木材防火剂的原料
B. 铜盐溶液都有毒,主要是由于铜离子能使蛋白质变性
C. 沼气的使用、玉米制乙醇都涉及生物质能的利用
D. 酸雨被称为“天堂的眼泪”,某雨水样品放置一段时间后,pH由 4.68变为 4.00,是因为水中溶解的 CO2增多
-
氯气是重要的化工原料。

(1)工业上常用 法生产氯气,写出发生反应的化学方程式 。
(2)工业上常用石灰乳和氯气反应制取漂白粉,使用石灰乳而不用石灰水的原因是 。部分流程如图所示,其主要设备是氯化塔,塔从上到下分四层.将含有3%~6%水分的熟石灰从塔顶喷洒而入,氯气从塔的最底层通入,这样加料的目的是 。
(3)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是 ,其原因可能是 ,由此可知(2)中氯化塔设计为四层是为了减少生产中类似副反应的发生。
=_____________(保留三位有效数字)。已知Ksp(BaCO3)=2.6×10−9,Ksp(BaSO4)=1.1×10−10。




