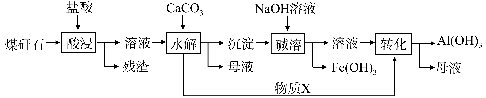-
(16分)某地煤矸石经预处理后主要含SiO2(61%)、Al2O3(30%)和少量的Fe2O3、FeO及钙镁的化合物等。某实验小组利用其提取Al(OH)3。
(1)“酸浸”过程中发生的主要反应的离子方程式为 。为提高“酸浸”时铝浸出率,可采取的措施之一是 。
(2)“氧化”的目的是 。检验Fe3+已水解完全的方法是 。
(3)滤渣Ⅱ的主要成分是CaCO3、Mg(OH)2和 。
(4)①上述流程中可循环利用的物质的化学式是 。
②“转化”时主要反应的离子方程式为 。
(5)Fe3+开始沉淀和沉淀完全的pH分别为2.1和3.2,Al3+开始沉淀和沉淀完全的pH分别为4.1和5.4。为了获得产品Al(OH)3,从氧化后的溶液开始,若只用纯碱一种试剂,后续操作是 。
-
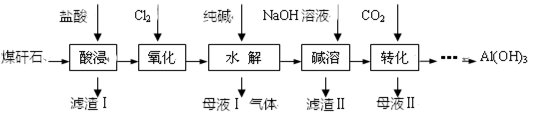
(10分)某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用煤矸石的工艺流程如下图所示。

(1)写出“酸浸”过程中主要反应的离子方程式(任写一个):
。
(2)物质X的化学式为________。“碱溶”时反应的离子方程式为_____________________________。
(3)已知Fe3+开始沉淀和沉淀完全的pH分别为2.1和3.2,Al3+开始沉淀和沉淀完全的pH分别为4.1和5.4。为了获得Al(OH)3产品,从煤矸石的盐酸浸取液开始,若只用CaCO3一种试剂,后续的操作过程是 ,再加入CaCO3调节pH到5.4,过滤得到Al(OH)3
(4)以煤矸石为原料还可以开发其他产品,例如在煤矸石的盐酸浸取液除铁后,常温下向AlCl3饱和溶液中不断通入HCl气体,可析出大量AlCl3·6H2O晶体。结合化学平衡移动原理解释析出晶体的原因: 。
-
某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用工艺设计如下:
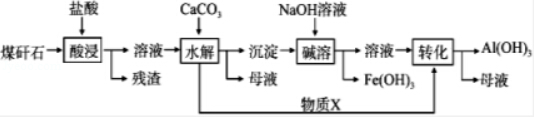
(1)“酸浸”过程中主要反应的离子方程式为: 、 .
(2)“酸浸”时,提高浸出速率的具体措施有 、 .(写出两个)
(3)“碱溶”的目的是 .物质X的化学式为 .
(4)从流程中分离出来的Fe(OH)3沉淀可在碱性条件下用KClO溶液处理,制备新型水处理剂高铁酸钾(K2FeO4),该反应的离子方程式为: .
(5)若根据过滤出的Fe(OH)3沉淀来推算煤矸石中Fe2O3的含量,须将沉淀清洗干净,检验沉淀是否洗干净的具体操作方法是 .
-
某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用工艺设计如下:
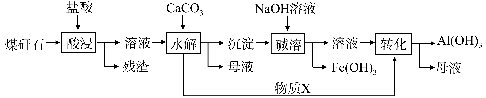
(1)“酸浸”过程中主要反应的离子方程式为__________ 、____________。
(2)“酸浸”时铝浸出率的影响因素可能有_____ ________、_____ ______。(写出两个)
(3)物质X的化学式为___________。“碱溶”时反应的主要离子方程式为:Fe3++3OH- = Fe(OH)3↓; 。
(4)已知Fe3+开始沉淀和沉淀完全的pH分别为2.1和3.2,Al3+开始沉淀和沉淀完全的pH分别为4.1和5.4为了获得产品Al(OH)3,从煤矸石的盐酸浸取液开始,若只用CaCO3一种试剂,后续操作过程是 。
(5)以煤矸石为原料还可以开发其他产品,例如在煤矸石的盐酸浸取液除铁后,常温下向AlCl3溶液中不断通入HCl气体,可析出大量AlCl3·6H2O晶体,结合化学平衡移动原理解释析出晶体的原因: 。
-
某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用工艺设计如下:
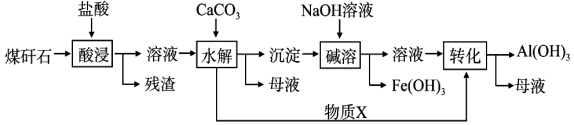
(1)“酸浸”过程中主要反应的离子方程式为:___________、___________。
(2)“酸浸”时,提高浸出速率的具体措施有___________、___________。(写出两个)
(3)“碱溶”的目的是___________。物 质X的化学式为___________。
质X的化学式为___________。
(4)从流程中分离出来的Fe(OH)3沉淀可在碱性条件下用KClO溶液处理,制备新型水处理剂高铁酸钾(K2FeO4),该反应的离子方程式为:___________。
-
某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用工艺设计如下:
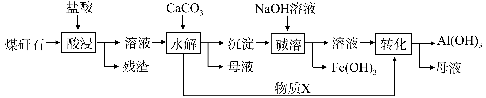
(1)“酸浸”过程中主要反应的离子方程式为_____________、_________________。
(2)“酸浸”时铝浸出率的影响因素可能有_____________、___________。(写出两个)
(3)物质X的化学式为___________。“碱溶”时反应的离子方程式为____________。
(4)已知Fe3+开始沉淀和沉淀完全的pH分别为2.1和3.2,Al3+开始沉淀和沉淀完全的pH分别为4.1和5.4。为了获得产品Al(OH) 3,从煤矸石的盐酸浸取液开始,若只用CaCO3一种试剂,后续操作过程是____________________。
(5)以煤矸石为原料还可以开发其他产品,例如在煤矸石的盐酸浸取液除铁后,常温下向AlCl3溶液中不断通入HCl气体,可析出大量AlCl3·6H2O晶体,结合化学平衡移动原理解释析出晶体的原因:_______________________。
-
某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用工艺设计如下:
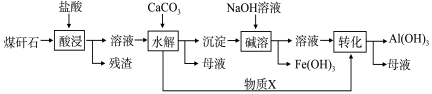
(1)“酸浸”过程中主要反应的离子方程式为:_____________、_____________。
(2)“酸浸”时,提高浸出速率的具体措施有_____________、_____________。(写出两个)
(3)“碱溶”的目的是_____________。物质X的化学式为_____________。
(4)从流程中分离出来的Fe(OH)3沉淀可在碱性条件下用KClO溶液处理,制备新型水处理剂高铁酸钾(K2FeO4),该反应的离子方程式为:_____________。
(5)若根据过滤出的Fe(OH)3沉淀来推算煤矸石中Fe2O3 的含量,须将沉淀清洗干净,检验沉淀是否洗干净的具体操作方法是_______________。
-
(16分)铝硅合金材料性能优良。铝土矿(含30% SiO2、40.8% Al2O3和少量Fe2O3等)干法制取该合金的工艺如下:
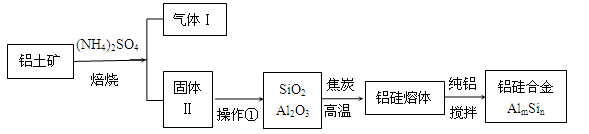
(1)若湿法处理铝土矿,用强酸浸取时,所得溶液中阳离子有 。
(2)铝硅合金材料中若含铁,会影响其抗腐蚀性。原因是 。
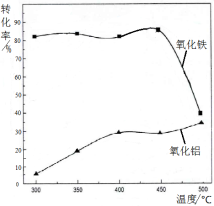
(3)焙烧除铁反应:4(NH4)2SO4 + Fe2O3  2NH4Fe(SO4)2 + 3H2O + 6NH3↑(Al2O3部分发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为 。指出气体Ⅰ的用途 (任写一种)。
2NH4Fe(SO4)2 + 3H2O + 6NH3↑(Al2O3部分发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为 。指出气体Ⅰ的用途 (任写一种)。
(4)操作①包括:加水溶解、 。若所得溶液中加入过量NaOH溶液,含铝微粒发生反应的离子方程式为 。
(5)用焦炭还原SiO2、Al2O3会产生中间体SiC、Al4C3。任写一个高温下中间体又与Al2O3反应生成铝、硅单质的化学方程式 。
(6)不计损失,投入1t铝土矿,当加入27kg纯铝后,铝硅合金中m:n = (摩尔质量:SiO2---60g/mol Al2O3---102 g/mol)。
-
用铝土矿(含30% SiO2、40.8% Al2O3和少量Fe2O3等)制取铝硅合金材料有湿法、干法等方法,其中干法制备的工艺流程如下:
(1)若湿法处理铝土矿,用强酸浸取时,所得溶液中阳离子有 。
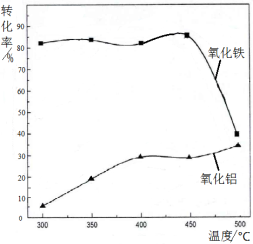
(2)焙烧除铁反应:4(NH4)2SO4 + Fe2O3  2NH4Fe(SO4)2 + 3H2O + 6NH3↑(Al2O3部分发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为 ,用电子式表示气体I的形成过程 。
2NH4Fe(SO4)2 + 3H2O + 6NH3↑(Al2O3部分发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为 ,用电子式表示气体I的形成过程 。
(3)操作①包括:加水溶解、 。
(4)用焦炭还原SiO2、Al2O3会产生中间体SiC、Al4C3。写一个高温下中间体与Al2O3反应生成铝单质的化学方程式 。
(5)铝硅合金材料中若含铁,会影响其抗腐蚀性。原因是 。
(6)不计损失,投入1t铝土矿,当加入54kg纯铝后,铝硅合金中m:n = 。
-
[化学——选修2:化学与技术](15分)某地煤矸石经预处理后含SiO2( 63%)、Al2O3( 25%) 、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用煤矸石的工艺流程如下图所示。

(1)写出“酸浸”过程中主要反应的离子方程式(任写一个): 。
(2)物质X足量时,“转化”过程中发生反应的有关离子方程式为 。
(3)已知Fe3+开始沉淀和沉淀完全的pH分别为2.1和3.7,A13+开始沉淀和沉淀完全的pH分别为4.1和5.4。为了获得Al( OH)3产品,从煤矸石的盐酸浸取液开始,若只用CaCO3一种试剂,后续的操作过程是 ,然后再加入CaCO3,调节pHCaCO3若只pH到5.4,过滤得到Al( OH)3 。
(4)以煤矸石为原料还可以开发其他产品,例如在煤矸石的盐酸浸取液除铁后,常温下向A1Cl3饱和溶液中不断通入HC1气体,可析出大量A1Cl3·6H2O晶体。结合化学平衡移动原理解释析出晶体的原因: 。
(5)工业上电解冶炼铝的原料用Al2O3而不用A1Cl3其原因是 。电解Al2O3冶炼铝时,阳极材料是 ,阳极需要定期更换,其原因是 。