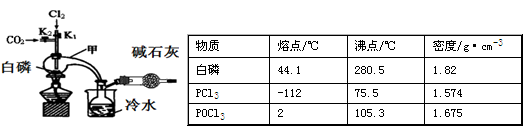-
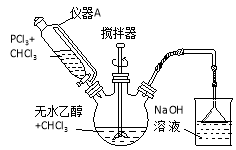
亚磷酸二乙酯[HPO(OC2H5)2]为重要的阻燃增塑剂。实验室采用三氯化磷和无水乙醇制备亚磷酸二乙酯PCl3 + 4C2H5OH → HPO(OC2H5)2 + HCl↑+2C2H5Cl + H2O;实验步骤如下:

①将40mL三氯甲烷和36.8g(0.8mol)无水乙醇混合后加入250mL三颈烧瓶中。
②从仪器A中滴加20mL三氯甲烷和27.5g (0.2mol)PCl3混合溶液,用冰水控温6~8℃,开动搅拌器,约1h滴加完毕。
③将反应物后的混合物倒入烧杯中,用10%的碳酸钠溶液中和至pH为7~8,再用去离子水洗涤三次,在仪器B中分离。
④减压蒸馏,收集产品,得23.32g产品。
(1)装置图中仪器A叫做恒压滴液漏斗,与分液漏斗比,滴液时的优点是________________;步骤③中仪器B名称为________________。图中NaOH溶液的作用为_____________________。
(2)用碳酸钠溶液洗涤的目的是______________;用去离子水洗涤的目的是_____________。
(3)减压蒸馏除得到产品外还可回收的有机物有_____________ 、___________________(写两个的结构简式)。
(4)从无水乙醇利用角度计算,本次实验产率为______________________(填数值)。
-
亚磷酸二乙酯[HPO(OC2H5)2]为重要的阻燃增塑剂。实验室采用三氯化磷和无水乙醇制备亚磷酸二乙酯PCl3 + 4C2H5OH → HPO(OC2H5)2 + HCl↑+2C2H5Cl + H2O;实验步骤如下:
①将40mL三氯甲烷和36.8g(0.8mol)无水乙醇混合后加入250mL三颈烧瓶中。
②从仪器A中滴加20mL三氯甲烷和27.5g (0.2mol)PCl3混合溶液,用冰水控温6~8℃,开动搅拌器,约1h滴加完毕。
③将反应物倒入烧杯中,用10%的碳酸钠溶液中和至pH为7~8,再用去离子水洗涤三次,在仪器B中分离。
④减压蒸馏,收集产品,得23.32g产品。
(1)装置图中仪器A叫做恒压滴液漏斗,与分液漏斗比,滴液时的优点是 ;步骤③中仪器B名称为 。图中NaOH溶液的作用为 。
(2)用碳酸钠溶液洗涤的目的是 ;用去离子水洗涤的目的是 。
(3)减压蒸馏除得到产品外还可回收的有机物有 (写两个的结构简式)。
(4)从无水乙醇利用角度计算,本次实验产率为 (填数值)。
-
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、妨织等工业。乙酸乙酯的实验室制法常采用如图装置:
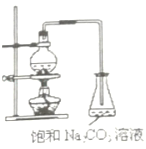
(1)烧瓶中除了乙酸和乙醇之外,还必须加的药品是___,其作用是___。
(2)能不能把饱和Na2CO3溶液换成饱和NaCl溶液?___,为什么?___。
(3)为了乙酸和乙醇回流,减少它们损失,该装置应该改进之处是:___。
(4)分离乙酸乙酯和饱和溶液,所需要的操作是___。
-
三氯化磷( )和三氯氧磷(POCl3)是两种遇水会强烈水解的物质。PCl3是合成药物的重要化工原料;POCl3用于制取染料中间体,有机合成的氯化剂、催化剂和阻燃剂,还常用作半导体掺杂剂及光导纤维原料。
)和三氯氧磷(POCl3)是两种遇水会强烈水解的物质。PCl3是合成药物的重要化工原料;POCl3用于制取染料中间体,有机合成的氯化剂、催化剂和阻燃剂,还常用作半导体掺杂剂及光导纤维原料。
I.白磷和Cl2化合制PCl3
已知白磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;PCl3遇O2会生成POCl3;POCl3能溶于PCl3。实验室制取PCl3的装置示意图和有关数据如下:
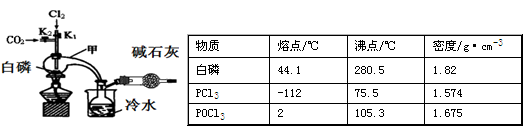
实验过程中要加入白磷、通入CO2 、通入Cl2、加热,实验时具体的操作顺序是:打开K2,使体系中充满CO2,再加入白磷,打开K1,通入氯气,再加热。
(1)干燥管中碱石灰的作用是_______________。
(2)PCl3强烈水解的产物是H3PO3和HCl,PC13遇水所得溶液中除OH-之外其它离子的浓度由大到小的顺序是____________________(己知亚磷酸H3PO3是二元弱酸:H3PO3  H++ H2PO3-,H2PO3-
H++ H2PO3-,H2PO3- H++HPO32-)。
H++HPO32-)。
(3)实验制得的粗产品中常含有POCl3、PC15等,PC15先用白磷除去后,再用____________方法除去PC13中的POCl3制备纯净的PCl3。
A.萃取 B.过滤 C.蒸馏 D.蒸发结晶
II.氯化水解法生产POC13
主要反应是:PC13+C12+H2O=POC13+2HCl,流程如下:

(1)若将0.01mol POCl3加到水中水解,再与含2.4gNaOH的溶液混合充分反应,并配成1L的溶液,取出少量的溶液于试管中,再向其中逐滴加入0.010mol/L的AgNO3溶液,则先产生的沉淀是_____________[已知Ksp(Ag3PO4)=1.4×10-16,Ksp(AgCl)=1.8×10-10]。
(2)通过下列方法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
A.取ag产品于锥形瓶中,加入足量NaOH 溶液,再加稀硝酸至酸性。
B.向锥形瓶中加入0.1000 mol/L的AgNO3溶液40.00mL,使Cl-完全沉淀。
C.向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖。
D.加入指示剂,用cmol/LNH4SCN溶液滴定过量Ag+至终点,记下所用体积bmL。
己知:AgSCN是白色沉淀,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是_____________(填字母序号),滴定终点的现象为_________________。
A.FeCl2 B.NH4Fe(SO4)2 C.淀粉 D.甲基橙
②实验过程中加入硝基苯的目的是覆盖氯化银,防止沉淀转化生成AgSCN而导致数据不准确。如无此操作,所测Cl元素含量将会______________(填“偏大”、“偏小”或“不变”)。
③根据上面实验数据计算三氯氧磷产品中Cl元素的含量为______________。
-
(12分)酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常用冰醋酸、无水乙醇和浓硫酸混合,在加热条件下反应制得:
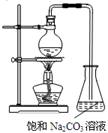
请根据要求回答下列问题:
(1) 写出该反应的化学方程式________
(2)此反应中浓硫酸的作用是 ________
饱和碳酸钠的作用是________
(3)若采用同位素示踪法研究该化学反应,反应物无水乙醇中含有18O,冰醋酸中均为16O,反应后的混合物中,含有18O的物质有________
(4)若用如图所示装置来制备少量的乙酸乙酯,锥形瓶中的现象为________,不过往往产率偏低,其原因可能为(任填2种)
-
(16分)酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业,乙酸乙酯的实验室和工业制法常采用如下反应:

请根据要求回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有________,________。(任写两点只要合理即可)
(2)浓硫酸的作用是:①________、②________。
(3)饱和NaCO3溶液的作用:
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)
| 同一反应时间 | 同一反应温度 |
| 反应温度/℃ | 转化率/% | 选择性/% | 反应时间/h | 转化率/% | 选择性/% |
| 40 | 77.8 | 100 | 2 | 80.2 | 100 |
| 60 | 92.3 | 100 | 3 | 87.8 | 100 |
| 80 | 92.6 | 100 | 4 | 92.3 | 100 |
| 120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
| 选择性100%表示反应无副反应发生 |
根据表中数据,下列________(填字母)为该反应的最佳条件。
A.120 ℃,4 h B. 80 ℃,2 h C. 60 ℃,4 h D.40 ℃,3 h
-
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业.乙酸乙酯的实验室和工业制法常采用如下反应:CH3COOH+C2H5OH
 CH3COOC2H5+H2O
CH3COOC2H5+H2O
请根据要求回答下列问题:
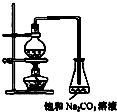
(1)若用右图所示装置来制备少量的乙酸乙酯,其中饱和碳酸钠溶液的作用是______.
(2)此反应以浓硫酸为催化剂,可能会造成______、______等问题.
(3)在图所示的装置中进行50mL 0.50mol/L醋酸与50mL 0.55mol/L NaOH溶液的中和反应.通过测定反应过程中所放出的热量可计算反应热.回答下列问题: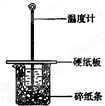
①从实验装置上看,图中尚缺少的一种玻璃用品是______;
②在题述反应条件下,测得反应前醋酸和NaOH溶液的温度均为25.43℃,反应后混合溶液的温度为28.73℃.已知反应前醋酸
和NaOH溶液的密度均为1.0g•cm-3,反应后混合溶液的比热容为c=4.18J/.试写出中和反应的热化学方程式:______.
-
下列关于实验室制备乙酸乙酯和乙酸丁酯的描述正确的是
A.均采用水浴加热 B.制备乙酸丁酯时正丁醇过量
C.均采用边反应边蒸馏的方法 D.制备乙酸乙酯时乙醇过量
-
下列关于实验室制备乙酸乙酯和乙酸丁酯的描述正确的是
A.均采用水浴加热  B.制备乙酸丁酯时正丁醇过量
B.制备乙酸丁酯时正丁醇过量
C.均采用边反应边蒸馏的方法 D.制备乙酸乙酯时乙醇过量
-
实验室制备乙酸乙酯的原理是:
CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
为了得到更多的乙酸乙酯常采用如下措施,
①原料选择无水乙醇和冰醋酸,而不是乙醇溶液或是醋酸溶液,其依据是____________________;
②通过控制反应温度,尽可能地将生成的乙酸乙酯从反应体系中脱离,有利于乙酸乙酯的生成,其依据是__________________;