-
已知某温度时0.01mol/L的NaOH溶液的pH=10,则此温度下水的离子积常数Kw=________.此温度下将pH=12的NaOH溶液V1 L与pH=1的H2SO4溶液V2 L混合,若所得混合溶液的pH=10,则V1:V2为________.
高三化学填空题中等难度题查看答案及解析
-
某温度(T ℃)时,测得0.01 mol·L-1的NaOH溶液的pH=11。在此温度下,将pH=2的H2SO4溶液Va L与pH=12的NaOH溶液Vb L混合,若所得混合液为中性,则Va∶Vb=______________。
高三化学填空题简单题查看答案及解析
-
某探究小组在某温度下测定溶液的pH时发现0.01mol/L 的NaOH溶液中,由水电离出的c(H+)•c(OH-)=10-22,该探究小组将pH=x的H2SO4溶液与pH=y的NaOH溶液按体积比1:10混合,混合后所得溶液恰好呈中性,若x=
y,则x为( )
A.2 B.3 C.4 D.5
高三化学单选题中等难度题查看答案及解析
-
(1)常温下,将1 mL pH=1的H2SO4溶液加水稀释到100 mL,稀释后的溶液中
=________。
(2)某温度时,测得0.01 mol·L-1的NaOH溶液的pH为11,则该温度下水的离子积常数Kw=________。该温度________(填“高于”或“低于”)25 ℃。
(3)常温下,设pH=5的H2SO4溶液中由水电离出的H+浓度为c1;pH=5的Al2(SO4)3溶液中由水电离出的H+浓度为c2,则
=________。
(4)常温下,pH=13的Ba(OH)2溶液a L与pH=3的H2SO4溶液b L混合(混合后溶液体积变化忽略不计)。
若所得混合溶液呈中性,则a∶b=________。
若所得混合溶液pH=12,则a∶b=________。
(5)在(2)所述温度下,将pH=a的NaOH溶液VaL与pH=b的硫酸Vb L混合。
①若所得混合液为中性,且a=12,b=2,则Va∶Vb=________。
②若所得混合液的pH=10,且a=12,b=2,则Va∶Vb=________。
高三化学简答题中等难度题查看答案及解析
-
用0.01mol·L-1H2SO4滴定1mol·L-1NaOH溶液,中和后加水至100.00mL。若滴定终点判断有误:(1)多加了1滴H2SO4;(2)少加了1滴H2SO4(设1滴H2SO4的体积为0.05mL)。则(1)与(2)溶液中H+离子的物质的量浓度之比为( )
A.10 B.50 C.5×103 D.104
高三化学选择题中等难度题查看答案及解析
-
向x mL 0.01 mol·L-1氨水中滴加等物质的量浓度的H2SO4溶液,测得混合溶液的pOH[pOH= -lgc(OH-)]、温度随着加入的硫酸溶液体积的变化如图所示,下列说法正确的是( )。
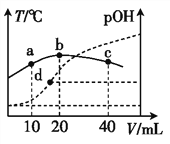
A.x=20
B.b点时溶液的pOH=pH
C.c点对应的溶液中:c(S
)>c(N
)>c(H+)>c(OH-)
D.a、b、d三点NH3·H2O的电离常数:K(b)>K(d)>K(a)
高三化学单选题困难题查看答案及解析
-
向x mL 0.01 mol·L-1氨水中滴加等物质的量浓度的H2SO4溶液,测得混合溶液的pOH[pOH= -lgc(OH-)]、温度随着加入的硫酸溶液体积的变化如图所示,下列说法正确的是( )。
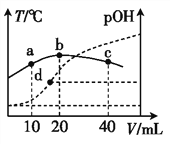
A. x=20
B. b点时溶液的pOH=pH
C. c点对应的溶液中:c(S
)>c(N
)>c(H+)>c(OH-)
D. a、b、d三点NH3·H2O的电离常数:K(b)>K(d)>K(a)
高三化学单选题困难题查看答案及解析
-
已知25℃时醋酸的电离常数为1.6×10-5,该温度下向20 mL 0.01 mol·L-1醋酸溶液中不断滴入0.01 mol·L−1 NaOH(aq),溶液pH变化如图所示。此过程溶液中离子浓度的关系错误的是
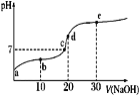
A. a点溶液的c(H+)=4×10-4mol·L-1
B. 水电离程度:e>d>c>b>a
C. b点:2c(Na+)=c(CH3COO-)+c(CH3COOH)
D. d点:c(OH-)=c(CH3COOH)+c(H+)
高三化学单选题中等难度题查看答案及解析
-
已知25℃时醋酸的电离常数为1.6×10-5,该温度下向20 mL 0.01 mol·L-1醋酸溶液中不断滴入0.01 mol·L−1 NaOH(aq),溶液pH变化如图所示。此过程溶液中离子浓度的关系错误的是
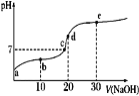
A.a点溶液的c(H+)=4×10-4mol·L-1
B.水电离程度:e>d>c>b>a
C.b点:2c(Na+)=c(CH3COO-)+c(CH3COOH)
D.d点:c(OH-)=c(CH3COOH)+c(H+)
高三化学单选题中等难度题查看答案及解析
-
已知25℃时醋酸的电离常数为1.6×10-5,该温度下向20 mL 0.01 mol·L-1醋酸溶液中不断滴入0.01 mol·L−1 NaOH(aq),溶液pH变化如图所示。此过程溶液中离子浓度的关系错误的是
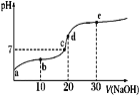
A.a点溶液的c(H+)=4×10-4mol·L-1
B.水电离程度:e>d>c>b>a
C.b点:2c(Na+)=c(CH3COO-)+c(CH3COOH)
D.d点:c(OH-)=c(CH3COOH)+c(H+)
高三化学单选题中等难度题查看答案及解析