-
合成氨工业对国防具有重要意义,如制硝酸、合成纤维以及染料等
(1)已知某些化学键的键能数据如下表:
化学键
N≡N
H—H
N—H
键能kJ·mol-1
946
436
390
合成氨的热化学反应方程式为________。
(2)常温下,向饱和NaCl与饱和氨水的混合溶液中通入过量CO2,有NaHCO3固体析出,该反应的化学方程式为;所得溶液中离子的电荷守恒式是________;若向饱和NaCl与饱和CO2的混合溶液中通入氨气,则没有NaHCO3固体析出,原因是________。
(3)氨氮废水(含NH3、NaOH和Na2SO4)超标排放会造成水体富营养化。右图通过直接电化学氧化法有效除去某工厂氨气。其中阴离子的流动方向为________(填“向a极”或“向b极”),电解过程中,b极区的pH________(填“增大”或“减小”或“不变”),阳极反应方程式为。
高三化学填空题中等难度题查看答案及解析
-
氨是一种重要的化工原料,工业合成氨对农业、化工和国防意义重大。合成氨反应为:
N2(g) +
H2(g)
NH3(g),回答下列问题:
(1)化学键键能数据如下:
化学键
H-H
N
N
N-H
E/kJ▪mol-1
436
946
391
上述反应的△H=____________;若正反应的活化能为Ea正(kJ/mol'),则逆反应的活化能Ea逆= kJ/mol (用含Ea正的代数式表示)。
(2)在合成氨的反应中,外界条件会对平衡发生移动产生影响。如图表示随外界条件改变,氨气的体积分数(φ)的变化趋势。若横坐标x表示压强,则变化趋势正确的是__________, (填曲线字母标号,下同);若x为温度,则变化趋势正确的是__________。

(3) p(N2)、p(H2)、p( NH3)分别代表N2、H2、NH3的分压,上述反应的压力平衡常数表达式Kp=_________(用平衡时的分压代替平衡时的浓度表示);已知:一定条件下,V正、V逆分别与k正、k逆成正比,其中k正、k逆为速率常数,随温度升高而增大,温度一定时,k正 :k逆为常数。若合成氨反应达到平衡后,再升高温度时,理论上活化分子百分数_______,(填“增大”“减小”或“不变”,下同),k正 :k逆与升高温度前比较将_____________。
(4)工业上,合成氨反应在高压条件下进行,实际上Kp值不仅与温度有关,还与压力和气体组成有关。一定条件下,上述合成氨反应接近平衡时,遵循如下方程:
 。其中r( NH3)为氨合成反应的净速率,a为常数,与催化剂性质及反应条件有关,该条件下,实验测得a=0.5,则反应达到平衡时,k正 、k逆、kp三者的关系式为____________________。
。其中r( NH3)为氨合成反应的净速率,a为常数,与催化剂性质及反应条件有关,该条件下,实验测得a=0.5,则反应达到平衡时,k正 、k逆、kp三者的关系式为____________________。高三化学综合题中等难度题查看答案及解析
-
合成氨工业对化学工业和国防工业具有重要意义,对农业生产起着重要作用。
(1)已知:N2(g)+O2(g)=2NO(g) △H1
H2(g)+1/2O2(g)=H2O(1) △H2
4NH3(g)+5O2(g)=4NO(g)+6H2O(1) △H3
N2(g)+3H2(g)⇌2NH3(g) △H4<0
则△H4= (用含△H1、△H2、△H3的代数式表示)。
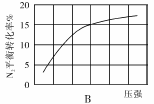
(2)在其他条件相同时,分别测定合成氨反应中N2的平衡转化率随压强变化的曲线如下图A、B所示,其中正确的是 (填“A”或“B”),其判断理由是 。

(3)在体积为2L的密闭容器中按物质的量1:3的比例充入N2、H2,进行下列四组合成氨实验:
组别
温度
N2起始量/mol
N2的物质的量/mol
5(s)
10(s)
15(s)
20(s)
25(s)
30(s)
35(s)
Ⅰ
T1
0.1
0.094
0.089
0.085
0.0825
0.081
0.080
0.080
Ⅱ
T2
0.1
0.090
0.085
0.082
0.080
0.080
0.080
0.080
Ⅲ
T3
0.2
0.179
0.165
0.153
0.146
x
x
x
Ⅳ
T4
0.2
0.173
0.161
0.155
0.150
0.150
0.150
0.150
①实验Ⅰ前10秒的平均速率v(NH3)= mol·L-1·s-1,T1温度下合成氨反应的平衡常数K= (列出计算式)。
②与实验Ⅰ相比,实验Ⅱ改变了一个条件,该条件可能是 。
③与实验I相比,实验Ⅲ中N2的平衡转化率 (填“增大”、“减小”或“不变”),平衡常数K (填“增大”、“减小”或“不变”)。
④实验Ⅲ与实验Ⅳ的反应条件温度不同,则T1 (填“大于”、“小于”或“等于”)T2,原因是 。
高三化学填空题困难题查看答案及解析
-
(1)合成氨工业对化学工业和国防工业具有重要意义.工业合成
氨的原理是:N2+3H22NH3△H<0,生产流程如图1所示.
①X的化学式为______;
②图中条件选定的主要原因是(选填字母序号)______;
A.升高温度、增大压强均有利于氨的合成
B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
③改变反应条件,会使平衡发生移动.图2表示随条件改变,氨气的百分含量的变化趋势.当横坐标为压强时,变化趋势正确的是(选填字母序号)______,当横坐标为温度时,变化趋势正确的是(选填字母序号)______.
(2)常温下氨气极易溶于水,其水溶液可以导电.
④用方程式表示氨气溶于水且显弱碱性的过程:______;
⑤氨水中水电离出的c(OH-)______ 10-7 mol•L-1(填写“>”、“<”或“=”);
⑥将相同体积、相同物质的量浓度的氨水和盐酸混合后,溶液中离子浓度由大到小依次为______.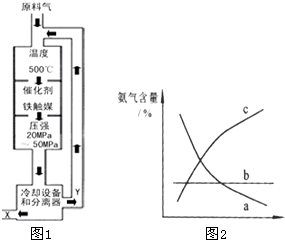
高三化学解答题中等难度题查看答案及解析
-
(1)合成氨工业对化学工业和国防工业具有重要意义。工业合成氨生产示意图如右图所示。
①合成氨条件选定的主要原因是(选填字母序号);
A.温度、压强对化学反应速率及化学平衡影响
B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
②改变反应条件,平衡会发生移动。压强增大,平衡常数K(填“增大”“减小”“不变”)
(2)氨气具有还原性,在铜的催化作用下,氨气和氟气反应生成A和B两种物质。A为铵盐,B在标准状况下为气态。在此反应中,若每反应1体积氨气,同时反应0.75体积氟气;若每反应8.96L氨气(标准状况),同时生成0.3molA。
①写出氨气和氟气反应的化学方程式;
②在标准状况下,每生成1 mol B,转移电子的数目为。
(3) 最近美国Simons等科学家发明了不必使氨先裂化为氢就可直接用于燃料电池的方法。它既有液氢燃料电池的优点,又克服了液氢不易保存的不足。其装置为用铂黑作为电极,加入强碱溶液中,一个电极通入空气,另一电极通入氨气。其电池反应为4NH3+3O2═2N2+6H2O。写出负极电极反应式。
高三化学填空题中等难度题查看答案及解析
-
(18分)(1)合成氨工业对化学工业和国防工业具有重要意义。工业合成氨生产示意图如图所示。

①X的化学式为________;
②上图中条件选定的主要原因是(选填字母序号)________;
A.温度、压强对化学平衡影响 B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
③改变反应条件,会使平衡发生移动。下图表示随条件改变,氨气的百分含量的变化趋势。当横坐标为压强时,变化趋势正确的是(选填字母代号)________,当横坐标为温度时,变化趋势正确的是(选填字母序号)________。

(2)常温下氨气极易溶于水,其水溶液可以导电。
①用方程式表示氨气溶于水的过程中存在的可逆反应
________,
②氨水中水电离出的c(OH-) ________10-7mol/L(填写“>”、“<”或“=”);
③将相同体积、相同物质的量浓度的氨水和盐酸混合后,溶液中离子浓度由大以小依次为。
(3)氨气具有还原性,在铜的催化作用下,氨气和氟气反应生成A和B两种物质。A为铵盐,B在标准状况下为气态。在此反应中,若每反应1体积氨气,同时反应0.75体积氟气;若每反应8.96L氨气(标准状况),同时生成0.3molA。
①写出氨气和氟气反应的化学方程式________;
②在标准状况下,每生成1 mol B,转移电子的物质的量为________mol。
高三化学填空题中等难度题查看答案及解析
-
合成氨对化学工业和国防工业具有重要意义。

(1)根据图1请写出合成氨的热化学方程式______
热量用
、
或
表示
。
(2)向合成塔中按物质的量之比l:4充入
、
进行氨的合成,图2为
时平衡混合物中氨气的体积分数与压强
的关系图。
①图2中氨气的体积分数为
时,
的转化率为______。
②图3中
,则温度为
时对应的曲线是______
填“a”或“b”
。
(3)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为
,一定温度下,在体积为2L的恒容容器中发生上述反应,各物质的物质的量变化如表:
时间
0
0
0
5
7
10
①分析表中数据,判断5min时反应是否处于平衡状态?______
填“是”或“否”
,前5min反应的平均反应速率
______。
②在相同实验条件下,若改为加入
,若要求平衡后
在反应混合气中质量分数不变,则还需加入的物质及其物质的量为______。
③反应在
内,CO的物质的量减少的原因可能是______
填字母
。
减少
的物质的量
降低温度
升高温度
充入
④下列方法中可以证明上述已达平衡状态的是______。
单位时间内生成
的同时生成
b.容器内压强不再变化
混合气体密度不再变化
混合气体的平均相对分子质量不再变化
的质量分数不再变化
⑤已知碳的气化反应在不同温度下平衡常数的对数值
如表:
气化反应式
lgK
700K
900K
1200K
则反应
在900K时,该反应平衡常数的对数值
______。
高三化学综合题中等难度题查看答案及解析
-
(12分)合成氨对化学工业和国防工业具有重要意义。
⑴向合成塔中按物质的量之比l:4充入N2、H2进行氨的合成,图A为T℃时平衡混合物中氨气的体积分数与压强(p)的关系图。
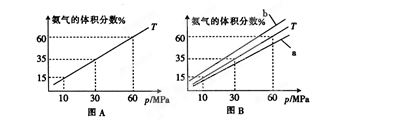
①图A中氨气的体积分数为15%时,H2的转化率为。
②图B中T=500℃,则温度为450℃时对应的曲线是(填“a”或“b”)。
⑵合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为CH4(g)+H2O(g)
CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
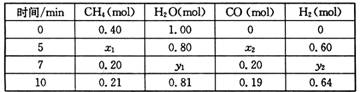
①分析表中数据,判断5 min时反应是否处于平衡状态? ________(填“是”或“否”),
前5 min反应的平均反应速率v(CH4)=________。
②该温度下,上述反应的平衡常数K=。
③反应在7~10 min内,CO的物质的量减少的原因可能是 (填字母)。
a.减少CH4的物质的量 b.降低温度 c.升高温度 d.充入H2
高三化学填空题中等难度题查看答案及解析
-
(14分)合成氨对化学工业和国防工业具有重要意义。
(1)向合成塔中按物质的量之比l:4充入N2、H2进行氨的合成,图A为T℃时平衡混合物中氨气的体积分数与压强(p)的关系图。
①图A中氨气的体积分数为15%时,H2的转化率为________。
②图B中T=450℃,则温度为500℃时对应的曲线是________(填“a”或“b”)。
(2)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为
CH4(g)+H2O(g)
CO(g)+3H2(g) △H>0,一定温度下,在体积为2 L的恒容容器中发生上述反应,各物质的物质的量变化如下表:
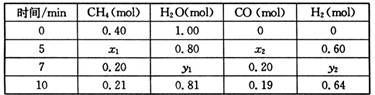
①分析表中数据,判断5 min时反应是否处于平衡状态? ________(填“是”或“否”),前5 min反应的平均反应速率v(CH4)=________。
②该温度下,上述反应的平衡常数K=________。
③反应在7~10 min内,CO的物质的量减少的原因可能是________(填字母)。
a.减少CH4的物质的量 b.降低温度 c.升高温度 d.充入H2
④若第7分钟时将容器压缩至1L,请在下列坐标系中画出从第7分钟到第11分钟建立新平衡时甲烷浓度随时间的变化曲线。
a
高三化学填空题简单题查看答案及解析
-
合成氨对化学工业和国防工业具有重要意义.
(1)向合成塔中按物质的量之比l:4充入N2、H2进行氨的合成,图A为T℃时平衡混合物中氨气的体积分数与压强(p)的关系图.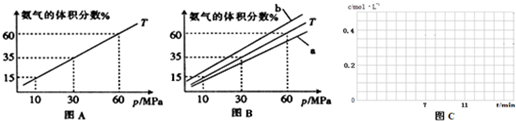
①图A中氨气的体积分数为15%时,H2的转化率为________.
②图B中T=450℃,则温度为500℃时对应的曲线是________(填“a”或“b”).
(2)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为
CH4(g)+H2O(g)⇌CO(g)+3H2(g)△H>0,一定温度下,在体积为2L的恒容容器中发生上述反应,各物质的物质的量变化如表:
①分析表中数据,判断5min时反应是否处于平衡状态?________(填“是”或“否”),前5min反应的平均反应速率v(CH4)=________.时间/min CH4(mol) H2O(mol) CO(mol) H2(mol) 0.40 1.00 5 x1 0.80 x2 0.60 7 0.20 y1 0.20 y2 10 0.21 0.81 0.19 0.64
②该温度下,上述反应的平衡常数K=________.
③反应在7~10min内,CO的物质的量减少的原因可能是________(填字母).
a.减少CH4的物质的量 b.降低温度 c.升高温度 d.充入H2
④若第7分钟时将容器压缩至1L,请在图C所示坐标系中画出从第7分钟到第11分钟建立新平衡时甲烷浓度随时间的变化曲线.高三化学填空题中等难度题查看答案及解析