有机高分子化合物在日常生活中有非常广泛的应用。一种广泛应用于电器、工业交通的工程塑料DAP的结构简式是:
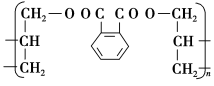
试回答:
(1)生产DAP工程塑料的单体的结构简式是__________________________。
(2)DAP工程塑料的单体,可以由两种有机物通过一步反应合成出来,则这两种有机物的结构简式是____________________和_______________。
高二化学填空题中等难度题
有机高分子化合物在日常生活中有非常广泛的应用。一种广泛应用于电器、工业交通的工程塑料DAP的结构简式是:

试回答:
(1)生产DAP工程塑料的单体的结构简式是__________________________。
(2)DAP工程塑料的单体,可以由两种有机物通过一步反应合成出来,则这两种有机物的结构简式是____________________和_______________。
高二化学填空题中等难度题
有机高分子化合物在日常生活中有非常广泛的应用。一种广泛应用于电器、工业交通的工程塑料DAP的结构简式是:

试回答:
(1)生产DAP工程塑料的单体的结构简式是__________________________。
(2)DAP工程塑料的单体,可以由两种有机物通过一步反应合成出来,则这两种有机物的结构简式是____________________和_______________。
高二化学填空题中等难度题查看答案及解析
日常生活中的塑料包括很多种,其中PET(聚对苯二甲酸乙二醇酯)塑料被广泛用于生产包装瓶、电器元件、汽车配件等;PS塑料被广泛应用于光学工业中,PET塑料、PS塑料可按下图所示合成。

(1)C能与含氧酸发生酯化反应,则C的分子式为________,其所含的官能团的名称为________。
(2)X、Y互为同分异构体,分子式为C8H10,则X的结构简式为________,
其核磁共振氢谱有________种峰。
(3)D分子中含有一个甲基,则D→E的化学方程式为________,
E与CH2=CH—CH=CH2在一定条件下1︰1发生反应生成除苯环外无支链的高聚物的化学方程式为________。
(4)Z是B的同分异构体,其具有如下性质:①遇FeCl3溶液显紫色;②能与NaHCO3溶液反应放出CO2;③苯环上的一氯代物只有三种;④苯环上只有2个取代基相邻。则Z的结构最多有________种,写出其中一种的结构简式________。
高二化学填空题困难题查看答案及解析
氯化物在工业生产、日常生活中应用都非常广泛。某学习小组为探究一些实用性很强的氯化物,进行了一系列的资料查询与具体实验。
(1)用于制造电池的原材料二氯亚砜(SOCl2),是一种液态化合物,沸点为77℃。在盛10mL水的锥形瓶中小心滴加8~10滴SOCl2可观察到剧烈反应,液面上形成白雾,并逸出刺激性气味的气体,该气体可使沾有品红试液的滤纸褪色。轻轻振荡锥形瓶,待白雾消失后往溶液中滴加AgNO3溶液,有不溶于稀HNO3的白色沉淀析出。室温下,小组某同学取2.38g SOCl2与水发生上述反应,测得放出热量为17.88 kJ。根据以上实验,写出SOCl2与水反应的热化学方程式_______________________。
(2)低温蒸干AlCl3溶液得到固体的主要成分是___________;小组某同学想制取无水AlCl3固体,他提出可以用AlCl3·6H2O与SOCl2混合后共热来制取无水AlCl3固体,你认为可行吗?请说明原因______________。
(3)TiO2是一种非常好的催化剂。某同学通过查阅资料显示:TiCl4水解程度很大,可以用于TiO2的制备,制备时加入大量的水,同时加热,促进水解趋于完全,所得TiO2·xH2O经焙烧得TiO2。请写出TiCl4水解的化学方程式__________________________。
(4)某同学利用NaCl溶液设计实验验证Fe在原电池反应中的生成物,使用Cu电极、Fe电极、经过酸化的3%NaCl溶液,组成原电池装置,实验结束后,该同学往Fe电极区滴入2滴黄色铁氰化钾溶液,现象是:______________________________。
高二化学填空题困难题查看答案及解析
铜及其化合物在工农业生产及日常生活中应用非常广泛。回答下列问题:
(1)纳米级Cu2O由于具有优良的催化性能而受到关注,制取Cu2O的两种方法如下表所示。
| 方法I | 用炭粉在高温条件下还原CuO生成Cu2O和CO2 |
| 方法II | 用肼(N2H4)还原新制Cu(OH)2 |
① 方法I中还原剂与氧化剂的物质的量之比为________。
② 方法II发生反应的化学方程式为______________。
(2)氢化亚铜是一种红色同体,可由下列反应制备:
4CuSO4+3H3PO2+6H2O=4CuH↓+4H2SO4+3H3PO4
该反应中每转移3 mol电子,生成CuH的物质的量为___________mol。
(3)氯化铜溶液中各种含铜微粒的分布分数(平衡时某微粒的浓度占各微粒浓度之和的分数)与c(C1-)之间的关系如图所示。
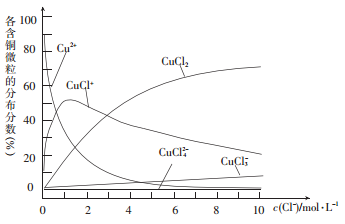
① 当c(C1-)= 9 mol/L时,溶液中3种主要含铜微粒浓度的大小关系为__________。
② 在c(C1-)= l mol /L的氯化铜溶液中,加人AgNO3溶液,CuCl+转化为Cu2+的离子方程式为____________。
(4)已知:Cu(OH)2是二元弱碱,25℃时Ksp[Cu(OH)2]=2.0×10-20。则此温度下在铜盐溶液中Cu2+发生水解反应的平衡常数为______________。
高二化学填空题困难题查看答案及解析
材料是人类社会生活的物质基础,材料创新则是科技进步的集中体现.
①不锈钢用品广泛用于日常生活,它是在普通钢中添加了 和镍等形成合金.
②塑料、纤维及橡胶为三大有机高分子材料,其中天然橡胶的结构简式为 .
③水泥、玻璃及陶瓷都是传统的硅酸盐材料,生产水泥和玻璃都用到的原料是 ;有机玻璃是一种 材料;SiC是一种新型的陶瓷,工业上用石英砂与焦炭高温下条件下生成SiC同时生成CO,该制备反应的化学方程式为 .
高二化学填空题中等难度题查看答案及解析
碳、 氮、磷、砷和硼的相关化合物在化工、医药、农药、材料等领域有着广泛的应用。锂、钠、铝、铁等金属在日常生活、工业生产中也占有举足轻重的地位,请回答下列问题:
(1)基态As原子的电子排布式为______________________;
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中B—N—B之间的夹角是___________________(填角度)。
(3)金属晶体的四种堆积如下图,金属钠的晶体堆积模型为___ (填字母)。
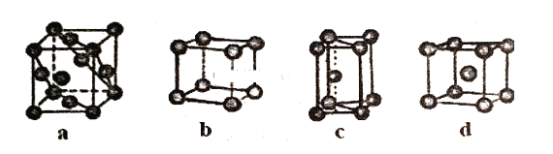
高二化学填空题中等难度题查看答案及解析
(18分)铁、铜等金属及其化合物在日常生活中应用广泛,回答下列问题。
(1)电子工业常用30%的FeCl3溶液腐蚀附在绝缘板上的铜箔制造印刷电路板,取其腐蚀后的废液,加 入一定量的铁粉后,若无固体剩余,则反应后的溶液中肯定有的离子是______________;若有红色固体,则反应后的溶液中肯定没有的离子是________,检验该离子的试剂为________。
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃-60℃,加入H2O2,反应一段时间后可制得硫酸铜,发生反应的化学方程式为:_____________________,
(3)实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾(FeSO4.7H2O),测定产品中绿矾含量的实验步骤:
a.称取5.7 g产品,溶解,配成250 mL溶液;
b.量取25 mL待测液于锥形瓶中;
c.用硫酸酸化的0.01 mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液的体积为40 mL。
根据上述步骤回答下列问题:
①滴定时发生反应的离子方程式为(完成并配平离子反应方程式)
②用硫酸酸化的KMnO4溶液滴定至终点的标志是 _____。
③上述产品中FeSO4·7H2O的质量分数为 。
(4)铁氰化钾 K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6] 的混合溶液可用于太阳能电池的电解液,该太阳能电池的工作原理示意图如图所示,其中催化剂a为________极,电极反应式为_______________;

高二化学填空题困难题查看答案及解析
(12分)铜及其化合物在工农业生产及日常生活中应用非常广泛。某研究小组用粗铜(含杂质铁)制备氯化铜晶体(CuCl2.2H2O)的流程如下。
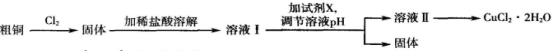
已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
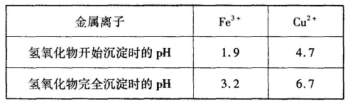
请回答下列问题:
(1)溶液I中加入试剂X可以调节溶液pH,从而除去Fe3+且不引入杂质。
①试剂X可选用下列物质中的__________(填代号)。
a.CuO b.NaOH c.Cu d.Cu(OH)2
②调节溶液pH时,理论上可选择pH最大范围是__________。
(2)由溶液Ⅱ制备CuCl2.2H2O的操作依次为:边滴加浓盐酸边加热浓缩、__________(填操作名称)、过滤、洗涤干燥。
(3)向溶液Ⅱ中通入H2S气体,溶液变浑浊,pH减小,用离子方程式解释其原因:__________.
(4)某学习小组用碘量法测定CuCl2.2H2O样品的纯度(杂质不与发生反应)。实验如下:
a.准确称取CuCl2.2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250 mL待测溶液。(已知: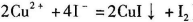 )
)
b.移取25. 00 mL待测溶液于锥形瓶中,加几滴指示剂,用c molNa2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL。 (已知:
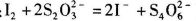 )
)
①实验中使用的指示剂名称为____________。
②达到滴定终点时,仰视滴定管读数将使测定结果_________(填“偏高”、“偏低”或“无影响”)。
③该样品中CuCl2.2H2O 的质量分数为_________(用含m、c、V的代数式表示,不用化简)。
高二化学填空题困难题查看答案及解析
铜及其化合物在工农业生产及日常生活中应用非常广泛。
(1) 由辉铜矿制取铜的反应过程为:
2Cu2S(s)+ 3O2(g)==2Cu2O(s)+2SO2(g) △H =-768.2kJ·mol-1,
2Cu2O(s)+Cu2S(s)=6Cu(s)+ SO2(g) △H =+116.0kJ·mol-1,
热化学方程式: Cu2S(s)+ O2(g)==2Cu(s)+2SO2(g) △H =______kJ·mol-1
(2) 氢化亚铜是一种红色固体,可由下列反应制备:4CuSO4+3H3PO2+6H2O==4CuH ↓+4H2SO4+3H3PO4。
①该反应还原剂是___________(写化学式)。
②该反应每转移6mol电子,生成CuH的物质的量为_____。
(3)采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示。
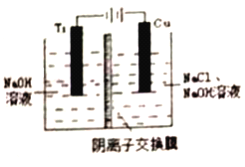
①该电池的阳极生成Cu2O反应式为___________________________。
②钛(Ti) 极附近的pH值_________(填“增大”、“减小”或“不变”)
高二化学综合题中等难度题查看答案及解析
铜及其化合物在工农业生产及日常生活中应用非常广泛。某研究小组用粗铜(含杂质铁)制备氯化铜晶体(CuCl2·2H2O )的流程如下。

已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| 金属离子 | Fe3+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 6.7 |
请回答下列问题:
(1)溶液I中加入试剂X可以调节溶液pH,从而除去Fe3+且不引入杂质。
①试剂X可选用下列物质中的__________(填代号)。
a.CuO b.NaOH c.Cu d..Cu(OH)2
②调节溶液pH时,理论上可选择pH最大范围是__________。
(2)由溶液Ⅱ制备CuCl2·2H2O的操作依次为:边滴加浓盐酸边加热浓缩、__________(填操作名称)、过滤、洗涤干燥。
(3)向0.1 mol·L-1的CuCl2溶液中通入H2S气体,溶液变浑浊,pH减小,用离子方程式解释其原因: 若KSP[CuS]=1.2×10-36 ,则生成沉淀时需要S2-的浓度为 mol·L-1。
(4)某学习小组用碘量法测定CuCl2·2H2O样品的纯度(杂质不发生反应)。实验如下:
a.准确称取CuCl2·2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250 mL待测溶液。(已知:2Cu2++4I-=2CuI+I2)
b.移取25.00 mL待测溶液于锥形瓶中,加几滴指示剂,用c mol·L-1Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL。(已知:I2+2S2O32-=2I-+S4O62-)
①实验中使用的指示剂名称为____________,达到滴定终点时,溶液颜色变化为 。
②该样品中CuCl2·2H2O 的质量分数为_________(用含m、c、V的代数式表示,不用化简)。
高二化学实验题极难题查看答案及解析