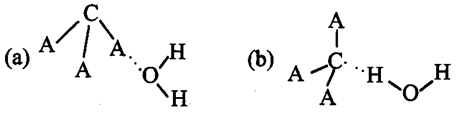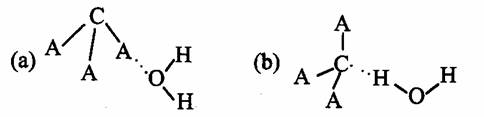-
【选修3:物质的结构与性质】Ⅰ.氟元素是电负性最大的非金属元素,且氟原子的半径小,因此氟单质极易和金属单质反应且把它们氧化到最高价态,如MnF7 、VF5 、CaF2 等。氟元素还可以和氧元素形成氟化物,如OF2 等。
请回答下列问题:
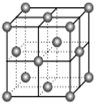
(1)V原子的核外电子排布式为 。如图表示一个不完整的CaF2 晶胞,则图中实心球表示 (填“F-或Ca2+ )。 设晶胞边长为a,则最近的F-和Ca2+之间的距离为 (用含a的代数式表示)。
(2)OF2 分子中氧原子的轨道杂化类型为 ,OF2被称为氟化物而不被称为氧化物的原因是 。
Ⅱ.纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2的化合物。回答下列问题:
(3)写出基态Cu+ 的核外电子排布式 。C、N、O三种元素的第一电离能由大到小的顺序是 。
(4)如图所示是铜的某种氧化物的晶胞示意图,该氧化物的化学式为 。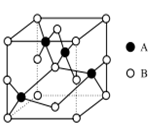
(5)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,在滴加氨水至沉淀刚全部溶解时可得到蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色的[Cu(NH3)4]SO4·H2O沉淀。该深蓝色沉淀中的NH3通过键与中心离子Cu2+结合。NH3分子中的N原子杂化方式是 。与NH3分子互为等电子体的一种微粒是 (任写一种)
-
【选修3:物质的结构与性质】Ⅰ.氟元素是电负性最大的非金属元素,且氟原子的半径小,因此氟单质极易和金属单质反应且把它们氧化到最高价态,如MnF7 、VF5 、CaF2 等。氟元素还可以和氧元素形成氟化物,如OF2 等。
请回答下列问题:
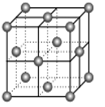
(1)V原子的核外电子排布式为 。如图表示一个不完整的CaF2 晶胞,则图中实心球表示 (填“F-或Ca2+ )。 设晶胞边长为a,则最近的F-和Ca2+之间的距离为 (用含a的代数式表示)。
(2)OF2 分子中氧原子的轨道杂化类型为 ,OF2被称为氟化物而不被称为氧化物的原因是 。
Ⅱ.纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2的化合物。回答下列问题:
(3)写出基态Cu+ 的核外电子排布式 。C、N、O三种元素的第一电离能由大到小的顺序是 。
(4)如图所示是铜的某种氧化物的晶胞示意图,该氧化物的化学式为 。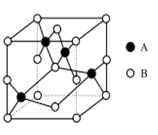
(5)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,在滴加氨水至沉淀刚全部溶解时可得到蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色的[Cu(NH3)4]SO4·H2O沉淀。该深蓝色沉淀中的NH3通过键与中心离子Cu2+结合。NH3分子中的N原子杂化方式是 。与NH3分子互为等电子体的一种微粒是 (任写一种)
-
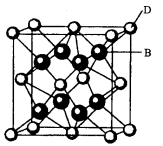
【化学一一选修物质结构与性质】(15分)有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物, D与B可形成离子化合物其晶胞结构如图所示。请回答下列问题。
(1)E元素原子基态时的价电子排布式为 ;
(2)A2F分子中F原子的杂化类型是 _____ ;
(3)C元素与氧形成的离子CO2-的立体构型是__________;写出一种与CO2-互为等电子体的分子的分子式________;
(4)将E单质的粉末加入CA3的浓溶液中,通入O2,充分反应后溶液呈深蓝色,该反应的离子方程式是______________________________________________________;
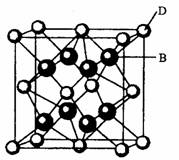
(5)从图中可以看出,D跟B形成的离子化合物的化学式为 ;若离子化合物晶体的密度为ag·cm-3,则晶胞的体积是 (写出表达式即可)。
-
[化学一一选修物质结构与性质](15分)
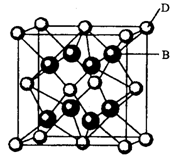
有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物,D与B可形成离子化合物其晶胞结构如右图所示。请回答下列问题。
(1)E元素原子基态时的电子排布式为________;
(2)A2F分子中F原子的杂化类型是________,F的氧化物FO3分子空间构型为________;
(3)CA3极易溶于水,其原因主要是________,试判断CA3溶于水后,形成CA3·H2O的合理结构________(填字母代号),推理依据是:
________。
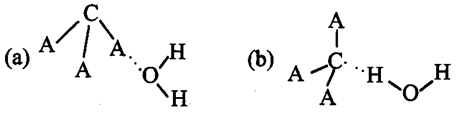
(4)从图中可以看出,D跟B形成的离子化合物的化学式为________;该离子化合物晶体的密度为ag·cm-3。,则晶胞的体积是________(写出表达式即可)。
-
[化学一一选修物质结构与性质](15分)
有A、B、C、D、E、F六种元素,A是周期表中原
子半径最小的元素,B是电负性最大的元素,C的2p轨
道中有三个未成对的单电子,F原子核外电子数是B与
C核外电子数之和,D是主族元素且与E同周期,E能
形成红色(或砖红色)的E2O和黑色的EO两种氧化物,
D与B可形成离子化合物其晶胞结构如右图所示。请
回答下列问题。
(1)E元素原子基态时的电子排布式为________;
(2)A2F分子中F原子的杂化类型是________,F的氧化物FO3分子空间构型为
________;
(3)CA3极易溶于水,其原因主要是________,试判断CA3溶于水后,形成CA3·H2O的合理结构________(填字母代号),推理依据是:
________。(4)从图中可以看出,D跟B形成的离子化合物的化学式为________;该离子化合物晶体的密度为ag·cm-3。,则晶胞的体积是________(写出表达式即可)。
-
【化学一一选修物质结构与性质】(15分)
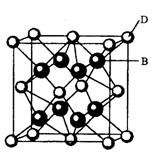
有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物, D与B可形成离子化合物其晶胞结构如图所示。
请回答下列问题。
(1)E元素原子基态时的价电子排布式为 ;
(2)A2F分子中F原子的杂化类型是 ;
(3)C元素与氧形成的离子CO2-的立体构型是__________;写出一种与CO2-互为等电子体的分子的分子式________;
(4)将E单质的粉末加入CA3的浓溶液中,通入O2,充分反应后溶液呈深蓝色,该反应的离子方程式是______________________________________________________;
(5)从图中可以看出,D跟B形成的离子化合物的化学式为 ;若离子化合物晶体的密度为ag·cm-3,则晶胞的体积是 (写出表达式即可)。
-
【化学选修3:物质结构与性质】A、B、C、D、E五种元素的原子序数依次增大,其中非金属元素A的基态原子中成对电子数是未成时电子数的两倍,C元素在地壳中含量最高,D的单质是短周期中熔点最低的金属,E的合金是我国使用最早的合金。
(1)E元素的基态原子电子排布式为__________________。
(2)A的某种氢化物A2H2分子中含有___个σ键和____个π键。
(3)A 的含氧酸根离子AO3n-的空间构型是___________。
(4)B的最简单的氢化物的沸点比A 的最简单的氢化物的沸点高得多,其原因是_____。
(5)E的最高价氧化物对应的水化物溶解于氨水中生成的复杂化合物的化学式是______。
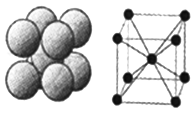
(6)下图是D单质的晶体堆积方式,这种堆积方式的晶胞中原子的配位数为____,若该原子的半径为rpm ,此晶体的密度ρ=______g/cm3(用含r的代数式表示,阿伏伽德罗常数用NA表示)。
-
[化学——选修3:物质结构与性质]
(1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。单位质量的A和B单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
| 电离能(KJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15399 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
①某同学根据上述信息,推断B的核外电子排布如下图所示,该同学所画的电子排布图违背 ,B元素位于周期表五个区域中的 区。
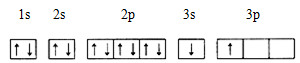
②ACl2分子中A的杂化类型为 ,ACl2的空间构型为 。
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①以体心立方堆积形成的金属铁中,其原子的配位数为 。
②写出一种与CN-互为等电子体的单质的电子式 。
③六氰合亚铁离子[Fe(CN)6]4-中不存在 。
A.共价键
B.非极性键
C.配位键
D.σ键
E.π键
(3)一种Al-Fe合金的立体晶胞如右图所示。请据此回答下列问题:
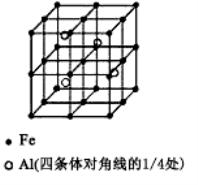
①确定该合金的化学式 。
②若晶体的密度=ρ g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为 cm。
-
[化学-选修物质结构与性质]
纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.
单位质量的A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
(1)某同学根据上述信息,推断B的核外电子排布如右图所示,
该同学所画的电子排布图违背了______.
(2)根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为______.
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确______,并阐述理由______.
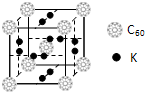
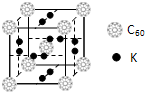
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体.写出基态钾原子的电子排布式______,该物质的K原子和C60分子的个数比为______.
(5)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是______.Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为______.

-
[化学-选修物质结构与性质]
纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.
单位质量的A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
(1)某同学根据上述信息,推断B的核外电子排布如右图所示,
该同学所画的电子排布图违背了______.
(2)根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为______.
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确______,并阐述理由______.
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体.写出基态钾原子的电子排布式______,该物质的K原子和C60分子的个数比为______.
(5)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是______.Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为______.