-
钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从钛白工业废酸(含钪、钛、铁、锰等离子)中提取氧化钪(Sc2O3)的一种流程如下:
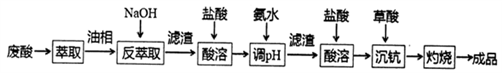
回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是____________________________。
(2)先加入氨水调节PH=3,过滤,滤渣主要成分是_____________;再向滤液加入氨水调节pH=6,滤液中 Sc3+ 的浓度为_____________。[25℃时,Ksp[Mn(OH)2]=1.9×10-13、Ksp [Fe(OH)3]=2.6×10-39,Ksp[Sc(OH)3]=9.0×10-31]
(3)用草酸“沉钪”。25℃时pH=2的草酸溶液中 =______________。写出“沉钪”得到草酸钪的离子方程式___________________________________。
=______________。写出“沉钪”得到草酸钪的离子方程式___________________________________。
[25℃时,草酸电离平衡常数为K1=5.0×10-2,K2=5.4×10-5]
(4)草酸钪“灼烧”氧化的化学方程式为_____________________________________。
(5)废酸中含钪量为15mg·L-1, VL废酸最多可提取Sc2O3的质量为_____________。
-
钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从钛白工业废酸(含钪、钛、铁、锰等离子)中提取氧化钪(Sc2O3)的一种流程如下:
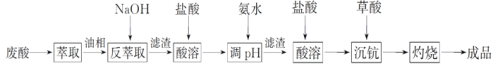
回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是______________________________。
(2)先加入氨水调节pH=3,过滤,滤渣主要成分是__________;再向滤液加入氨水调节pH=6,滤液中Sc3+的浓度为_____________。(已知:Ksp[Mn(OH)2]=1.9×10-13、Ksp[Fe(OH)3]=2.6×10-39,Ksp[Sc(OH)3]=9.0×10-31)
(3)用草酸“沉钪”。25 ℃时pH=2的草酸溶液中 =__________(保留两位有效数字)。写出“沉钪”得到草酸钪的离子方程式__________________________________。[已知Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5]
=__________(保留两位有效数字)。写出“沉钪”得到草酸钪的离子方程式__________________________________。[已知Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5]
(4)草酸钪“灼烧”氧化的化学方程式为______________________________________________。
(5)废酸中含钪量为15 mg·L-1,V L废酸最多可提取Sc2O3的质量为____________。
-
钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从钛白工业废酸(含钪、钛、铁、锰等离子)中提取氧化钪(Sc2O3)的一种流程如下:
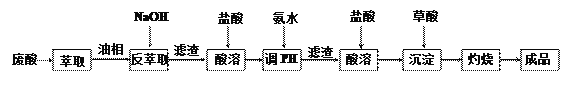
回答下列问题:
(l)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是________________________________。
(2)25℃时,先加入氨水调节pH =3,过滤,滤渣主要成分是_______;再向滤液加入氨水调节pH=6,滤液中Sc3+的浓度为________。Ksp[ Mn(OH)2]=1.9×10-13、Ksp[Fe(OH)3]=2.6×10-39,Ksp[Sc(OH)3]=9.0×10-31]
(3)用草酸“沉钪”。25℃时pH=2的草酸溶液中 =_______(保留两位有效数字)。写出“沉钪”得到草酸钪的离子方程式_________。(已知Kal(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5)
=_______(保留两位有效数字)。写出“沉钪”得到草酸钪的离子方程式_________。(已知Kal(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5)
(4)草酸钪“灼烧”氧化的化学方程式为_____________。
(5)废酸中含钪量为15mg/L,V L废酸最多可提取Sc2O3的质量为____________。
-
钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从钛白工业废酸(含钪、钛、铁、锰等离子)中提取氧化钪(Sc2O3)的一种流程如下:
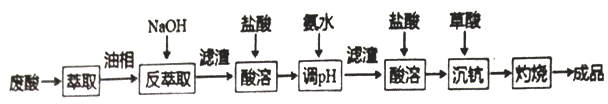
回答下列问题:
(l)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是__________。
(2)先加入氨水调节pH =3,过滤,滤渣主要成分是_______;再向滤液加入氨水调节pH=6,滤液中Sc3+的浓度为________。[己知:Ksp[Mn(OH)2]=1.9×10-13、Ksp[Fe(OH)3]=2.6×10-39,Ksp[Sc(OH)3]=9.0×10-31]
(3)用草酸“沉钪”。25℃时pH=2的草酸溶液中 =_______(保留两位有效数字)。写出“沉钪”得到草酸钪的离子方程式_________。
=_______(保留两位有效数字)。写出“沉钪”得到草酸钪的离子方程式_________。
(已知Kal(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5)
(4)草酸钪“灼烧”氧化的化学方程式为_____________。
(5)废酸中含钪量为15mg/L,V L废酸最多可提取Sc2O3的质量为____________。
-
钪(Sc)及其化合物在电子、宇航、超导等方面有着广泛的应用。某工厂的钛白水解工业废酸中,Sc3+浓度为18mg/L,还含有大量的TiO2+、Fe3+、H+、SO42-等。下图为从该工业废酸中提取Sc2O3的一种流程。

回答下列问题:
(1)在钛白水解工业废酸中,加入双氧水是为了使TiO2+转化为难萃取的[Ti(O2)(OH(H2O)4]+。[Ti(O2)(OH(H2O)4]+中Ti 的化合价为+4,其中非极性键的数目为_______。
(2)钪的萃取率(E%)与O/A 值[萃取剂体积(O)和废酸液体积(A)之比]的关系如左下图,应选择的最佳O/A值为_______;温度对钪、钛的萃取率影响情况见右下表,合适的萃取温度为10-15℃,其理由是_____________________。

(3)洗涤“油相“可除去大量的钛离子。洗染水是用浓硫酸、双氧水和水按一定比例混合而成。混合过程的实验操作为________________。
(4)25℃时,用氨水调节滤液的pH,当pH=3.5时,滤渣II的主要成分是_______;当pH=6时,滤液中Sc3+的浓度为________。(Ksp[Fe(OH)3]=2.6×10-39,Ksp[Sc(OH)3]=9.0×10-31)
(5)写出用草酸(H2C2O4)“沉钪”得到Sc2(C2O4)3的离子方程式_____________。
(6)若从1m3该工厂的钛白水解度酸中提取得到24.4gSc2O3,则钪的提取率为______(保留三位有效数字)。
-
钪(Sc)及其化合物在电子、宇航、超导等方面有着广泛的应用。某工厂的钛白水解工业废酸中Sc3+浓度为18mg/L,还含有大量的TiO2+、Fe3+、H+、SO42-等。下图为从该工业废酸中提取Sc2O3的一种流程。

回答下列问题:
(1)在钛白水解工业废酸中,加入双氧水是为了使TiO2+转化为难萃取的[Ti(O2)(OH)(H2O)4]+。[Ti(O2)(OH)(H2O)4]+中Ti的化合价为+4价,其中非极性键的数目为______________。
(2)钪的萃取率(E%)与O/A值[萃取剂体积(O)和废酸液体积(A)之比的关系如下图,应选择的合适O/A值为__________;温度对钪、钛的萃取率影响情况见下表,合适的萃取温度为10~150C,其理由是________________________________________。

(3)洗涤“油相”可除去大量的钛离子。洗涤水是用浓硫酸、双氧水和水按一定比例混合而成。混合过程的实验操作为__________________。
(4)25℃时,用氨水调节滤液的pH,当pH=3.5时,滤渣Ⅱ的主要成分是_________,当pH=6时,滤液中Sc3+的浓度为_________。(Ksp[Fe(OH)3]=2.6×10-39;Ksp[Sc(OH)3]=9.0×10-31)
(5)写出用草酸(H2C2O4)“沉钪”得到Sc2(C2O4) 3的离子方程式__________________。
(6)若从1m3该工厂的钛白水解废酸中提取得到24.4gSc2O3,则钪的提取率为_________(保留三位有效数字)
-
镓(31Ga)是一种重要金属元素,镓及其化合物在电子工业、光电子工业、国防工业和超导材料等领域有着广泛的应用。回答下列问题:
(1)基态Ga原子占据最高能级电子的电子云轮廓图形状为__________,未成对电子数为________________。
(2)Ga(NO3)3中阴离子的立体构型是_____________,写出一个与该阴离子的立体构型相同的分子的化学式___________。
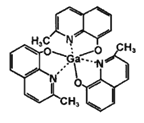
(3)2-甲基-8-羟基喹啉镓(如图)应用于分子印迹技术,2-甲基-8-羟基喹啉镓中五种元素电负性由大到小的顺序是____________________________(填元素符号),提供孤电子对的成键原子是_____________。
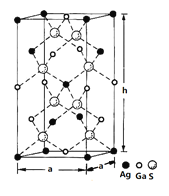
(4)一种硅镓半导体材料的晶胞结构如图所示由硫、镓、银形成的化合物的晶胞是底面为正方形的长方体,结构如下图所示,则该晶体中硫的配位数为___________,晶胞底面的边长a=5.75 nm,高h=10.30nm,该晶体密度为__________________g·cm-3(列出计算式即可)。
-
镓(31Ga)是一种重要金属元素,镓及其化合物在电子工业、光电子工业、国防工业和超导材料等领域有着广泛的应用。回答下列问题:
(1)基态Ga原子占据最高能级电子的电子云轮廓图形状为__________,未成对电子数为________________。
(2)Ga(NO3)3中阴离子的立体构型是_____________,写出一个与该阴离子的立体构型相同的分子的化学式___________。
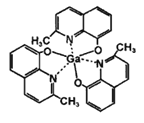
(3)2-甲基-8-羟基喹啉镓(如图)应用于分子印迹技术,2-甲基-8-羟基喹啉镓中五种元素电负性由大到小的顺序是____________________________(填元素符号),提供孤电子对的成键原子是_____________。
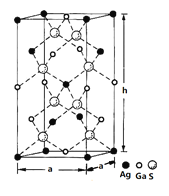
(4)一种硅镓半导体材料的晶胞结构如图所示由硫、镓、银形成的化合物的晶胞是底面为正方形的长方体,结构如下图所示,则该晶体中硫的配位数为___________,晶胞底面的边长a=5.75 nm,高h=10.30nm,该晶体密度为__________________g·cm-3(列出计算式即可)。
-
[化学——选修2:化学与技术]碲及其化合物具有许多优良性能,被广泛用于冶金、化工、医药卫生等工业领域。铜阳极泥(主要成分除含Cu、Te外,还有少量Ag和Au)经如下工艺流程得到粗碲。
(1)“加压硫酸浸出”过程中会发生以下化学反应:Cu2Te+2O2=2CuO+TeO2 ;TeO2+H2SO4=TeOSO4+H2O
①Ag2Te也能与O2发生类似Cu2Te的反应,化学方程式为____________。
②工业上给原料气加压的方法是________。
(2)操作Ⅰ是________。
(3)“含碲浸出液”的溶质成分除了TeOSO4外,主要是____________(填化学式)。
(4)“电 解沉积除铜”时,将“含碲浸出液”置于电解槽中,铜、碲沉淀的关系如下图。电解初始阶段阴极的电极反应式是________。
解沉积除铜”时,将“含碲浸出液”置于电解槽中,铜、碲沉淀的关系如下图。电解初始阶段阴极的电极反应式是________。
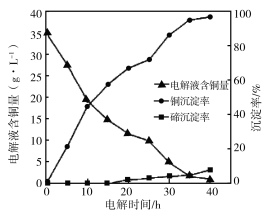
(5)向“含碲硫酸铜母液”通入SO2并加入NaCl反应一段时间后,Te(IV)浓度从6.72 g·L-1下降到0.10 g·L-1,Cu2+浓度从7.78 g·L-1下降到1.10 g·L-1。
①TeOSO4生成Te的化学方程式为________。
②研究表明,KI可与NaCl起相同作用,从工业生产的角度出发选择NaCl最主要的原因是________。
③计算可得Cu2+的还原率为85.9%,Te(IV)的还原率为________。
-
碲及其化合物具有许多优良性能,被广泛用于冶金、化工、医药卫生等工业领域。铜阳极泥(主要成分除含Cu、Te外,还有少量Ag和Au)经如下工艺流程得到粗碲。

(1)“加压硫酸浸出”过程中会发生以下化学反应:
Cu2Te+2O2=2CuO+TeO2 ;TeO2+H2SO4=TeOSO4+H2O
①Ag2Te也能与O2发生类似Cu2Te的反应,化学方程式为________。
②工业上给原料气加压的方法是________。
(2)操作Ⅰ是________。
(3)“含碲浸出液”的溶质成分除了TeOSO4外,主要是________(填化学式)。
(4)“电解沉积除铜”时,将“含碲浸出液”置于电解槽中,铜、碲沉淀的关系如下图。电解初始阶段阴极的电极反应式是________。

(5)向“含碲硫酸铜母液”通入SO2并加入NaCl反应一段时间后,Te(IV)浓度从6.72 g·L-1下降到0.10 g·L-1,Cu2+浓度从7.78 g·L-1下降到1.10 g·L-1。
①TeOSO4生成Te的化学方程式为________。
②研究表明,KI可与NaCl起相同作用,从工业生产的角度出发选择NaCl最主要的原因是________。
③计算可得Cu2+的还原率为85.9%,Te(IV)的还原率为________。

=______________。写出“沉钪”得到草酸钪的离子方程式___________________________________。













