-
我国是氧化铝生产大国,工业上每生产1 t氧化铝将排出1~2 t赤泥,赤泥大量堆积会对环境造成严重污染。赤泥中主要成分及含量:CaO约占46%、SiO2约占22%、Al2O3约占7%、Fe2O3约占11%、TiO2约占5%及少量其他物质。
(1)一种利用废弃赤泥的方法是将赤泥配成一定的液固比,作为一种吸收剂,吸收热电厂排放的含SO2的烟气,写出吸收SO2时可能发生的化学反应方程式______________________。
(2)为综合利用赤泥中的各种成分,某科研小组设计了如下工艺流程:
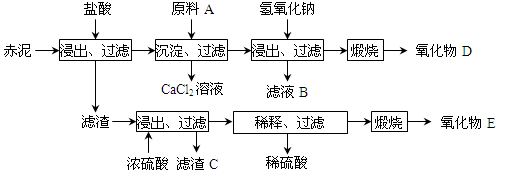
已知:TiO2不溶于稀盐酸、稀硫酸,能溶于浓硫酸生成TiOSO4(硫酸氧钛,易水解)。
①氧化物D的化学式是_____________,原料A最好是下列物质中的____________。
A.氨水 B.氢氧化钠 C.生石灰 D.双氧水
②写出上述工艺中投入氢氧化钠时反应的离子方程式_________________________。
③写出上述工艺中稀释时发生水解反应的化学方程式__________________________。
-
治理SO2、CO、NOx污染是化学工作者研究的重要课题。
Ⅰ.硫酸厂大量排放含SO2的尾气会对环境造成严重危害。
(1)工业上可利用废碱液(主要成分为Na2CO3)处理硫酸厂尾气中的SO2,得到Na2SO3溶液,该反应的离子方程式为______。
Ⅱ.沥青混凝土可作为反应;2CO(g)+O2(g)⇌2CO2(g)的催化剂。如图表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
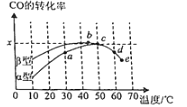
(2)a、b、c、d四点中,达到平衡状态的是______。
(3)已知c点时容器中O2浓度为0.02mol•L-1,则50℃时,在α型沥青混凝土中CO转化反应的平衡常数K=______(用含x的代数式表示)。
(4)观察分析图,回答下列问题:

①CO转化反应的平衡常数K(a)______K(c)。
②在均未达到平衡状态时,同温下β型沥青混凝土中CO转化速率比α型要______(填“大”、“小”)。
③______点时CO与O2分子之间发生有效碰撞的几率在整个实验过程中最高。
-
防治环境污染,保护生态环境已成为全人类的共识。
①近年,我国不少地区雾霾天气频发,给人们的生产生活和健康造成了严重影响。导致雾霾形成的主要污染物是________。
空气污染指数是根据空气中SO2、________和可吸入颗粒物等污染物的浓度计算出来的数值。
② 燃煤产生的CO2、SO2经处理可生产多种化工产品。将CO2通入氨的氯化钠饱和溶液中可制得碳酸氢钠,该反应的化学方程式为____________________________。
SO2经石灰石—石膏法或氨水法处理后可分别得到副产品石膏(CaSO4·2H2O)和硫酸铵,这两种副产品中,硫元素的质量分数较高的是______________(填化学式)。
③ 工业废水中的重金属离子的去除,通常采用加入适量碱控制废水的pH,将重金属离子转化为________(填“盐”“氧化物”或“氢氧化物”)的形式而沉淀除去。“地沟油”流入餐桌已严重威胁到人的健康,综合利用“地沟油”的一种方法是将其发生________(填“氧化”“水解”或“加成”)反应以获取甘油和高级脂肪酸。
-
下列有关燃料的说法错误的是( )
A.含硫化石燃料的大量燃烧是形成酸雨的主要原因
B.绿色化学的核心就是利用化学原理对工业生产上造成的环境污染进行彻底治理
C.以压缩天然气、液化石油气代替燃油可减少大气污染
D.燃料不完全燃烧排放的CO是大气污染物之一
-
工业废水随意排放会造成严重污染,根据成分不同可采用不同的处理方法。
(1)电池生产工业废水中常含有Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去。已知室温下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2。
①请用离子方程式说明上述除杂的原理______________________。
②FeS高温煅烧产生的SO2气体通入下列溶液中,能够产生沉淀的是_________(填序号)
A.Ba(NO3)2 B.BaCl2
C.Ba(OH)2 D.溶有NH3的BaCl2溶液
③已知元素在高价态时常表现氧化性,若在酸性CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀,则生成CuCl的离子方程式是___________。
(2)电解法处理酸性含铬废水(主要含有Cr2O72-)时,在废水中加入适量NaCl,以铁板作阴、阳极,处理过程中存在如下反应Cr2O72+6Fe2++14H+═2Cr3++6Fe3++7H2O,最后Cr3+ 以Cr(OH)3形式除去,下列说法不正确的是______(填序号)
A.阳极反应为Fe-2e-═Fe2+
B.电解过程中溶液pH减小
C.过程中有Fe(OH)3沉淀生成
D.电路中每转移12 mol电子,最多有2mol Cr2O72-被还原
(3)废氨水可以转化成氨,氨再设计成碱性燃料电池。右图是该燃料电池示意图,产生的X气体可直接排放到大气中,a电极作_________极(填“正”“负”“阴”或“阳”),其电极反应式为___________。
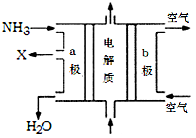
-
水是人类赖以生存的重要物质,而水污染却严重影响着人类的生存环境。目前,不会造成水污染的是
A. 降雨淋洗将大气中的污染物冲入水中
B. 农田排水
C. 冰川融化
D. 工业生产中废渣、废液的任意排放
-
随着上海工农业生产的发展和城市居民生活水平的提高,环境污染日趋严重。每天有大量的工业废水和生活污水排入黄浦江;农村养殖、耕作方式发生了改变,猪饲料由“水花生”等天然饲料转变为人工复合饲料。农作物施肥由人畜粪尿变成以化肥为主,而大量的人畜粪尿也被倒入河流,造成黄浦江水体严重污染,生态平衡严重失调。请根据以上资料分析:
(1)造成黄浦江水污染的主要原因是 。
(2)造成黄浦江水域“水花生”大量生长繁殖的元凶是
① ;② 。
(3)控制黄浦江水体污染的根本措施是 。
-
某市晚报曾报道,该市七条交通主干道的空气污染严重,其主要原因是( )。
A.燃烧煤所排放的废气造成的
B.几十万辆汽车、助力车等排放的废气造成的
C.工业生产中的废渣、废水、废气造成的
D.不断地降雨和各种污水造成的
-
水是人类赖以生存的重要物质,而水体污染却严重影响着人类的生存环境。目前,水体污染主要来自( )
①工业生产中废渣、废液的任意排放 ②雨水和土壤接触③农业生产中农药、化肥的过量使用④城市生活污水的任意排放 ⑤生活垃圾和废旧电池的随意丢弃
A.①②③⑤ B.②③④⑤ C.①③④⑤ D.①②③④⑤
-
水是人类赖以生存的重要物质,而水污染却严重影响着人类的生存环境。目前,水污染主要来自( )
①工业生产中废渣、废液的任意排放 ②雨水和土壤接触 ③农业生产中农药、化肥的过量使用 ④城市生活污水的任意排放 ⑤生活垃圾和废旧电池的随意丢弃
A. ①②③⑤ B. ②③④⑤ C. ①③④⑤ D. ①②③④⑤


