-
(1)在试管里放入一小块铜片,注入一定体积的浓硫酸,给试管加热,使之反应。若铜片还有剩余硫酸是否消耗完毕?
①结论及理由是:_________________________________________。
②向100毫升18 mol/L的H2SO4溶液中加入足量的铜片并加热,充分反应后,被还原的H2SO4的物质的量________
A.小于0·9 mol B.等于0·9 mol C.在0·9 mol与1.8 mol之间 D.大于1·8 mol
③50g的胆矾加热到100℃失去部分结晶水后,质量变为35.6g,则失去水后的硫酸铜晶体的化学式是________
A.CuSO4·H2O B.CuSO4·2H2O C.CuSO4·3H2O D.CuSO4
(2)足量的锌投入到一定量的浓硫酸中,充分反应后共收集到SO2和H222.4L(标准状况)。
①简述能产生H2的原因是______________________________
②上述变化中体现浓硫酸强氧化性的反应方程式是:________
③反应共消耗金属锌的质量为_________g。
④以上数据能否计算出消耗的硫酸的物质的量? _________(填“能”或“不能”)
高一化学填空题中等难度题查看答案及解析
-
在试管里放入一块铜片,注入一定体积的浓硫酸,给试管加热,使之反应。
(1)若铜片还有剩余,硫酸________消耗完毕(填“已”或 “没有”)。其理由是___________________________________________________________________。
(2)用一定量的废铜屑制取胆矾,有两种方法:一种是取Cu与浓H2SO4直接反应;二是先将铜在空气中加热使之生成CuO,再与稀H2SO4反应,其中_________种方法好,理由是 _____________________________________________________。
高一化学填空题中等难度题查看答案及解析
-
在一支试管里放入一小块铜片,注入一定体积的浓硫酸,再给试管加热,充分反应。
(1)写出反应的化学方程式_________________;若试管中铜片还有剩余,硫酸_________(填“已”或“未”)消耗完毕,其理由是 __________________________;
(2)若反应中有0.02molH2SO4被还原,则在标准状况下收集到的气体体积为__________mL,参加反应的铜的质量为____g。
高一化学填空题中等难度题查看答案及解析
-
某化学兴趣小组为探索铜与浓硫酸的反应,用如图所示装置进行有关实验。
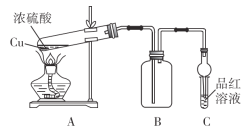
甲组取a g铜片和一定量的浓硫酸放入试管中加热,直到反应完毕,最后发现试管中还有一定量的H2SO4和Cu剩余。
(1)写出装置A中所发生反应的化学方程式:_______________________________。
(2)若用含0.2 mol H2SO4的浓硫酸与过量铜片共热,能否收集到0.1 mol SO2:______(填“能”或“不能”)。
(3)当集气瓶B中的气体收集满时,装置C中有可能观察到的现象是_____________。
(4)为什么有一定量的余酸却未能使Cu完全溶解,你认为原因是_________________。
(5)乙组同学认为:实验装置C有可能造成环境污染,乙组同学设计了最简单方法给予解决:在C试管口塞上一团沾有_________(填化学式)溶液的棉花。
(6)为了证明反应结束后的试管中的确有剩余的稀硫酸,可选择的试剂是_______。
A.铁粉 B.Na2CO3溶液 C.BaCl2溶液 D.NaOH溶液
高一化学实验题中等难度题查看答案及解析
-
某化学课外兴趣小组探究铜与浓硫酸的反应情况.甲.乙.丙三位同学进行了下列实验:取12.8g铜片和20ml.18mol/L的浓硫酸放在圆底烧瓶中共热,直至反应完毕,最后发现烧瓶中还有铜片剩余外,同时根据所学的知识认为还有较多的硫酸剩余.
(1)请写出铜跟浓硫酸反应的化学方程式: ,
试问:为什么较多的余酸不再与铜片继续反应?简述理由: .
可以证明有余酸的实验方案是 (填写字母,错选或多选扣分).
a.再加入铁粉 b.再滴入BaCl2溶液
c.再加入银 d.再滴入Na2CO3溶液
(2)甲学生设计求余酸浓度的实验方案是测定产生气体的量.其方法有多种,请问下列方案中不可行的是 (填写字母,错选或多选扣分).
a.将产生的气体缓缓通过预先称量盛有碱石灰的干燥管,结束反应后再次称量.
b.将产生的气体缓缓通入酸性高锰酸钾溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀.
c.用排水法测定其产生气体的体积(折算成标准状况).
d.用排饱和NaHSO3溶液的方法测出其产生气体的体积(折算成标准状况).
(3)乙同学设计测定余酸浓度的实验方案是:测定反应后的混合液中Cu2+的量.在反应后的溶液中加蒸馏水稀释至100ml,加入足量Na2S溶液,充分反应后,过滤.洗涤.干燥、称量沉淀.请写出生成沉淀的离子方程式: .
(4)根据甲、乙两同学的实验方案,除测算产生气体的物质的量或反应掉的铜的物质的量外,尚缺少的测量数据是 .
(5)丙同学提出甲、乙两同学的实验方案设计的复杂,为此他设计了下列较为简易的实验方案:取出反应后的铜片,进行洗涤.干燥.称量.若称得剩余铜片的质量为Wg,测得反应后溶液的体积为Vml,请计算剩余硫酸的物质的量浓度= mol/L(用含W.V的代数式表示)
高一化学实验题困难题查看答案及解析
-
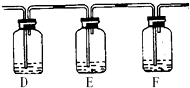
某中学高一课外兴趣小组为探究铜跟硫酸的反应情况,设计了如图所示装置进行有关实验.
(1)先关闭活塞a,将6.4g铜片和12mL某浓度的浓硫酸放在圆底烧瓶中共热至反应完毕,发现烧瓶中还有铜片剩余.再打开活塞a,将气球中的氧气缓缓挤入圆底烧瓶,最后铜片完全消失.
写出上述过程中烧瓶内发生的化学方程式:
关闭活塞a________;
打开活塞a________;
(2)该小组甲同学对“如何检验SO2中混有少许CO2”这个问题很感兴趣,他将A中铜片换作木炭粉,并在A、B之间连接了如下装置:
试剂:a.NaOH溶液 b.品红溶液 c.酸性KMnO4溶液 d.Ca(OH)2溶液
请回答:
①该同学的实验装置A中发生的化学方程式:________.
②若要达到此目的,可以在:(填所提供试剂编号)
D中加入________;E中加入________;F中加入________.
(3)事实证实,第(1)问铜片完全消失后,硫酸仍有剩余,乙同学欲测定余酸的物质的量浓度,假设反应前后溶液体积变化忽略不计,他向反应后溶液中加入含溶质a mol的NaOH溶液刚好使溶液中Cu2+全部沉淀.据此,他能求出余酸的物质的量浓度吗?若能,请写出余酸物质的量浓度的表达式:________mol/L(用含a的代数式表达,若不能,该空不填).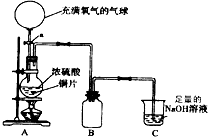
高一化学填空题中等难度题查看答案及解析
-
(9分)某研究性学习小组利用废铜制取CuSO4:
(1) 甲学生进行了下列实验:取含6.4g铜的废铜和10ml 18ml·L-1浓硫酸放在圆底烧瓶中共热,起到反应完毕,最后发现烧瓶中还有铜片剩余。他根据自己所学的化学知识,认为烧瓶中还有较多的硫酸剩余。你认为他的判断是否正确________,其理由是:________
________。
写出相关的化学方程式:________。
(2) 乙同学认为甲设计的实验方案不好,他自己设计的思路是:2Cu+O2==2CuO;CuO+H2SO4
==CuSO4+H2O。对比甲的方案,乙同学的优点是:________
________。
(3) 丙同学采用向含有废铜屑的热的稀H2SO4中,不断通入空气也能制备CuSO4,请写出相关的化学方程式:________。
高一化学填空题简单题查看答案及解析
-
在一支试管中放入一块很小的铜片,再加入少量浓硫酸,然后把试管固定在铁架台上。把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中。塞紧试管口,在玻璃导管口处缠放一团蘸有
溶液的棉花。给试管加热,观察现象。当反应一段时间以后,停止加热。回答下列问题:

(1)写出a处反应的化学方程式________,
浓硫酸所体现的作用是________性。
(2)试管中的液体反应一段时间后,处滤纸条的变化为________。待试管中反应停止后,给玻璃管放有蘸过品红溶液的滤纸处微微加热,滤纸条的变化为________。
(3)待试管中液体冷却后,取试管上层液体加入一支试管中,再慢慢加入少量水,可观察溶液呈________色。
(4)玻璃导管口处缠放一团蘸有Na2CO3溶液的棉花所起的作用是________
(5)如果浓硫酸的浓度为
,铜片是过量的,加热使之反应,当被还原的硫酸为
。则浓硫酸的实际体积________(填写“大于”、“等于”或“小于”)
。
高一化学实验题中等难度题查看答案及解析
-
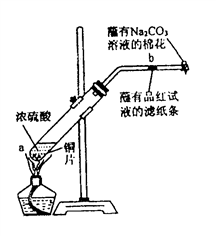
在一支试管中放入一块很小的铜片,再加入少量浓硫酸,然后把试管固定在铁架台上。把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中。塞紧试管口,在玻璃导管口处缠放一团蘸有
溶液的棉花。给试管加热,观察现象。当试管中的液体逐渐透明时,停止加热。
回答下列问题:
(1)写出a处反应的化学方程式____________________________________________。
(2)试管中的液体反应一段时间后,
处滤纸条的变化为_____________。待试管中反应停止后,给玻璃管放有蘸过品红溶液的滤纸处微微加热,滤纸条的变化为_______。
(3)待试管中液体冷却后,将试管上层液体倒去,再慢慢加入少量水,可观察溶液呈______色。
(4)玻璃导管口处缠放一团蘸有Na2CO3溶液的棉花所起的作用是____________
(5)如果浓硫酸的浓度为
,铜片是过量的,加热使之反应,当被还原的硫酸为
。则浓硫酸的实际体积_____________(填写“大于”、“等于”或“小于”)
。
高一化学实验题困难题查看答案及解析
-
在浓硝酸中放入铜片,若铜有剩余,待反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,其原因是 (用离子方程式解释)。
若将9.60g铜跟一定量的浓硝酸反应,铜消耗完时,共产生气体4.48L(标准状况),则被还原的硝酸的物质的量是 mol,所得气体的平均相对分子质量为 。
高一化学填空题困难题查看答案及解析