-
雷尼镍( Raney-Ni)是一种多孔结构的镍铝合金,对氢气具有强吸附性,是烯烃、炔烃氢化反应的高效催化剂。一种以铜镍渣( 主要含Cu、Fe、Co和Ni)生产雷尼镍的流程如下:

下表列出了有关金属离子生成氢氧化物沉淀的pH:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.3 | 9.9 | 9.2 |
(1)“酸浸”时,如通入空气并不断搅拌,可将“滤渣1”氧化溶解,离子方程式为___________。
(2)“除铁”时,先加入适量H2O2 氧化Fe2+,理论上消耗的n(H2O2):n(Fe2+)=____;再加入NiO以调节溶液的pH。应控制pH的范围为__________________。
(3)“电解”(以惰性材料作电极)是为了获得单质镍。电解产物中可循环利用的物质是_______。
(4)“碱浸”是为了形成多孔结构的雷尼镍,反应的离子方程式为_________________。使用新制雷尼镍进行氢化反应时,不加氢气也可实现氢化的目的,原因是____________________。
(5)“滤液”主要成分与过量CO2 反应的离子方程式为__________________________。
-
(12分)
雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,由镍-铝合金为原料制得。
(1)元素第一电离能:Al▲ Mg(选填:“>”、“<”、“=”)
(2)雷尼镍催化的一实例为:

化合物b中进行sp3杂化的原子有:▲ 。
(3)一种铝镍合金的结构如下图,与其结构相似的化合物是:▲ (选填序号)。
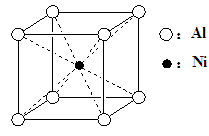
a.氯化钠 b.氯化铯 c.石英 d.金刚石
(4)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀。
①Ni2+在基态时,核外电子排布式为:▲ 。
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为4)。

-
A.雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,由镍-铝合金为原料制得。
(1)元素第一电离能:Al▲ Mg(选填:“>”、“<”、“=”)
(2)雷尼镍催化的一实例为:
化合物b中进行sp3杂化的原子有: ▲ 。
(3)一种铝镍合金的结构如下图,与其结构相似的化合物是:▲ (选填序号:a.氯化钠 b.氯化铯 c.石英 d.金刚石)。

(4)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀。
①Ni在基态时,核外电子排布式为:▲ 。
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为4)。

-
(15分)
雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,由镍-铝合金为原料制得。
(1)元素第一电离能:Al________Mg(选填:“>”、“<”、“=”)
(2)雷尼镍催化的一实例为:
化合物b中进行sp3杂化的原子有:________。
(3)一种铝镍合金的结构如下图,与其结构相似的化合物是:(选填序号:a.氯化钠 b.氯化铯 c.石英 d.金刚石)。

(4)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀。
①Ni在基态时,核外电子排布式为:________。
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为4)。

-
一种带有多孔结构的镍铝合金对H2具有较强的吸附性,其高催化活性和热稳定性使得该镍铝合金被用于很多工业过程中和有机合成反应中。下图是以镍黄铁矿(主要成分为NiS、FeS等)为原料制备该镍铝合金的工艺流程图:
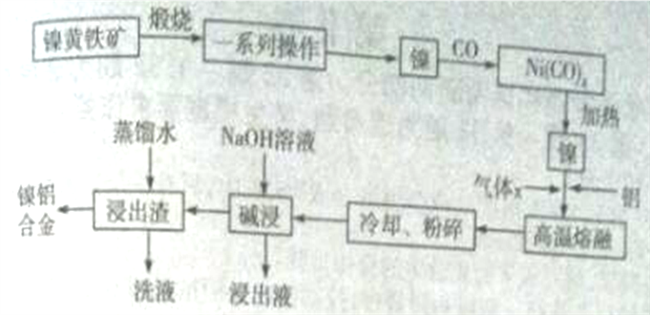
回答下列问题:
(1)Ni(CO)4中C、O化合价与CO中的C、O化合价相同,则Ni化合价为_______价。
(2)在空气中“煅烧”生成Ni2O3和Fe2O3,写出Fe2O3的化学方程式________________。
(3)操作“镍 Ni(CO)4
Ni(CO)4 镍”的目的是__________。
镍”的目的是__________。
(4) Ni、Al高温熔融时,气体x的作用是___________。对“高温熔融”物冷却后,需要进行粉碎处理,粉碎处理的目的是________________。
(5)“碱浸”可以使镍产生多孔结构,从而增强对H2的吸附性,“浸出液”中的主要离子是_____________;“浸出液”中的铝元素可循环利用,写出回收“浸出液”中的铝元素,并制备“高温熔融”时的原料Al的流程:_____________(示例:CuO Cu2+
Cu2+ Cu)。
Cu)。
-
骨架型镍催化剂因其具有多孔结构对氢气有极强吸附性,故常用作加氢反应的催化剂。一种镍铜硫化矿(主要成分为Ni2S和Cu2S)为原料制备骨架型镍的工艺流程如下:
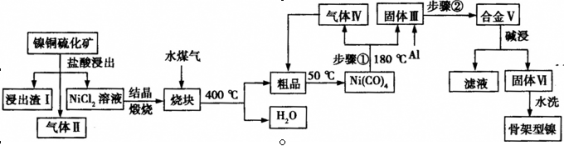
⑴镍铜硫化矿酸浸所得的浸出渣Ⅰ的主要成分是Cu2S,气体Ⅱ中主要含有两种成分,则该步反应的化学方程式为 ;
⑵写出步骤①的化学方程式 。合金Ⅴ在碱浸前要粉碎,粉碎的目的是 ;
⑶碱浸时选择浓NaOH溶液,反应的离子方程式是: ;
⑷碱浸后残铝量对骨架型镍的催化活性有重大影响。分析如图,残铝量在 范围内催化剂活性最高,属于优质产品;
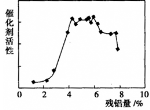
⑸使用新制骨架型镍进行烯烃加氢反应,有时不加入氢气也可以完成反应,原因是 。
-
某金属有机多孔材料FJI-H14在常温常压下对CO2具有超高的吸附能力,并能高效催化CO2与环氧乙烷衍生物的反应,其工作原理如图所示。下列说法不正确的是( )
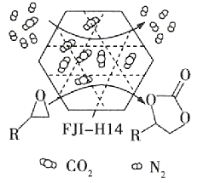
A.该材料的吸附作用具有选择性
B.该方法的广泛使用有助于减少CO2排放
C.在生成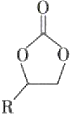 的过程中,有极性共价键形成
的过程中,有极性共价键形成
D.其工作原理只涉及化学变化
-
某金属有机多孔材料FJI-H14在常温常压下对CO2具有超高的吸附能力,并能高效催化CO2与环氧乙烷衍生物的反应,其工作原理如图所示。下列说法不正确的是( )

A.该材料的吸附作用具有选择性
B.该方法的广泛使用有助于减少CO2排放
C.在生成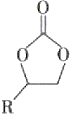 的过程中,有极性共价键形成
的过程中,有极性共价键形成
D.其工作原理只涉及化学变化
-
兰尼镍是一种带有多孔结构的细小晶粒组成的镍铝合金,被广泛用作有机物的氢化反应的催化剂。以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的工艺流程如下图所示:
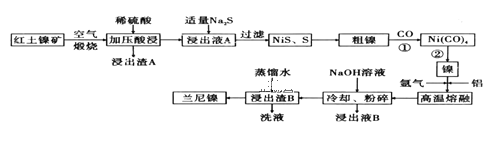
(1)煅烧时主要生成的气体产物是___________,浸出渣A的主要成分是____________ 。
(2)向浸出液A中加入适量Na2S,发生氧化还原的离子方程式为________________________。若Na2S过量时,则过滤出的固体中会混有__________;
(3)已知Ni(CO)4的沸点是42.2℃,Ni(S)+CO(g) ⇌ Ni(CO)4(g)的平衡常数与温度的关系如下:
| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
步骤①、步骤②的最佳温度分别是_______、_______(填选项代号)
A. 25℃ B. 30℃ C. 50℃ D. 80℃ E. 230℃
(4)加氢氧化钠的目的是溶解部分铝,形成多孔结构的镍铝合金,已知红土镍矿中NiS质量分数45.5%,取1Kg红土镍矿进行制备(不考虑制备过程中镍的损耗),熔融时加入270g铝,浸出时消耗800mL 5mol/LNaOH,理论上生成的兰尼镍的化学式为 __________。
-
兰尼镍是一种带有多孔结构的细小晶粒组成的镍铝合金,被广泛用作有机物的氢化反应的催化剂。以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的工艺流程如下图所示:

(1)在形成Ni(CO)4的过程中,碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为___________;
(2)已知红土镍矿煅烧后生成Ni2O3,而加压酸浸后浸出液A中含有Ni2+,写出有关镍元素的加压酸浸的化学反应方程式______________________;
(3)向浸出液A中通入H2S气体,反应的离子方程式是____________________;
(4)“高温熔融”时能否将通入氩气换为CO并说明原因_____________________;
(5)“碱浸”的目的是使镍铝合金产生多孔结构,从而增强对氢气的强吸附性,此过程
中发生反应的离子方程式为___________________。浸出反应所用的NaOH溶液的浓度要大,若NaOH溶液较稀时,则会产生少量的Al(OH)3沉淀而阻止浸出反应的持续进行,请用化学反应原理加以解释:________________________。
(6)浸出液B可以回收,重新生成铝以便循环利用。请设计简单的回收流程:
浸出液B→________________________。(示例:CuOCu2+Cu)












 的过程中,有极性共价键形成
的过程中,有极性共价键形成
 的过程中,有极性共价键形成
的过程中,有极性共价键形成
